Clear Sky Science · ar
ZFP57 هو منظم للنمو بعد الولادة والصحة مدى الحياة
كيف يشكل الحليب المبكر الصحة مدى الحياة
ما يحدث في الأيام الأولى من الحياة يمكن أن يتردد صداه لعقود. تُظهر هذه الدراسة أن بروتينًا أموميًا واحدًا، يدعى ZFP57، يساعد في تحديد مدى تطور الغدة الثديية، ومكونات حليب الثدي، وكيف ينمو الصغار ويتعاملون مع الطاقة لبقية حياتهم. من خلال تتبع تأثير هذا البروتين من الأم الحامل إلى الجراء المُرضَّعة، يكشف الباحثون عن طبقة جينية مخفية تحت الفوائد المعروفة للتغذية المبكرة.
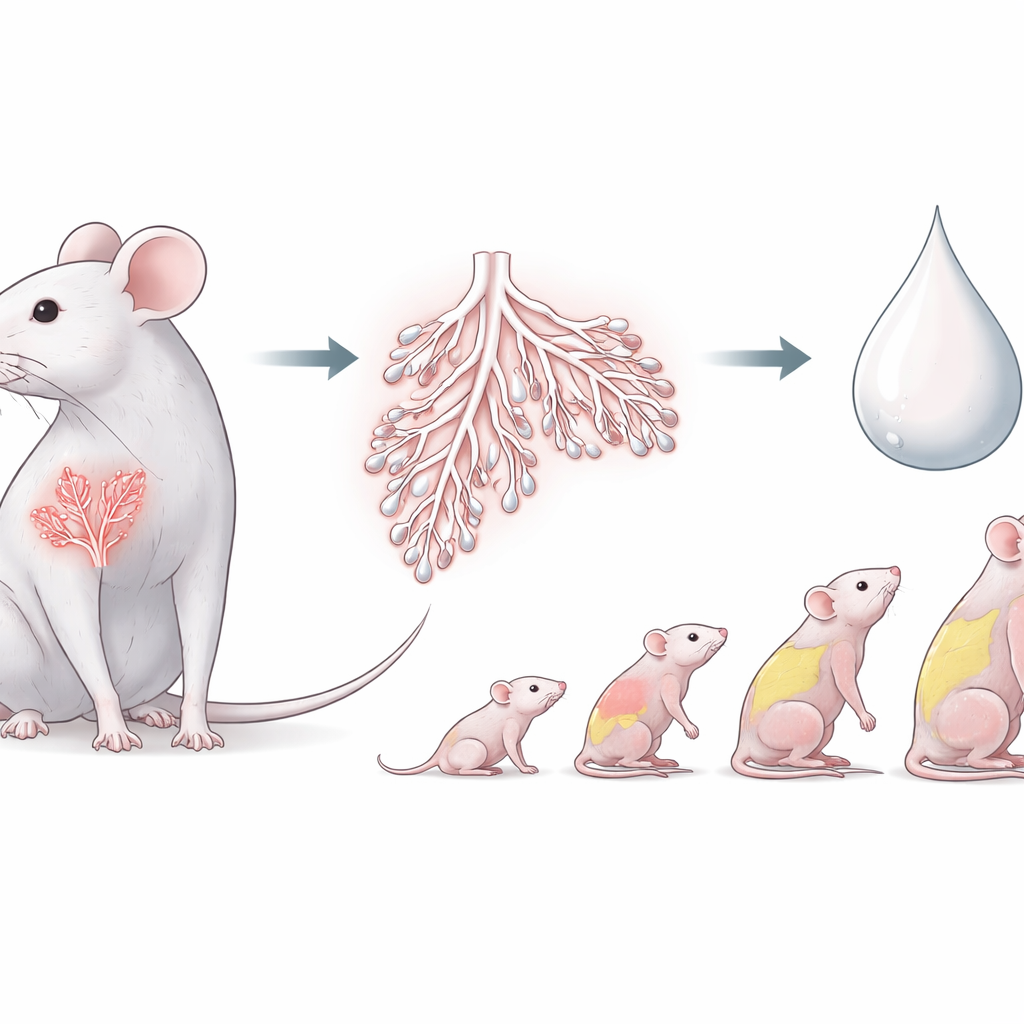
حارس للنمو قبل وبعد الولادة
كان ZFP57 معروفًا بالفعل كمنظم رئيسي لـ «الطبع الجينومي»، وهو نظام وضع علامات كيميائية يخبر بعض الجينات سواء كانت وراثتها من الأم أو الأب. هذه العلامات ضرورية للنمو الطبيعي قبل الولادة. العمل الجديد يتساءل عما إذا كان ZFP57 يهم أيضًا لاحقًا، بعد الولادة، عندما تُرضع الأمهات صغارهن عبر الحليب. باستخدام الفئران، يظهر المؤلفون أن ZFP57 نشط ليس فقط في الأجنة والمشيمة، بل أيضًا في أنسجة البالغين، بما في ذلك الدماغ والغدة الثديية. وهذا يشير إلى أن الجزيء نفسه الذي يساعد في التحكم في نمو الجنين قد يساهم أيضًا في إدارة التغذية بعد الولادة.
كيف تُبرمج غدة الأم للرضاعة
فحص الفريق الغدد الثديية لفئران إناث طبيعية ونقصانة لـ Zfp57 عبر مراحل رئيسية: قبل الحمل، وخلال الحمل، وفترة الرضاعة المبكرة. فرزوا أنواع خلايا مختلفة وقرأوا مستويات نشاط آلاف الجينات. بينما استمر تطور الغدة بشكل عام، كانت التفاصيل الدقيقة مختلفة عندما غاب ZFP57. قبل الحمل، أظهرت الغدد الطافرة تشعبًا أكثر كثافة وتفعيلًا مبكرًا لجينات تُشغل عادة في مراحل لاحقة للتحضير لإنتاج الحليب. خلال الحمل، انقلب النمط: انخفضت التشعبات ونشاط الجينات المتعلقة بالحليب، وخضعت العديد من الخلايا لموت مبرمج. هذه التغيرات عطلت التوازن بين أنواع الخلايا التي تبني وتحافظ على عضو منتج للحليب صحي.
جودة الحليب، أنماط النمو، والأمهات غير المتطابقة
تُرجمت هذه التغيرات البنيوية والجزيئية إلى حليب ومجموعة صغار مختلفين. أنتجت الأمهات الناقصة لـ Zfp57 حليبًا بمستويات أعلى من الدهون المؤكسدة ومستويات أقل من بعض الفسفوليبيدات التي تساعد في تغليف الدهون داخل قطرات. الجِراء المُرضَّعة من هذه الأمهات، بغض النظر عن جيناتها الخاصة، نما في البداية أبطأ وفشل بعضها في الازدهار. ومع ذلك، مجموعة واحدة من الصغار، تحمل طفرة محددة في Zfp57 وتطورت في أرحام ناقصة لـ Zfp57، استجابت بشكل مختلف جدًا: فعلى الرغم من مشاكل الرضاعة المبكرة وتأخر مظهر تناول الحليب، اكتسبت وزنًا مفرطًا خلال فترة الرضاعة. كشفت تجارب تبديل الأمومة، حيث تم تبادل الولدان بين أمهات ذات جينات مختلفة، أن النمو كان الأفضل عندما تطابق الخلفية الجينية للأم المُرضِّعة الظروف التي اختبرها الصغير في الرحم. عندما رعي جرٌّ تكيف مع بيئة أمومية واحدة لدى أم جينية مختلفة، غالبًا ما اندفع نموهم واستقلابهم نحو نهايات متطرفة.
من التغذية المبكرة إلى أيض البالغ
لم تنته القصة عند الفطام. تابع الباحثون الفئران لمدة ستة أشهر، ما يعادل تقريبًا مرحلة البلوغ المبكر لدى الإنسان. أظهر الصغار الذين تطوروا في أمهات ناقصة لـ Zfp57 وحملوا النسخة المعدلة من Zfp57 تغيرات دائمة: زيادة في دهون الجسم، انخفاض في الكتلة الخالية من الدهون، واعتماد أقوى على حرق الدهون بدلًا من الكربوهيدرات، حتى وهم على نفس النظام الغذائي المعتاد كالمجموعة الضابطة. كما أن بعضهم أزال السكر من الدم بكفاءة أقل، وهو علامة على ضعف تحمل الجلوكوز المرتبط بمتلازمة التمثيل الغذائي. ولاحظ الباحثون أن هذه المشكلات الطويلة الأمد كانت أسوأ عندما تم رعاية مثل هؤلاء الصغار لدى أمهات طبيعيات، ما يبرز كيف يمكن لعدم التوافق بين البيئة ما قبل الولادة والتغذية ما بعد الولادة أن يرسخ مسارات صحية غير مرغوبة.
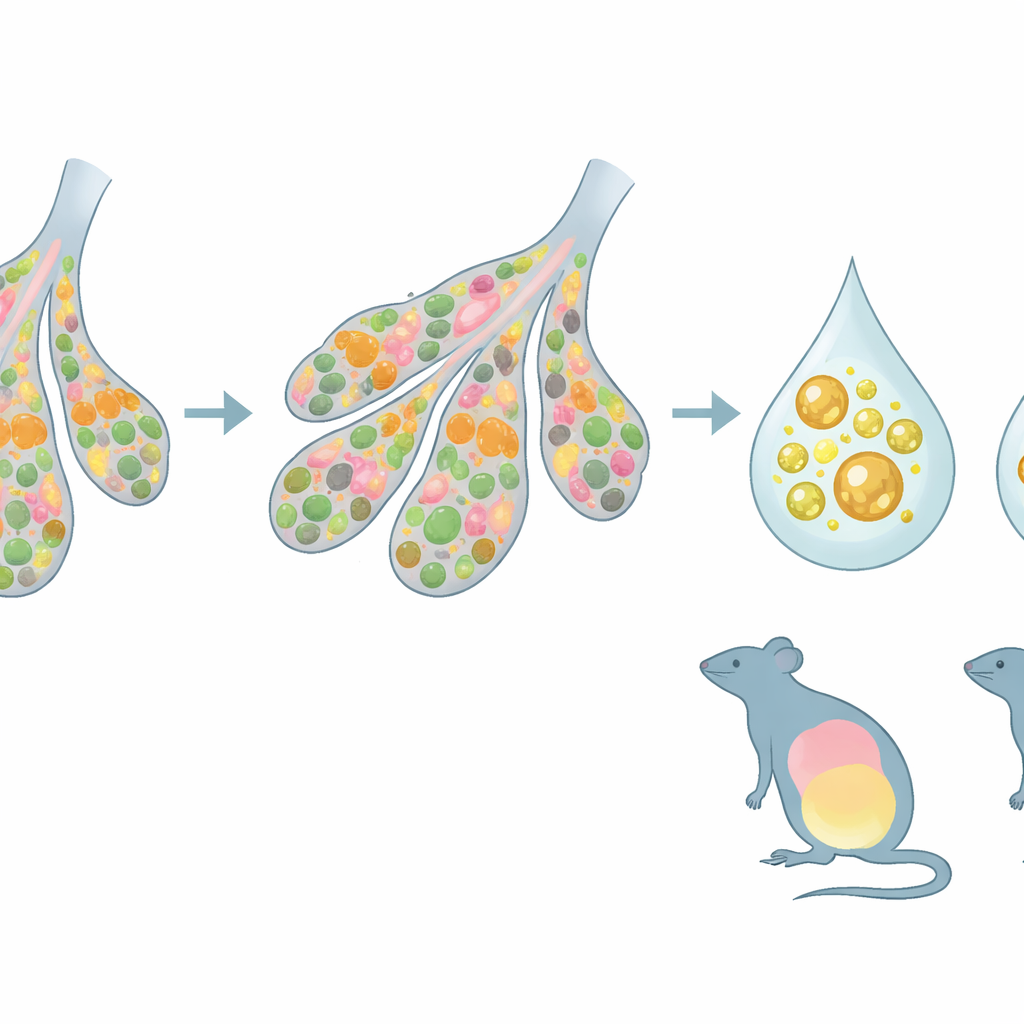
لماذا يهم هذا للصحة البشرية
من خلال الكشف عن دور لـ ZFP57 في تشكيل وظيفة الغدة الثديية وتركيب الحليب، مستقلاً عن واجباته الكلاسيكية في الطبع الجينومي، يربط هذا العمل جينًا أموميًا بالتحكم في الموارد قبل وبعد الولادة على حد سواء. يدعم ذلك الفكرة القائلة بأن الأمهات والصغار متكيّفون جينيًا: بيئة الرحم وإمداد الحليب مضبوطان لبعضهما، وخرق هذا التوافق يمكن أن يكون له تكاليف دائمة. وعلى الرغم من أن الدراسة أُجريت في الفئران، فإن ZFP57 مهم أيضًا لدى البشر، حيث ترتبط طفراته بمشكلات أيضية في وقت مبكر من الحياة. تشير النتائج إلى أن بعض المخاطر مدى الحياة للسمنة والسكري قد تنشأ ليس فقط من النظام الغذائي نفسه، بل من كيفية إعداد جيناتنا للتغذية المبكرة ومدى توافق البيئتين قبل وبعد الولادة.
الاستشهاد: Hanin, G., AlSulaiti, B., Costello, K.R. et al. ZFP57 is a regulator of postnatal growth and life-long health. Nat Commun 17, 2080 (2026). https://doi.org/10.1038/s41467-026-68608-9
الكلمات المفتاحية: تغذية في وقت مبكر من الحياة, تعديل جيني فوقي, غدة ثديية, صحة أيضية, الطبع الجيني الجينومي