Clear Sky Science · ar
توسيع نطاق الحمولات في الروابط الدوائية المضادة للأجسام عبر إيصال الأدوية الحاوية على مجموعات هيدروكسي من خلال فوسفوراميدات قابلة للتحلل الذاتي
صواريخ أكثر ذكاءً ضد السرطان
يمكن أن تكون أدوية السرطان قوية للغاية، لكن تأثيرها غالباً ما يشبه القصف الشامل: فهي تصيب الأنسجة السليمة تقريباً بنفس شدة الأورام. اخترعت روابط الجسم-الدواء المضادة (ADCs) لحل هذه المشكلة عبر ربط دواء قوي بجسم مضاد يتوجه نحو خلايا السرطان، محولاً العلاج إلى صاروخ موجه. يوضح هذا المقال «قابس» كيميائي جديد بين الجسم والدواء يجعل هذه الصواريخ أكثر دقة ومرونة، فاتحاً الباب أمام أنواع أكثر بكثير من أدوية السرطان عما تستطيع ADCs الحالية حمله.
لماذا تظل الأدوية الموجهة الحالية محدودة
تتألف ADCs من ثلاثة أجزاء: جسم مضاد يتعرف على علامة على خلايا السرطان، ودواء سام («الحمولة»)، وموصل كيميائي يربطهما. تعتمد معظم ADCs المعتمدة على عدد محدود من أنواع الحمولات التي تلحق الضرر بالحمض النووي أو تعيق انقسام الخلايا بطرق متشابهة. أحد الأسباب الرئيسية هو الموصل: يجب أن يحمل الدواء بقوة أثناء دوران ADC في مجرى الدم، ثم يطلقه بشكل نظيف داخل خلية الورم. تعمل الموصلات الحالية بشكل جيد فقط مع مجموعات كيميائية محددة على الأدوية، خاصة الأمينات، وغالباً ما تواجه صعوبة مع العديد من الأدوية التي تحتوي على مجموعات هيدروكسيل (–OH). هذا يترك عدداً هائلاً من العوامل العلاجية الواعدة على الرف لأنها لا يمكن توصيلها بأمان أو بكفاءة بتصاميم ADC الحالية.
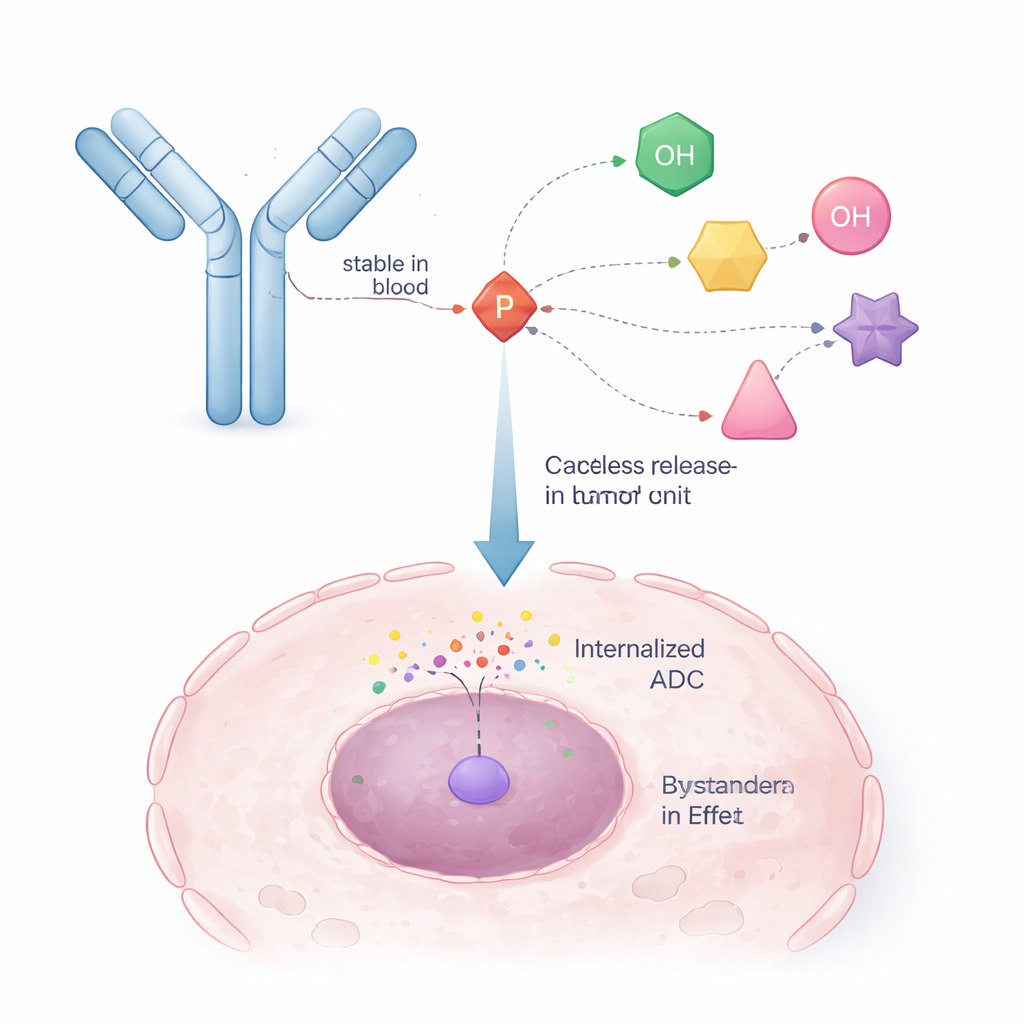
اقتباس حيلة من أقراص مضادة للفيروسات
لجأ الباحثون إلى استراتيجية مثبتة بالفعل في الأدوية المضادة للفيروسات تُدعى ProTides. في تلك الأدوية، تخفي وحدة كيميائية قائمة على الفسفور مؤقتاً مجموعة الفوسفات المشحونة في الدواء حتى تتمكن من دخول الخلايا، ثم تتحلل داخلياً لإطلاق الشكل النشط. أعاد المؤلفون هندسة هذا المفهوم بحيث يُستخدم أحد أذرع نواة الفسفور للارتباط بالجسم المضاد، بينما تحمل الأذرع الأخرى دواء السرطان. هذا يخلق موصلاً «قابلاً للتحلل الذاتي»: بمجرد أن يقطع مُحفز داخلي (مثل إنزيم داخل خلية الورم) جزءاً صغيراً من البنية، ينهار مركب الفسفور بطريقة محكومة ويطلق جزيء الدواء الأصلي مع استعادة مجموعة الهيدروكسيل دون تعديل.
بناء قابس كيميائي متعدد الاستخدامات
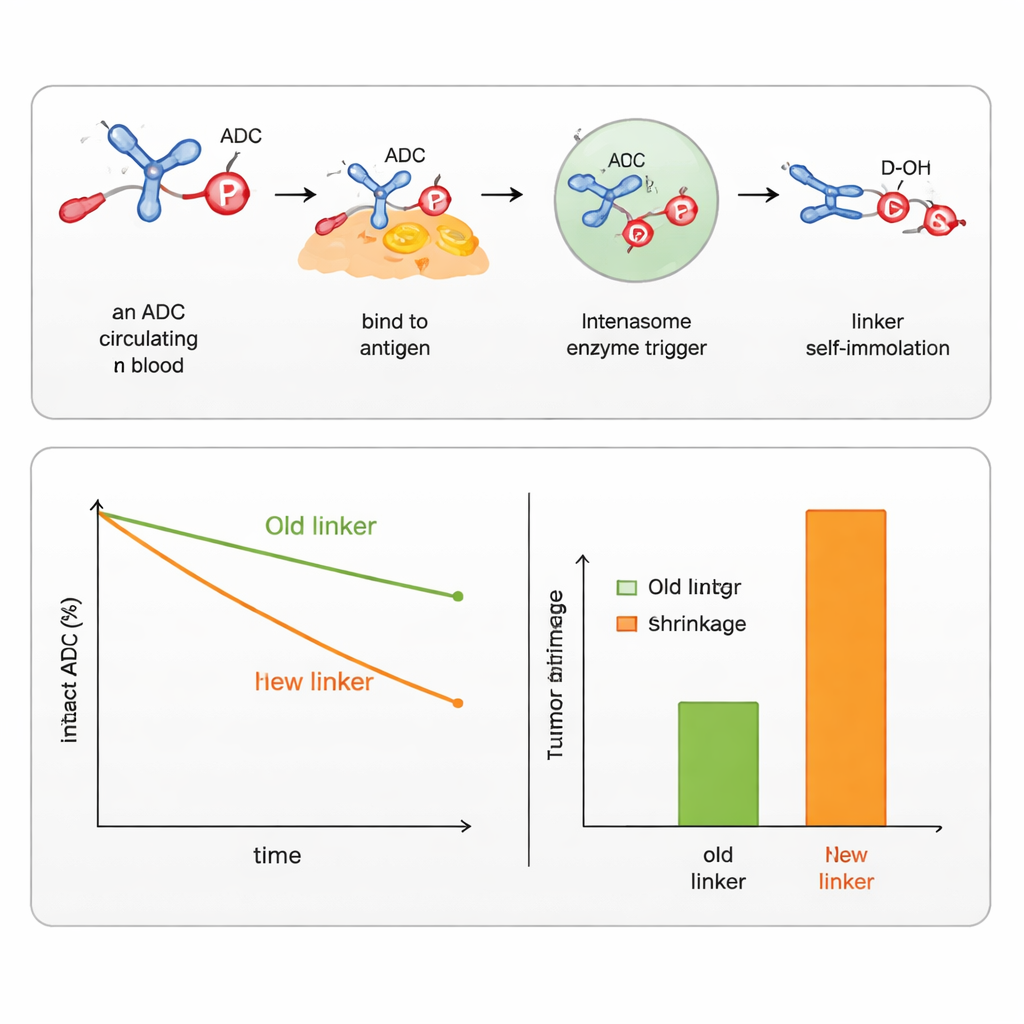
أظهر الفريق أنه عبر تعديل المجموعات المحيطة بذرة الفسفور يمكنهم ضبط مدى استقرار الموصل في الدم وسرعة تحلله داخل الخلايا. صمموا نسخاً تستجيب لأنواع متعددة من المحفزات الشائعة داخل خلايا السرطان، بما في ذلك الاسترازات والبروتيازات (إنزيمات تقطع روابط محددة)، وكذلك إنزيمات تتعرف على مجموعات سكرية أو ظروف اختزالية في حيزات الخلية. باستخدام هذه التصاميم، نجحوا في ربط وإطلاق كل من الكحولات العطرية (مثل العلاج الكيميائي SN38) والكحولات الأليفاتية (مثل DXd، الحمولة الموجودة في ADC معتمد لعلاج سرطان الثدي). مقارنة وجهًا لوجه مع الموصلات التجارية الحالية لـ SN38 وDXd، حافظت موصلات الفوسفوراميدات الجديدة على بقاء الأدوية مرتبطة لفترة أطول في المصل، وناولت كمية أكبر من الدواء إلى الأورام، وأنتجت تقلصاً أقوى للأورام في الفئران، مع إظهار تأثير أقل على الخلايا السليمة.
فتح الباب للعديد من حمولات أدوية السرطان الجديدة
لاختبار مدى تعميم استخدام الموصل، جمع الباحثون ADCs تحمل عشرة أدوية مختلفة كلها تحتوي على الأقل على مجموعة –OH واحدة لكنها تعمل بطرق مختلفة داخل خلايا السرطان. شملت هذه مثبطات تركيب الحمض النووي، وطَيّ البروتين (HSP90)، وأيضاً استقلاب الطاقة (NAMPT وDHODH)، وترجمة البروتين، إضافة إلى عوامل معروفة مثل باكليتاكسيل وجيمسيتابين. على الرغم من التنوّع الكبير في البنى، تمكنوا من تصنيع ADCs متجانسة بتحميل دوائي عالي لجميعها. في دراسات خلوية عبر أنواع سرطان متعددة، أظهرت معظم هذه ADCs فعالية بنطاق النانومولار أو حتى دون النانومولار وانتقائية واضحة للخلايا التي تعبّر عن الهدف المناعي، مؤكدة أن الموصل قادر بشكل متسق على إطلاق الدواء النشط داخل الخلايا المناسبة.
جيمسيتابين كنموذج توضيحي
جيمسيتابين علاج كيماوي مستخدم على نطاق واسع، لكن صورته التقليدية تُطرد من الجسم بسرعة بحيث يضطر المرضى لتلقي جرعات كبيرة ومتكررة، ما يقيّد الكمية الممكن إعطاؤها بأمان. باستخدام موصل الفوسفوراميد، ربط المؤلفون الجيمسيتابين بجسم مضاد يستهدف HER2 إما عند أحد موضيعي الهيدروكسيل أو الآخر وأظهروا أن كلا النسختين استعادتا النشاط الكامل بمجرد دخولهما خلايا السرطان. في نماذج الفئران ذات الأورام الإيجابية لـ HER2، أدت جرعة واحدة من ADC الجيمسيتابين — تحوي نحو ألف مرة أقل من إجمالي الجيمسيتابين مقارنة بنُظم الدواء الحر التقليدية — إلى سيطرة قوية وانتقائية على الورم. كان سلوك ADC في مجرى الدم مطابقاً تقريباً لسلوك الجسم المضاد العاري، وتحمَّلَت الجرعات العالية جيداً في الجرذان، مما يوحي بهامش أمان واسع.
ماذا يعني هذا لعلاج السرطان في المستقبل
لغير المتخصصين، الرسالة الأساسية هي أن هذا العمل يقدم موصلاً كيميائياً جديداً وقابلاً للتكيّف بدرجة كبيرة يتيح للأجسام المضادة حمل مجموعة أوسع بكثير من أدوية السرطان من قبل، وبأمان أكبر. من خلال ضمان بقاء الأدوية ملتصقة أثناء تداوُلها وإطلاقها نظيفاً فقط بعد أن يتم جر ADC داخل خلية سرطانية، تحسّن موصلات الفوسفوراميد مقدار الدواء الذي يصل إلى الورم وتقلل الأضرار الجانبية للأنسجة السليمة. وبقدر الأهمية نفسها، تسمح هذه الموصلات بإعادة توظيف الأدوية الجزيئية الصغيرة القوية الموجودة بالفعل — ذات أشكال وآليات عمل مختلفة — كعلاجات موجهة. قد يوسّع هذا بشكل كبير قائمة ADCs المتاحة للمرضى ويساعد في مكافحة الأورام التي أصبحت مقاومة لمجموعة الحمولات المحدودة الحالية.
الاستشهاد: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
الكلمات المفتاحية: روابط الجسم-الدواء المضادة, توصيل أدوية السرطان, روابط قابلة للتحلل الذاتي, كيمياء الفوسفوراميدات, العلاج الكيميائي الموجه