Clear Sky Science · ar
التسيّج بالليجاند للتحكم في موقع التفاعل وتحديد الإتّجاه المرآتي في سيانَة C–H للأمينات الثانوية
لماذا تؤثر تغييرات صغيرة في الروابط على أدوية كبرى
تحتوي العديد من الأدوية الأكثر مبيعًا على لبنات بناء صغيرة تعتمد على النيتروجين تُدعى أمينات. التغييرات الطفيفة في كيفية اتصال الذرات حول هذه الأمينات يمكن أن تحول دواء ضعيفًا إلى علاج قوي ودقيق — أو إلى مادة غير فعالة أو حتى ضارة. تصف هذه الورقة طريقة جديدة لتعديل هذه اللبنات الأمينية حسب الرغبة، مما يتيح للكيماائيين اختيار الموضع الدقيق على الجزيء الذي يتفاعلون فيه وأي شكل مرآتي (مِرآة ضوئية) يصنعون، وهذان الأمران أساسيان لتصميم أدوية أكثر أمانًا وفعالية.
اختيار موقع واحد على جزيء مزدحم
غالبًا ما تحتوي الأمينات في الأدوية على عدة روابط كربون–هيدروجين (C–H) متشابهة للغاية تتصرف في العادة بنفس الشكل تقريبًا. يرغب الكيميائيون في استبدال واحد فقط من تلك الذرات الهيدروجينية بمجموعة مفيدة، مثل مجموعة السيانو (–CN)، دون إِحداث تغيّر في باقي الجزيء. هذا صعب لأن التفاعلات القياسية تميل إلى الحدوث في أكثر المواضع نشاطًا التي يحددها هيكل الجزيء، لا اختيار الكيميائي. هنا، يعمل المؤلفون مع أمينات ثانوية بسيطة ومرنة تحمل سلسلتين كربونيتين مختلفتين على النيتروجين. يوضحون أنه انطلاقًا من نفس الأمين، يمكنهم توجيه التفاعل إلى أحد موضعين مجاورين — إما بجانب مجموعة N‑methyl الصغيرة (الموقع المسمّى α′) أو إلى كربون أبعد على السلسلة الأخرى (الموقع β) — ببساطة عن طريق تغيير الليجاند المحيط بمحفز النحاس.
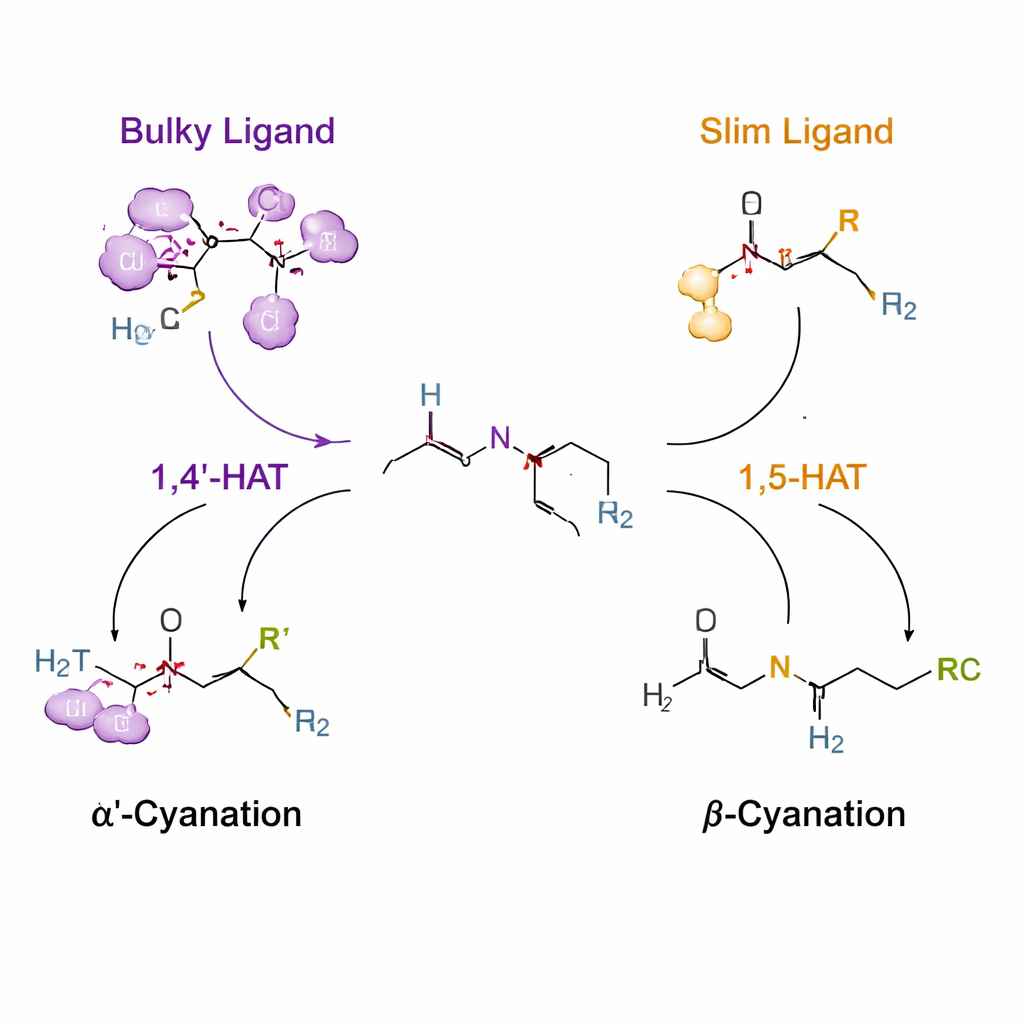
استخدام "قفزات" الهيدروجين المسيطر عليها لتوجيه التفاعلية
الحيلة الأساسية تعتمد على عملية تُدعى نقل ذرة الهيدروجين (hydrogen atom transfer)، حيث يقوم رادكال قصير العمر متمركز على النيتروجين بانتزاع هيدروجين من كربون قريب. عادةً ما تُفضّل مثل هذه الرادكالات مسافة معينة، مفضلةً الوصول ذي الحلقة المكونة من ستة أعضاء المعروف باسم 1,5‑HAT. يقوم المؤلفون بإرفاق ذراع مؤقت من يوريا وكلور للجزيء الأميني بحيث، تحت تحفيز النحاس، يتكوّن هذا الرادكال النيتروجيني ويمكنه انتزاع الهيدروجين إما من الموقع α′ أو من الموقع β. عبر تصميم ليجاندات — جزيئات عضوية تحيط بالنحاس — يعيدون تشكيل بيئة الرادكال. ليجاند ضخم جدًا (اسمه L14) يدفع النظام نحو خطوة 1,4′‑HAT غير المألوفة التي تستهدف مجموعة N‑methyl، مما يعطي سيانة انتقائية في الموقع α′. أما الليجاندات الأرفع (مثل L8) فتتيح المسار التقليدي 1,5‑HAT، موجهةً التفاعل إلى الموقع β بدلاً من ذلك.
من التحكم بالموقع إلى التحكم باليدوية
بعيدًا عن اختيار موقع التفاعل، يسعى الفريق أيضًا للتحكم في اليدوية أو التيميّز اليدوي (الشللية)، وهو أمر حيوي لأن العديد من الأدوية توجد على هيئة أشكال يسرى ويسرى‑عكسية تتصرف بشكل مختلف في الجسم. لتحقيق ذلك، يدخلون ليجاندات كيرالية — جزيئات لها شكل مِسَلّي — في معقّد النحاس. يعطي ليجاندان من هذا النوع، L24 وL41، تفضيلًا عاليًا لصورة مرآتية واحدة عندما يثبّت التفاعل مجموعة السيانو في المواقع β، بما في ذلك المواقع البينيّة الملاصقة للحلقات العطرية (benzyllic) والمواقع الحفيفة بجانب روابط مزدوجة كربون‑كربون (allylic). عبر طيف واسع من المواد الأولية الأمينية، توفّر الطريقة منتجات β‑سيانية بانتقائية ممتازة لكل من الموقع واليدوية، وتعمل على مقياس غرامي، ما يدل على أن العملية عملية ومتماسكة للتطبيق في التوليف.
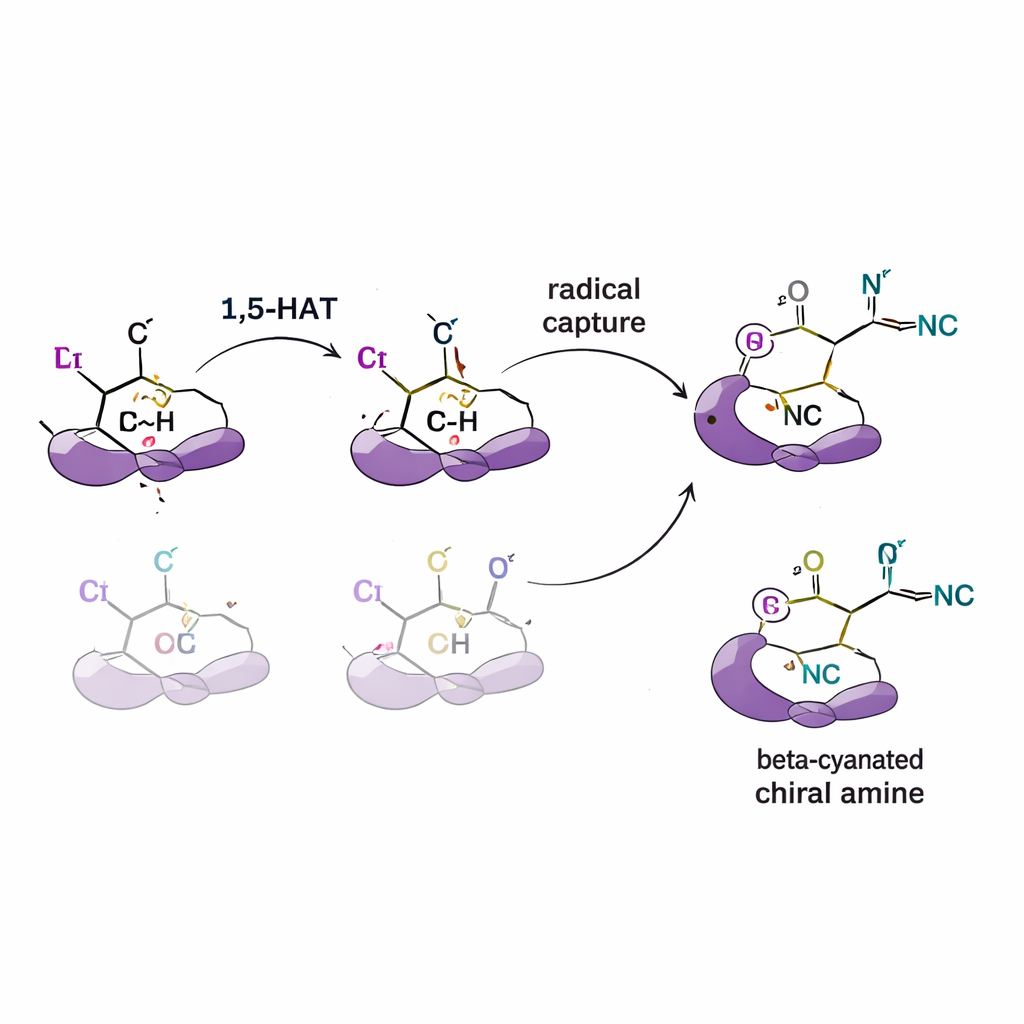
اختبار الآلية وراء الانتقائية
لفهم كيفية نشوء هذا التحكم، ينفذ المؤلفون سلسلة تجارب آليّة. بإضافة "مصائد" للرادكالات، يؤكدون أن وسطًا بينيًا راديكاليًا تفاعليًا متورط بالفعل. باستخدام مواد أساس فيها بعض ذرات الهيدروجين مستبدلة بالديوتيريوم (شكل أثقل من الهيدروجين)، يكتشفون تأثيرات نظائر حركية تشير إلى أن خطوة نقل الهيدروجين هي الخطوة البطيئة والتي تحدد الانتقائية. تُظهر تجارب التعليم أيضًا أن الهيدروجين يتحرك في خطوة واحدة باتجاه واحد بدل التبادل ذهابًا وإيابًا بين المواضع. تدعم محاكاة حاسوبية مكملة (نظرية الدوال الكثافة) هذه النتائج، مشيرةً إلى أن شكل وحجم الليجاند يغيّر طاقة مسارات نقل الهيدروجين المتنافسة وطريقة اتحاد الرادكال بعدها مع النحاس والسيانيد لتكوين صورة مرآتية مفضلة.
ما الذي يعنيه هذا لتصميم الأدوية المستقبلية
بشكل عام، تقدم هذه الدراسة استراتيجية مرنة لإعادة هندسة مجموعات الأمين الشائعة في موضعين مرتبطين ارتباطًا وثيقًا، عند الطلب، مع تحكم دقيق في التيميّز الجزيئي. بتبديل الليجاند على محفز النحاس فقط، يمكن للكيميائيين اختيار ما إذا كانوا سيضعون مجموعة السيانو على وحدة N‑methyl الصغيرة أم على الكربون المجاور لسلسلة جانبية مختلفة، ويمكنهم فعل ذلك عبر العديد من الجزيئات المعقدة الشبيهة بالأدوية. وبما أن مجموعات السيانو تشكل نقاط انطلاق ثمينة للانتقال إلى العديد من المجموعات الوظيفية الأخرى، فإن هذا النهج "ضبط‑الموقع" و"ضبط‑اليد" من شأنه أن يسهل استكشاف وتحسين أدوية جديدة مبنية على نفس الهياكل الأمينية الأساسية.
الاستشهاد: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
الكلمات المفتاحية: تعديل الأمينات, نقل ذرة الهيدروجين, التحفيز بالنحاس, السيانة الانتقائية الإنانتيو مريّة, كيمياء دوائية