Clear Sky Science · ar
إنزيم حديدي أحادي النواة شديد الديناميكية لصناعة الإيزونيتريل على مرحلتين
كيف تبني البكتيريا أدوات كيميائية غريبة
الإيزونيتريلات مجموعات كيميائية صغيرة لكنها قوية، تتصرف كالموس السويسري: يمكنها التقاط المعادن، والتفاعل بطرق متعددة، وغالباً ما تعمل كـ«رأس ضارب» في مضادات حيوية وسموم طبيعية فعالة. بعض البكتيريا الممرِضة، بما في ذلك مسبب السل المتفطرة السلية، تُرفق الإيزونيتريل بسلاسل دهنية لمساعدتها في نَهْب المعادن من العائل. تستعرض هذه المقالة كيف ينجز أحد إنزيماتهم، المسمى Rv0097، هذه الكيمياء الصعبة على مرحلتين مُنسقتين بعناية.
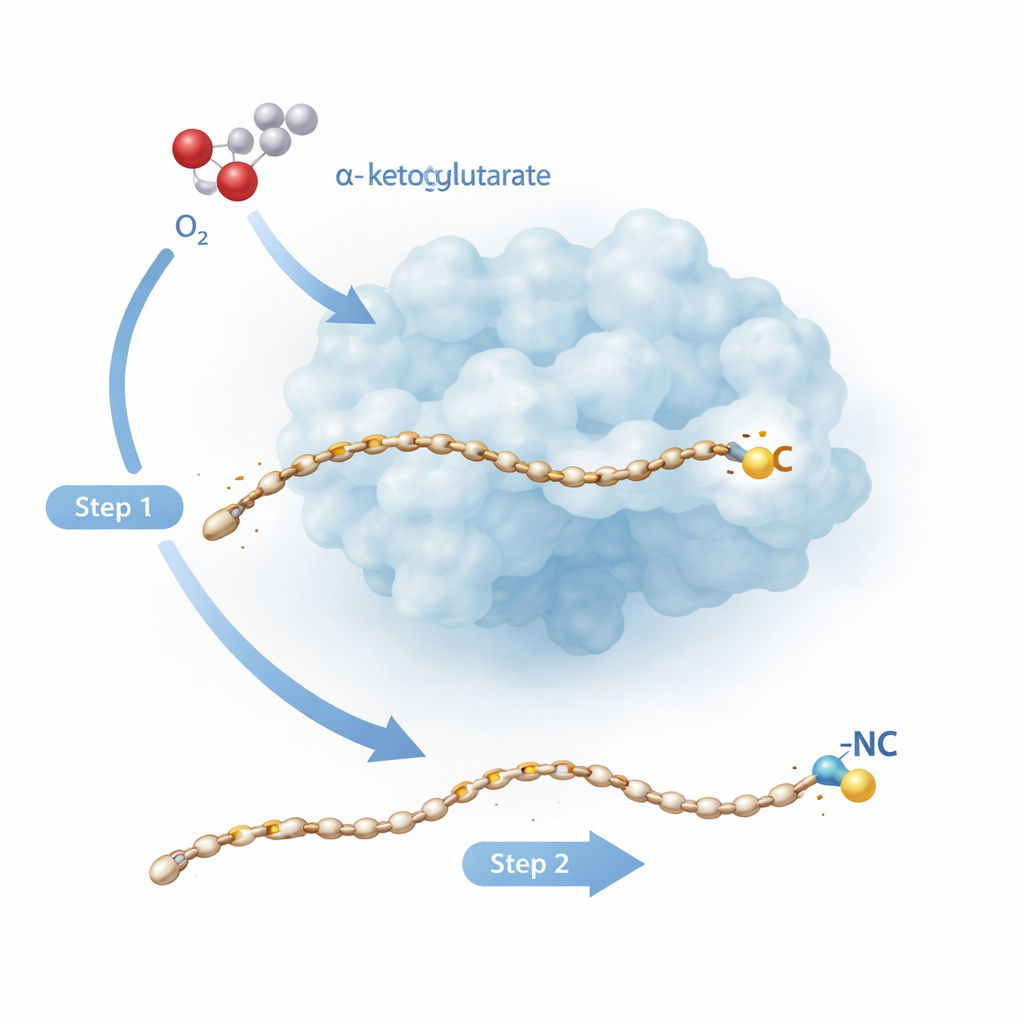
تحوّل جزيئي من مرحلتين
ينتمي Rv0097 إلى عائلة كبيرة من الإنزيمات المعتمدة على الحديد التي عادةً ما تقوم بمهام أبسط مثل إضافة الأكسجين لموضع واحد في جزيء. هنا، المهمة أصعب: بدءاً من لبنة بناء «غليسيل–حمض دهني»، يجب على الإنزيم إنشاء مجموعة إيزونيتريل جديدة كلياً، مع كلتا الذرتين الرئيسيتين—الكربون والنيتروجين—القادمتين من نفس جزء الغليسين الصغير. أبحاث سابقة على إنزيم ذي صلة، ScoE، اقترحت أن هذا لا يمكن إنجازه ضربة واحدة؛ بدلاً من ذلك هناك نصفا تفاعل منفصلان، كل منهما تعمل به حالة حديد–أكسجين تتكون عندما يحرّق الإنزيم جزيئاً مساعداً يسمى α‑كيتوجلوتارات ويدمج معه الأكسجين الجوي. تتجه الدراسة الجديدة إلى إنزيم السل Rv0097 لمراقبة، بدقة ذرية، كيف يمكن لإنزيم أن يربط هاتين الخطوتين الشديدتين على نفس الركيزة دون فقدان السيطرة.
تجميد الإنزيم أثناء الفعل
باستخدام البلورة بالأشعة السينية، التقط الباحثون ستة عشر لقطة عالية الدقة لـ Rv0097 في حالات مختلفة: خالٍ، مرتبط بركيزته الدهنية (جزيء مكون من عشرة كربونات يُدعى CADA)، مرتبط بالمساعد α‑كيتوجلوتارات، وفي تراكيب تحاكي وسائط تفاعل عابرة. تُظهر هذه البُنى أن Rv0097 يمتلك شخصية منقسمة. في حالة الراحة، يكون موقعه النشط مغلقاً إلى حد كبير، مع حمض أميني رئيسي (فينيل ألانين 102) يتقلب بين اتجاهين يحافظان على جيب ذيل الدهن جافاً وجاهزاً للالتصاق المحب للدهون. عند ارتباط CADA، يستقر هذا البقايا في وضع واحد وتُثبت الرأس القطبي للركيزة بسلاسل جانبية مشحونة بينما يستقر ذيلها الزيتي داخل نفق مريح. تَحَوُّر هذا الزوج البابي من البقايا (F102 وغلايسين مجاور G204) إما يسد الجيب أو يسمح بدخول ماء زائد، مما يقلّص النشاط بشكل حاد ويغيّر أطوال السلاسل التي يفضّلها الإنزيم.
أغطية متحركة وحلقات دينامية
بعيداً عن جيب الركيزة، يتصرف Rv0097 كآلة صغيرة لديها أبواب متحركة. لاحظ الفريق تبدّلات «مفتوحة» و«مغلقة» حيث يتأرجح منطقتان شبيهان بالغطاء متباعدتين أو متقاربتين فوق الموقع النشط. يكشف الفتح مركز الحديد ويخلق مساراً لدخول α‑كيتوجلوتارات والركيزة؛ أما الإغلاق فيحمي التفاعلات من الماء المحيط بمجرد بدء التفاعل. تعمل حلقتان سطحيّتان مرنتان، تُسمى حلقة الهستيدين وحلقة الأرجينين نسبةً للحموض الأمينية التي تحملانهما، كباب إضافي. في بعض البنى، تتأرجح هذه الحلقات إلى الداخل بحيث يستطيع بقايا الأرجينين الإمساك بـα‑كيتوجلوتارات؛ وفي أخرى تتأرجح إلى الخارج، مما يبدو أنه يخلق قناة جانبية يمكن أن تغادر من خلالها شظايا المساعد المستهلكة (السوكسينات وثاني أكسيد الكربون) ويَدخل α‑كيتوجلوتارات جديد للخطوة الثانية—كل ذلك بينما يبقى وسيط مشتق من الركيزة مُقفلًا في مكانه.
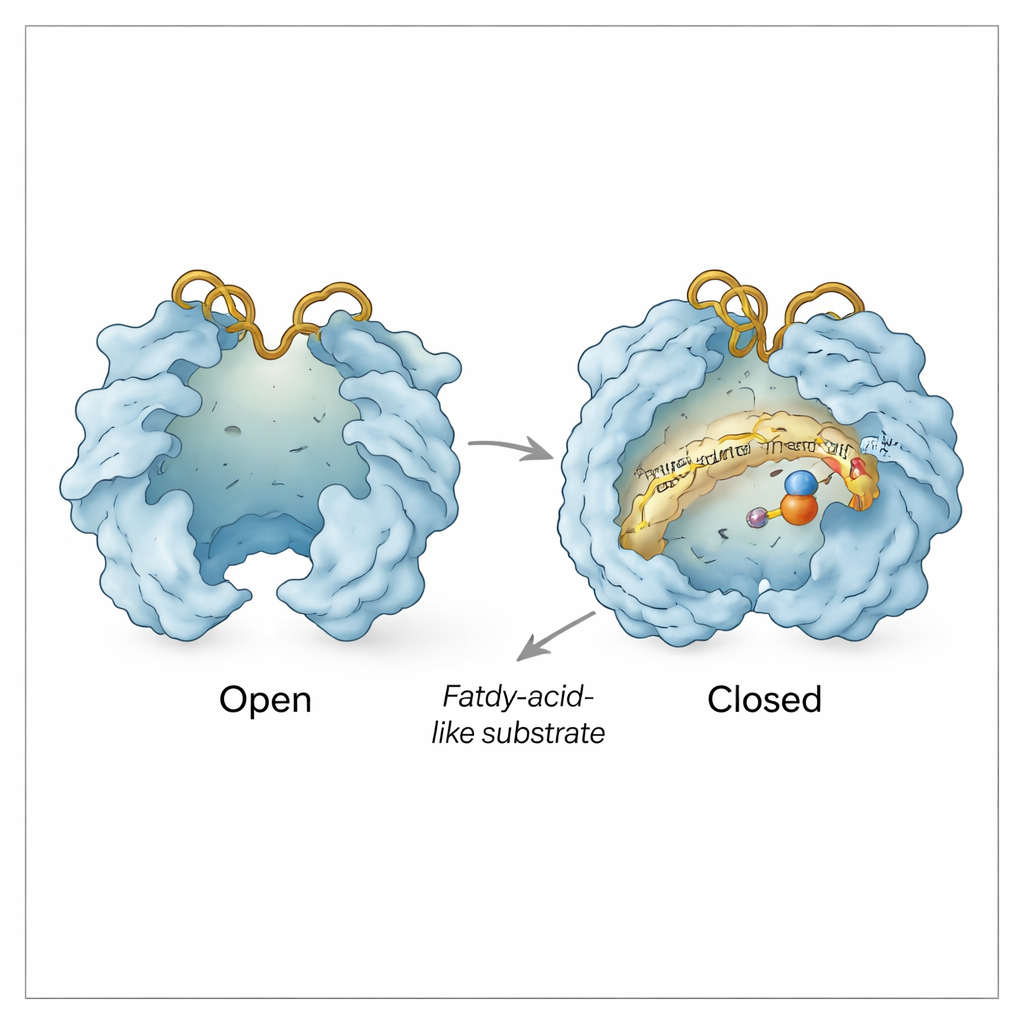
حماية وسيط هش
تدعم الاختبارات الكيميائية الحيوية هذه الصورة البِنوية. يحوّل النصف الأول من التفاعل CADA إلى وسيط إيمين شديد التفاعلية كان سيتفكك بسرعة لو انزلق إلى المحلول. من خلال احتجاز منتجه المتحلل كيميائياً، يُظهر المؤلفون أن معظم هذا الوسيط يُكشف فقط عندما يكون الإنزيم لا يزال موجوداً، ما يعني أنه يبقى مرتبطاً ومحمياً داخل Rv0097 بين النصفين التفاعليين. وتفسّر البنى كيف يحدث ذلك: إعادة تموضع دقيقة لحلقات الهستيدين والأرجينين، إلى جانب تحرّكات طفيفة لبقايا مجاورة، تبدو وكأنها تُختم الوسيط داخل تجويف محمي بينما تسمح في الوقت نفسه لجزيئات صغيرة مثل α‑كيتوجلوتارات والسوكسينات وثاني أكسيد الكربون بالتبادل عبر قنوات مُتحكّم بها.
لماذا هذا مهم للسل وما وراءه
تكشف هذه النتائج معاً أن Rv0097 خط إنتاج أحادي البروتين شديد الديناميكية يستخدم الكيمياء المعتمدة على الحديد مرتين متتاليتين على نفس الركيزة دون أن يطلق منتجاً نصفياً خطيراً إلى الخارج. بالنسبة لبكتيريا السل، تستند دقة هذه العملية إلى تصنيع جزيئات مزينة بالإيزونيتريل تساعدها في الحصول على المعادن الأساسية داخل الجسم، وتدل الدراسات الجينية على أن المسار مهم لبقائها أثناء العدوى. بالنسبة للكيميائيين ومصممي الأدوية، يقدم العمل خارطة طريق لهندسة إنزيمات ذات صلة لبناء مركبات جديدة تحتوي الإيزونيتريل، ويقترح أن تعطيل الأغطية والمفاتيح المتحركة في Rv0097 قد يكون وسيلة لتطوير مضادات حيوية جديدة.
الاستشهاد: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
الكلمات المفتاحية: تخليق الإيزونيتريل, إنزيم حديدي غير هِيمي, المتفطرة السلية (Mycobacterium tuberculosis), ديناميكية الإنزيم, مركبات طبيعية معلِّقة بالمعادن