Clear Sky Science · ar
تعطيل التوازن الحديدي يجعل سرطان البنكرياس أكثر حساسية للكهرباء القاطعة غير القابلة للانعكاس
توظيف الكهرباء والحديد ضد سرطان قاتل
يعد سرطان البنكرياس من أصعب أنواع السرطان معالجة، وحتى العلاجات الموضعية العدوانية غالباً ما تفشل في منع عودته. تستكشف هذه الدراسة طريقة جديدة لجعل إجراء قائم—التحريض الكهربائي غير القابل للانعكاس، الذي يقتل الأورام باستخدام نبضات كهربائية قصيرة وعالية الشدة—يعمل بشكل أفضل وبأمان أكبر. من خلال تعطيل ذكي لكيفية تعامل الخلايا السرطانية مع الحديد، يُظهر الباحثون أنهم يستطيعون دفع الخلايا الناجية نحو شكل مدمر من الموت، مما قد يقلل من احتمال عودة الورم.
لماذا النبضات الكهربائية وحدها غير كافية
يعالج التحريض الكهربائي غير القابل للانعكاس (IRE) الأورام عن طريق إدخال أقطاب رفيعة داخل السرطان أو حوله وإطلاق نبضات سريعة ذات جهد عالٍ. تخترق هذه النبضات أغشية الخلايا فتُحدث ثقوباً دائمة، ما يقتل العديد من الخلايا السرطانية ويحفز استجابة مناعية. لكن المجال الكهربائي ليس متجانساً تماماً. المناطق التي تتلقى نبضات أضعف قليلاً قد تترك خلايا سرطانية حية، وهذه الخلايا الناجية يمكن أن تُعيد تكوين ورم جديد. عندما فحص الفريق خلايا سرطان البنكرياس وأورام الفئران المعرضة لمجال كهربائي دون مستوي مميت، وجدوا أنه بدلاً من الموت عبر عملية تقودها الحديد تسمى الفرابتوزيس، قامت هذه الخلايا بتشغيل برنامج واسع لمكافحة الأكسدة. تم تعزيز جينات حماية رئيسية، بما في ذلك تلك التي تساعد على تحييد الضرر المرتبط بالحديد، مما سمح للخلايا بتحمّل الهجوم والتعافي.
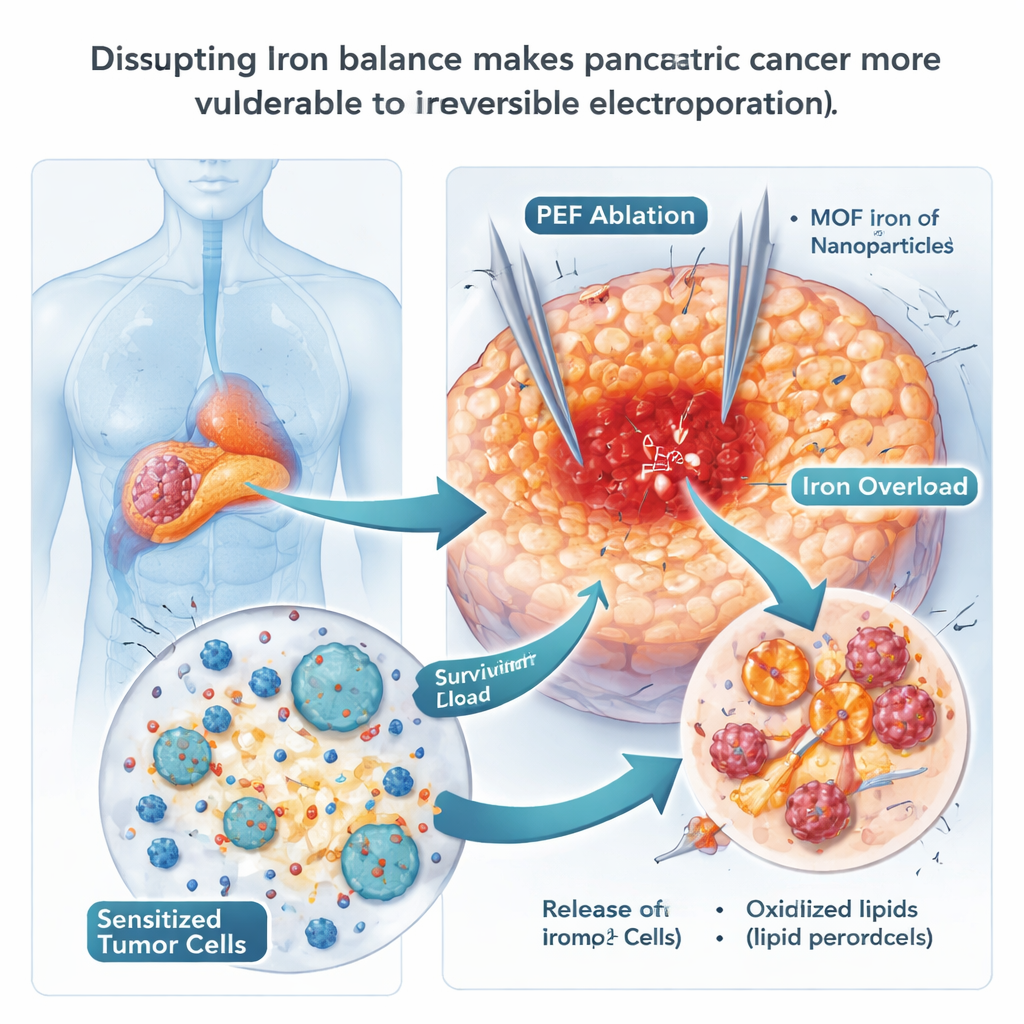
استخدام جزيئات الحديد النانوية لدفع الخلايا نحو الدمار
نظراً لاعتماد الفرابتوزيس على الحديد، اختبر العلماء ما إذا كانت الجسيمات النانوية الغنية بالحديد قادرة على دفع الخلايا السرطانية إلى حد الانهيار. استخدموا جسيمات هيكلية معدنية-عضوية مصممة خصيصاً تحتوي على الحديد (MOF-Fe)، والتي تُطلق الحديد بسرعة داخل الحويصلات الحمضية في الخلايا. في الأطباق المخبرية، تراكمت الخلايا السرطانية التي امتصت هذه الجسيمات على شكل حديد حر ودهون مؤكسدة في أغشيتها، وهي علامات تقليدية للفرابتوزيس، وتشكّلت مستعمرات أقل بكثير. في الفئران، أدى الجمع بين MOF-Fe وIRE إلى تأخير رجوع الورم لفترة أطول من أي علاج منفرد، وأظهرت الأورام مزيداً من علامات التلف التأكسدي. ومع ذلك، كان هذا التأثير مؤقتاً: بعد نحو ثلاثة أسابيع بدأت الأورام في الانتعاش، ما يشير إلى أن السرطان وجد طريقاً للتكيف مع حمولة الحديد الزائدة.
استهداف "خزنة" الحديد داخل الخلية
لفهم هذا المقاومة، حلل الفريق البروتينات التي تغيرت بعد العلاج بـMOF-Fe. برز سلاسل الفيريتين الثقيلة 1 (FTH1)، جزء من مركب تخزين الحديد في الخلية—المكافئ الجزيئي لخزنة مقاومة للحريق للحديد الزائد. عندما ارتفعت مستويات FTH1 تجريبياً، أصبحت الخلايا السرطانية أكثر مقاومة للفرابتوزيس؛ وعندما خُفضت FTH1، أصبحت أكثر عرضة. أشار ذلك إلى أن FTH1 يعمل كدرع مركزي ضد الموت الناجم بالحديد. ثم أنشأ الباحثون جزيئاً مصمماً، C20U4V، مبنياً من حمض الأراكيدونيك (دهن شديد القابلية للأكسدة) مرتبطاً بجزء قَصدي من نوع "PROTAC" الذي يوجّه بروتينات محددة نحو آلية التخلص في الخلية. في وجود MOF-Fe، ارتبط C20U4V بالفيريتين وجذبه ليُوسم ويُدمر، مما خفض مستويات FTH1 بشكل حاد ومنع الخلية من إغلاق الحديد بأمان.
من أطباق الخلايا إلى الأورجانويدات والفسلجيات الحيّة
عند دمج MOF-Fe وC20U4V، أظهرت خلايا سرطان البنكرياس ضغوطاً أكسدية أعلى، ودهون غشائية أكثر تضرراً، وميتوكوندريا أضعف، وقدرة متناقصة بدرجة كبيرة على إعادة النمو. ظهر هذا التآزر أيضاً في أورجانويدات ثلاثية الأبعاد مشتقة من مرضى حقيقيين—هياكل صغيرة شبيهة بالأورام نمت من مرضى—حيث انهارت حجم الأورجانويد وعددها بفعل الثنائي الدوائي. وبما أن C20U4V دُهني ولا يذوب في الماء، عبّأه الفريق في ميشيلات صغيرة حساسة للأكسجين التفاعلي (M-C20U4V) تستطيع الدوران في مجرى الدم وإطلاق الدواء في الأنسجة الورمية المتضررة والمجهدة. في نماذج الفئران التي وُضعت فيها أورام بنكرياس تحت الجلد وفي البنكرياس نفسه، أدى المزيج الثلاثي من IRE وMOF-Fe وM-C20U4V إلى تقلص الأورام بفعالية أكبر وإطالة البقاء مقارنة بأي علاج مفرد أو مزدوج. أظهرت الأورام المعالجة خلايا انقسامية أقل، ومؤشرات أكثر على الفرابتوزيس، وتوغلاً أكبر لخلايا T وخلايا مناعية أخرى، مما يشير إلى أن الاستراتيجية لا تقتل الخلايا السرطانية مباشرة فحسب، بل تساعد أيضاً الجهاز المناعي على التعرف على الورم ومهاجمته.
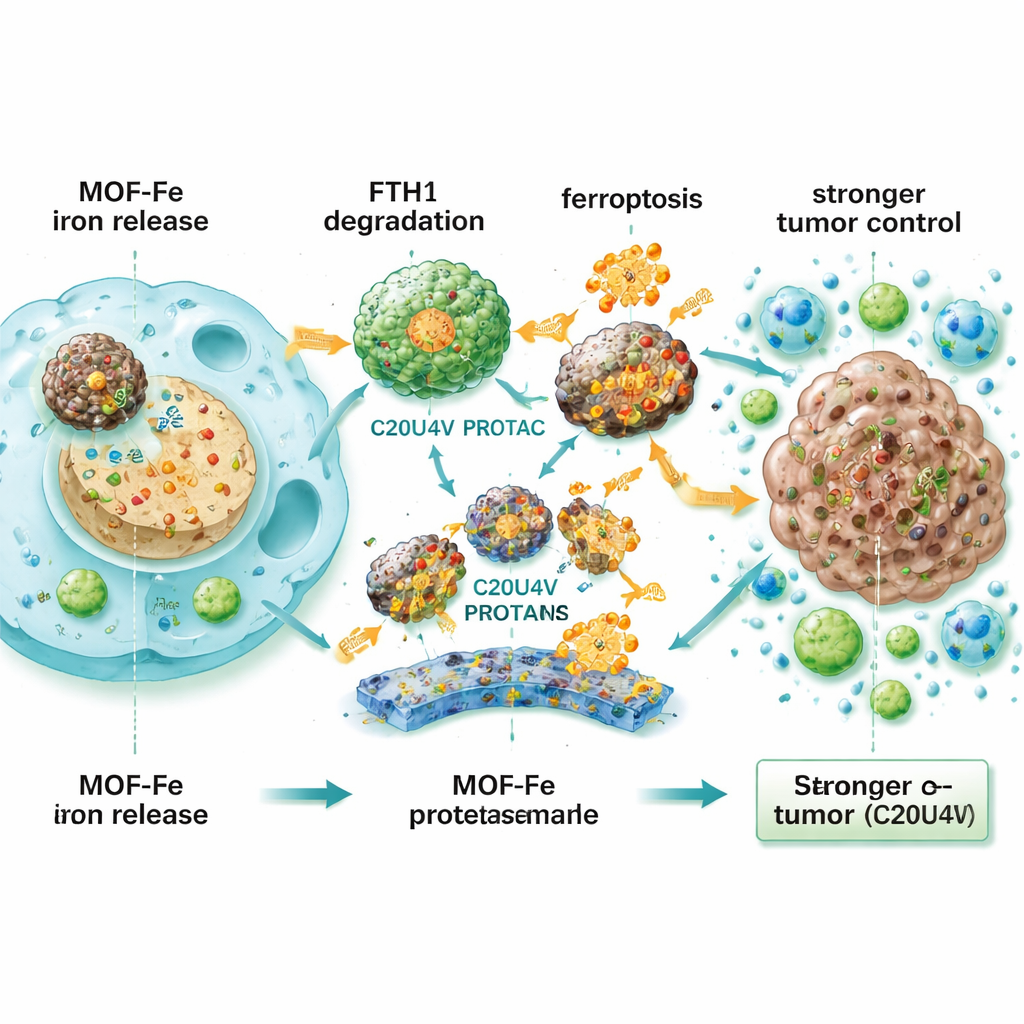
ما الذي قد يعنيه هذا للمرضى
بالنسبة لغير المتخصص، الفكرة الأساسية بسيطة: غالباً ما تهرب أورام البنكرياس بعد الاجتثاث بالنبضات الكهربائية لأن بعض الخلايا السرطانية تبقى حية وتتأقلم بسرعة. تُظهر هذه الدراسة أن تحميل تلك الخلايا بالحديد وتعطيل "قفل الأمان" الذي يخزن الحديد في الوقت نفسه يمكن أن يجبرها على الدخول في حالة ذاتية التدمير لا تستطيع مقاومتها بسهولة. بينما لا يزال هذا النهج في مرحلة تجريبية ويتطلب اختبارات واسعة للسلامة والجدوى لدى البشر، فإنه يشير إلى أن تعديل طريقة تعامل الأورام مع عنصر أساسي مثل الحديد قد يحوّل علاجاً موضعياً ناقصاً إلى ضربة أكثر حسمًا ضد أحد أخطر أنواع السرطان.
الاستشهاد: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
الكلمات المفتاحية: سرطان البنكرياس, التحريض الكهربائي غير القابل للانعكاس, الفرابتوزيس, جزيئات الحديد النانوية, علاج PROTAC