Clear Sky Science · ar
HIF يحافظ على دائرة تنظيم نسخي لتعبير EPAS1 في سرطان الكلية ذو الخلايا الصافية
لماذا يحتاج سرطان الكلية إلى نظرة أدق
سرطان الخلايا الكلوية الصافية هو الشكل الأكثر شيوعًا لسرطان الكلية، ويتلقى الآن العديد من المرضى أدوية تمنع بروتينًا يُدعى HIF‑2α. يمكن لهذه الأدوية تقليص الأورام، لكنها لا تعمل بنفس الفعالية لدى الجميع. تطرح هذه الدراسة سؤالًا بسيطًا لكنه مهم: ما الذي يجعل بعض أورام الكلية تُنتج HIF‑2α بكميات كبيرة، وهل يمكن لفهم هذا "المفتاح التشغيل" أن يساعدنا في التنبؤ بمن سيستفيد أكثر من العلاج وكيفية تصميم علاجات جديدة؟
مستشعر الأكسجين الذي ينحرف عن مساره
تستخدم خلايا الكلية السليمة بروتين أمان يُدعى VHL للحفاظ على ضوابط محكمة لعوامل استشعار الأكسجين المعروفة باسم HIFs. عندما يتوفر الأكسجين بكثرة، يشير VHL إلى بروتينات HIF ليتم التخلص منها، مما يمنعها من تشغيل الجينات التي تعزز نمو الأوعية الدموية وانقسام الخلايا. في سرطان الكلية ذو الخلايا الصافية، غالبًا ما يفقد VHL أو يتعرض للضرر. ونتيجة لذلك، ينجو أحد أفراد عائلة HIF، وهو HIF‑2α (المشفَّر بواسطة جين EPAS1)، من التحلل ويتراكم. أظهرت أعمال سابقة أن نشاط HIF‑2α المرتفع مرتبط بنمو أسرع للأورام ونتائج أقل إيجابية، وأن حجب HIF‑2α يمكن أن يبطئ أو يوقف الأورام لدى بعض المرضى. ومع ذلك، لم تكن الخطوات الجزيئية التي تزيد من نشاط جين EPAS1 في أورام الكلية مفهومة جيدًا.
مفتاح DNA مخفي لجين سرطاني
باستخدام عينات أورام من مرضى وبيانات خلية مفردة ونماذج خلايا سرطانية، يُظهر المؤلفون أن رنا الرسول لـ HIF‑2α أعلى بشكل ملحوظ في أورام الكلية ذات الخلايا الصافية مقارنةً بنسيج الكلية الطبيعي أو أنواع أورام الكلية الأخرى. ثم يفحصون منطقة EPAS1 في الجينوم بحثًا عن علامات كيميائية وبنيوية تشير إلى وجود DNA تنظيمي نشط. يكشف هذا عن معزز قوي — نوع من مفاتيح الجينات بعيدة المدى — يقع على بعد نحو 70,000 حرف DNA أعلى من EPAS1 وينشط خصيصًا في الأورام الصافية. في خلايا الورم، يكون الكروماتين عند هذا المعزز مفتوحًا، مزينًا بعلامات التنشيط، ويتشكل حلقة تلامس محفز EPAS1، بينما يكون هذا النطاق صامتًا إلى حد كبير في خلايا الأنابيب الكلوية الطبيعية. يترابط نشاط هذا المعزز مع مستويات أعلى من EPAS1 في مجموعات بيانات سرطانية كبيرة. 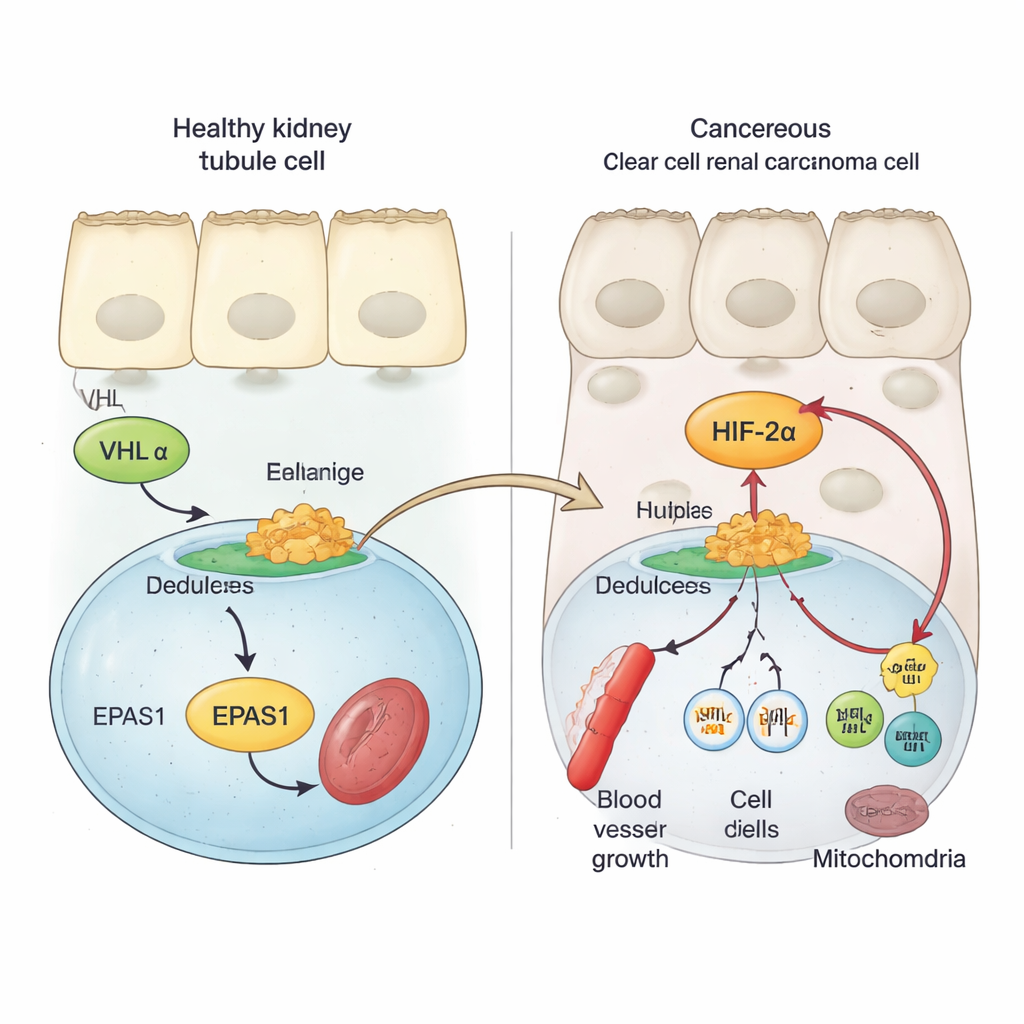
حلقة تعزيز ذاتية التعزيز يقودها عوامل هوية الكلية
تجد الدراسة أن بروتينات HIF تفعل أكثر من مجرد الاستجابة لنقص الأكسجين — فهي تساعد فعليًا في دفع إنتاجها الخاص. عندما يعيد الباحثون VHL أو يزيلون بروتين شريك رئيسي لـ HIF (HIF‑1β)، تنخفض مستويات EPAS1 ويصبح المعزز أقل وصولًا. يُظهر رسم الاتصالات المباشرة بين البروتين وDNA أن HIF يرتبط بمنطقتين معززتين أعلى EPAS1، بما في ذلك المعزز الخاص بالخلايا الصافية. في خلايا الورم الكلوية، يحتل هذا المعزز أيضًا عوامل النسخ PAX8 وHNF‑1β، وهي عوامل تساعد في تحديد هوية خلايا الكلية ومعروفة بدعمها لنمو الورم. يؤدي تعطيل PAX8 أو HNF‑1β، أو طفرة مواقع ارتباطهما داخل المعزز، إلى خفض رنا وبروتين HIF‑2α وإضعاف نشاط المعزز. توضح هذه النتائج معًا دائرة تنظيمية ذاتية: HIF‑2α، بالتعاون مع عوامل خط الكلية، يعزز نشاط معزز EPAS1، الذي بدوره يحفز إنتاج المزيد من HIF‑2α.
التقاطع بين المخاطر الوراثية وسلوك الورم على نفس الدائرة
لطالما تم الإشارة إلى منطقة EPAS1 في دراسات جينيه على مستوى الجينوم كنقطة ساخنة لمخاطر سرطان الكلية، مع ارتباط بعض المتغيرات الموروثة بمعدلات أعلى من السرطان وبطفرات VHL في الأورام. من خلال دمج البيانات الوراثية مع قياسات التعبير الجيني، يُظهر المؤلفون أن الأفراد الحاملين للنسخة عالية المخاطر من متغير رئيسي في EPAS1 يميلون إلى امتلاك مستويات أعلى من HIF‑2α في أورامهم — وحتى في خلايا الأنابيب الكلوية الطبيعية عندما يُثَبّت HIF تجريبيًا. يوحي ذلك بأن الاختلافات الوراثية الموروثة يمكن أن تضبط مدى استجابة المعزز، مما يمهد لبعض الكلى لأن ترفع HIF‑2α أكثر عندما يُفقد VHL. تُظهر تجارب في خلايا الورم الدماغي الأرومي أن نفس المعزز يمكن أن يُفعل أيضًا في بعض أورام الدماغ، مما يوحي بأن هذه الوحدة التنظيمية قد تُعاد استخدامها في سرطانات أخرى حيث يلعب HIF‑2α دورًا مهمًا. 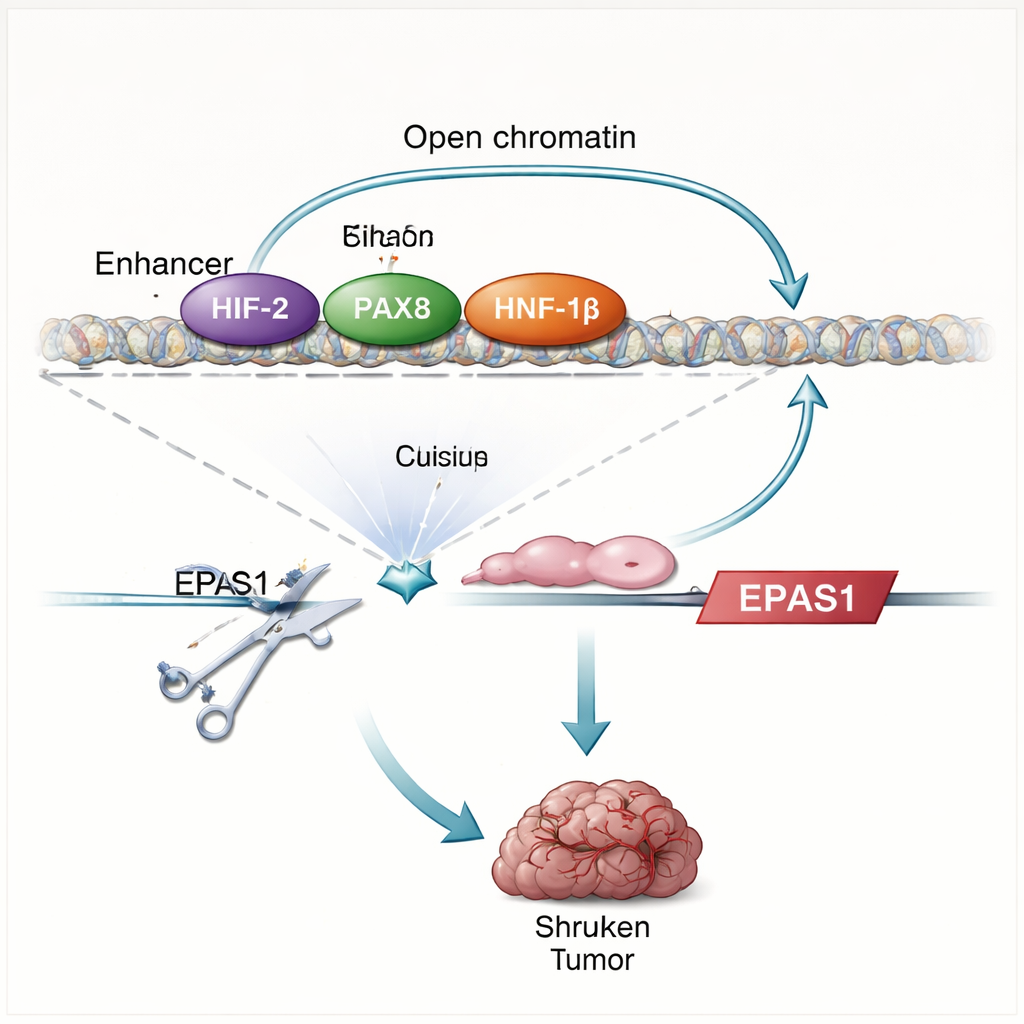
كسر الحلقة لإيقاف نمو الورم
لاختبار مدى أهمية هذا المعزز، استخدم الفريق تقنية تحرير الجينوم CRISPR لإتلاف نماذج ارتباط HIF داخل المعزز في خطوط خلايا سرطان الكلية وخلايا ورم مرضى طازجة. أدى هذا القطع إلى خفض رنا HIF‑2α بنحو الثلث إلى النصف، وخفض مستويات جينات معروفة كمستهدفة لـ HIF‑2α مثل CCND1 وVEGFA، وأضعف برنامج الجينات المرتبط بنقص الأكسجين على نطاق أوسع. عندما تُزرع الخلايا المحررة في الفئران، تفشل إلى حد كبير في تكوين أورام، على النقيض الحاد مع الخلايا الضابطة. يتطابق نمط التغيرات الجينية بعد تعطيل المعزز عن كثب مع آثار حجب HIF‑2α مباشرة بدواء سريري، مما يؤكد أن هذا العنصر الوحيد من DNA هو محرك رئيسي لمسار HIF‑2α في هذه السرطانات.
ماذا يعني هذا للمرضى والعلاجات
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن المؤلفين كشفوا عن مفتاح DNA معزز ذاتي التعزيز يبقي بروتينًا كبيرًا محفزًا للسرطان، HIF‑2α، في حالة تشغيل مستمرة في أورام الكلية ذات الخلايا الصافية. يعتمد هذا المفتاح على فقدان فرامل الأمان VHL وعلى بروتينات مساعدة خاصة بالكلية، ويتأثر بالمتغيرات الوراثية الموروثة. نظرًا لأن المعزز نشط للغاية في العديد من الأورام الصافية ومرتبط ارتباطًا وثيقًا بشدة نشاط مسار HIF‑2α، فإن قياس نشاطه — أو استهدافه مباشرة — قد يساعد في تحديد المرضى الأكثر استفادة من مثبطات HIF‑2α الحالية وقد يوفر طرقًا جديدة لإيقاف هذا الطريق عندما تصبح الأورام مقاومة للأدوية.
الاستشهاد: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
الكلمات المفتاحية: سرطان الكلية ذو الخلايا الصافية, HIF-2α, معزز EPAS1, طفرات VHL, وراثة سرطان الكلية