Clear Sky Science · ar
مؤشرات بيولوجية للاستجابة للعلاج قبل الجراحة بالپالبوسيكليب مع أناستروزول في سرطان الثدي الإيجابي لمستقبل الإستروجين/سلبي HER2 المقاوم للعلاج الهرموني: تجربة من المرحلة 2
لماذا يهم هذا البحث المرضى والعائلات
تستجيب العديد من النساء المصابات بصورة شائعة من سرطان الثدي في البداية جيدًا لأدوية حجب الهرمونات، ثم تصبح أورامهن مقاومة وتعاود النمو. تطرح هذه الدراسة سؤالًا ملحًا: هل يمكن أن يساعد إضافة دواء جديد يوقف دورة الخلية إلى العلاج الهرموني القياسي في هذه الحالات الصعبة، وهل يمكننا العثور على إشارات في الورم تتنبأ بمن سيستفيد ومن لن يستفيد؟
نظرة أقرب على سرطانات الثدي العنيدة
ركزت التجربة على سرطانات الثدي الإيجابية لمستقبل الإستروجين وسلبية HER2، وهو أكثر الأنواع شيوعًا. جميع المرضى الـ34 كانوا يتلقون مسبقًا العلاج الهرموني قبل الجراحة (مثبط الأروماتاز) لكن أظهرت أورامهم استمرار نشاط انقسام الخلايا، مما يعني أن السرطان اعتُبر «مقاومًا هرمونيًا». عالج الباحثون هؤلاء المرضى قبل الجراحة بمزيج من دواء هرموني، أناستروزول، ومثبط دورة الخلية پالبوسيكليب. قاسوا سرعة انقسام خلايا الورم باستخدام العلامة Ki67. إذا انخفضت Ki67 إلى مستويات منخفضة جدًا بعد أسبوعين، وُصِف الورم بأنه وصل إلى «توقف كامل لدورة الخلية»، مما يشير إلى أن انقسام الخلايا السرطانية توقّف بفعالية.
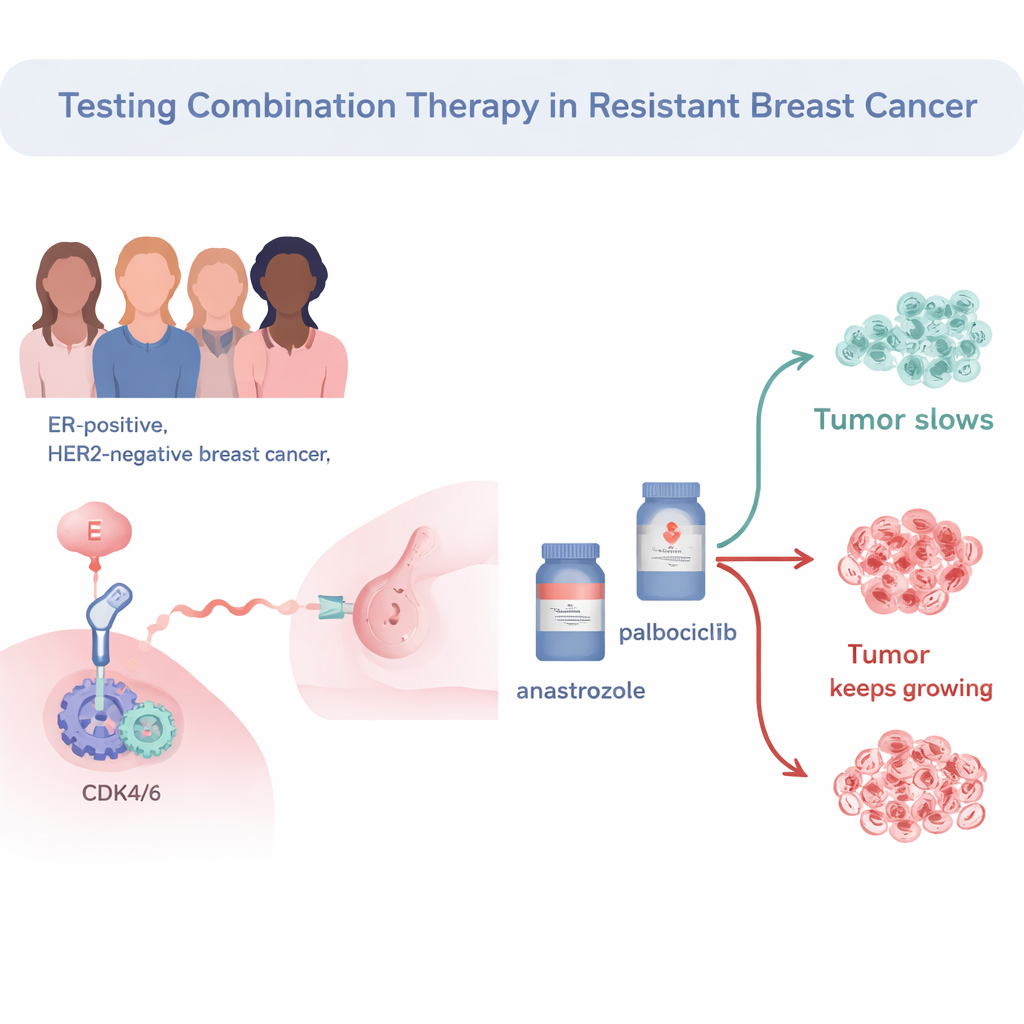
من استجاب لمزيج الأدوية؟
من بين 33 مريضة أمكن تقييم أورامهن بالكامل، وصل 57.6% إلى توقف كامل لدورة الخلية بعد أسبوعين فقط من العلاج المركب. عندما استُخدم معيار أكثر تواضعًا — بتصنيف الأورام على أنها «حساسة» إذا انخفضت Ki67 إلى أقل من 10% — اعتُبر حوالي ثلثَي الأورام مستجيبة. المرضى الذين بقيت أورامهن نشطة بدرجة عالية على مؤشر Ki67 كان شائعًا أن تكون سرطاناتهن أكثر عدائية: درجتها أعلى، حجمها أكبر، ومستويات Ki67 الابتدائية أعلى. كما كان من الأرجح أن تنتمي هذه الأورام إلى ما يُسمى الأنماط الجزيئية «غير اللمعية» والتي تميل عمومًا لأن تكون أكثر عدائية مقارنةً بأورام «لومينال A» الكلاسيكية المدفوعة بالهرمونات.
ما الذي يجعل بعض الأورام مقاومة للعلاج؟
تجاوز الفريق نسب الاستجابة البسيطة وحللوا عينات الأورام بعمق باستخدام تسلسل الحمض النووي، وتسلسل الرنا، وقياس البروتينات. لم تُحدَّد الأورام المقاومة بطفرة واحدة؛ بل أظهرت نمطًا من «التوصيل المفرط النشاط». بالمقارنة مع الأورام الحساسة، كان لدى الأورام المقاومة إشارة مستقبل إستروجين مخففة لكن نشاط أقوى في المسارات التي تدفع انقسام ونمو الخلايا، مثل جينات دورة الخلية، ومسار النمو mTOR، والعديد من الشبكات الالتهابية والمتعلقة بالإنترفيرون. كما أظهرت مستويات أعلى من «مكابح» الجهاز المناعي، المعروفة باسم نقاط التفتيش المناعية، بما في ذلك جينات مثل IDO1 وPD-L1 التي تساعد الأورام في التحايل على دفاعات الجسم.
من المسارات إلى علاجات محتملة جديدة
لاختبار ما إذا كانت هذه المسارات النشطة بدرجة مفرطة قد تُستغل ضد السرطان، أنشأ الباحثون موديلات خلوية مخبرية أصبحت مقاومة لمثبطات CDK4/6 مثل پالبوسيكليب. أظهرت هذه الخلايا المقاومة نفس بصمة تعزيز دورة الخلية وإشارات الإنترفيرون/الالتهاب التي لوحظت في أورام المرضى. عند تعريضها لأدوية تحجب إشارة JAK-STAT — وهي مسار رئيسي أسفل الإنترفيرون — كان دواء واحد، باكريتينيب، فعالًا بشكل خاص في إبطاء نمو الخلايا المقاومة وأورجانويدات مأخوذة من أورام المرضى. يشير هذا إلى أن اقتران مثبطات CDK4/6 بأدوية تستهدف JAK قد يكون استراتيجية واعدة للمرضى الذين تغلبت سرطاناتهم على التركيبات الحالية.
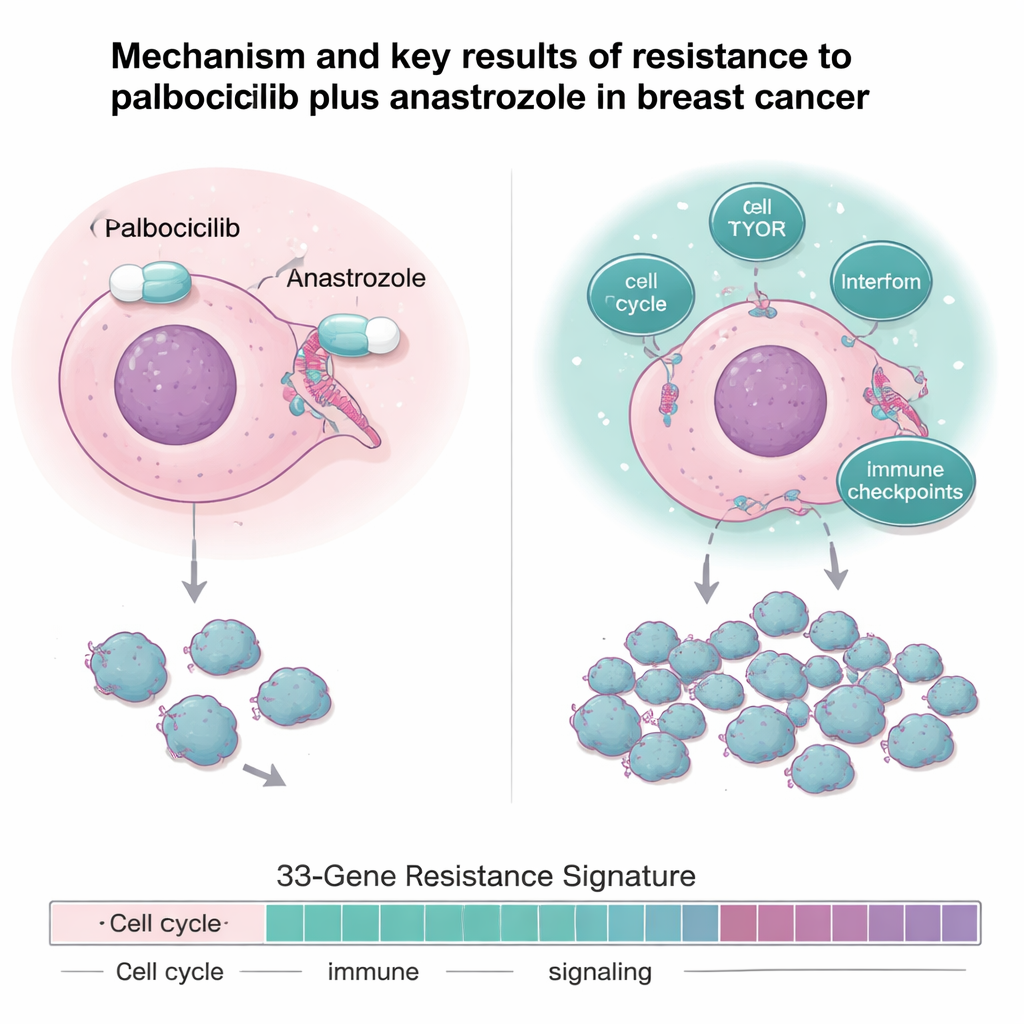
بصمة جينية تتنبأ بالمآل
بمقارنة الأورام الحساسة والمقاومة عبر تجربتين مرتبطتين، بنى الباحثون «بصمة مقاومة» مكونة من 33 جينًا تلتقط جينات تشارك في انقسام الخلية، وإصلاح الحمض النووي، وإشارات النمو، والأيض، والاستجابات المناعية/الالتهابية. كانت هذه البصمة الجينية دقيقة جدًا في التمييز بين الأورام الحساسة والمقاومة داخل التجربة. والأهم من ذلك، عندما طُبقت نفس البصمة المكونة من 33 جينًا على مجموعة مستقلة من 151 مريضًا بسرطان ثدي نقيلي عُولجوا في الممارسة الروتينية بمثبطات CDK4/6 إضافةً إلى العلاج الهرموني، كان لدى المرضى الذين سجَّلت أورامهم درجات عالية لبصمة المقاومة وقت أقصر قبل تقدم المرض وبقاء إجمالي أقصر. بعبارة أخرى، يمكن لهذه البصمة الجينية المقاسة قبل العلاج أن تشير إلى المرضى غير المرجح أن يجنوا فائدة طويلة الأمد من التركيبات القياسية القائمة على CDK4/6.
ماذا يعني هذا للرعاية المستقبلية
بالنسبة للأشخاص الذين يواجهون سرطان الثدي الإيجابي لمستقبل الإستروجين والمقاوم للهرمونات، تقدم هذه الدراسة كلًّا من الطمأنينة وخريطة طريق. تُظهر أن إضافة پالبوسيكليب إلى أناستروزول لا تزال قادرة على إيقاف نمو الورم في أكثر من نصف الحالات المقاومة. وفي الوقت ذاته تكشف أن بعض الأورام تعتمد على مسارات نمو بديلة ومتعلقة بالمناعة، مما يجعلها أصعب في السيطرة. تشير البصمة الجديدة المكونة من 33 جينًا والاكتشاف أن أدوية تستهدف JAK مثل باكريتينيب يمكن أن تكبح الخلايا المقاومة إلى طريق أكثر تخصيصًا للعلاج: بتحديد من هم غير المرجح أن يستجيبوا للتراكيب القياسية وتوجيههم مبكرًا نحو تجارب تختبر شركاء دوائيين جدد يستهدفون مباشرةً مسارات نجاة الخلايا الاحتياطية للسرطان.
الاستشهاد: Kong, T., Mabry, A., Highkin, M. et al. Biomarkers of response to neoadjuvant palbociclib plus anastrozole in endocrine-resistant estrogen receptor-positive/HER2-negative breast cancer: a phase 2 trial. Nat Commun 17, 949 (2026). https://doi.org/10.1038/s41467-026-68570-6
الكلمات المفتاحية: سرطان الثدي إيجابي مستقبل الإستروجين, مثبطات CDK4/6, مقاومة هرمونية, مؤشرات حيوية للورم, پالبوسيكليب أناستروزول