Clear Sky Science · ar
هياكل التيلوميراز البشري المرتبط بالنيوكليوتيدات في عدة مراحل من دورة إضافة تكرار الحمض النووي التيلوميري
لماذا تهم نهايات كروموسوماتنا
في كل مرة تنقسم فيها الخلية، تقصر الأغطية الواقية في نهايات كروموسوماتنا — المسماة التيلوميرات — قليلًا. إذا أصبحت قصيرة جدًا، تتوقف الخلايا عن الانقسام أو تعمل بشكل غير طبيعي، مما يساهم في الشيخوخة والمرض. آلة جزيئية تسمى التيلوميراز يمكنها إعادة بناء هذه الأغطية وتكون نشطة بشكل غير عادي في معظم السرطانات. يكشف هذا البحث، بتفصيل غير مسبوق، كيف يمسك التيلوميراز البشري بالتيلوميرات ويمددها خطوة بخطوة، مقدمًا دلائل قد تساعد مستقبلًا على ضبط هذا الإنزيم في اضطرابات مرتبطة بالعمر والسرطان.
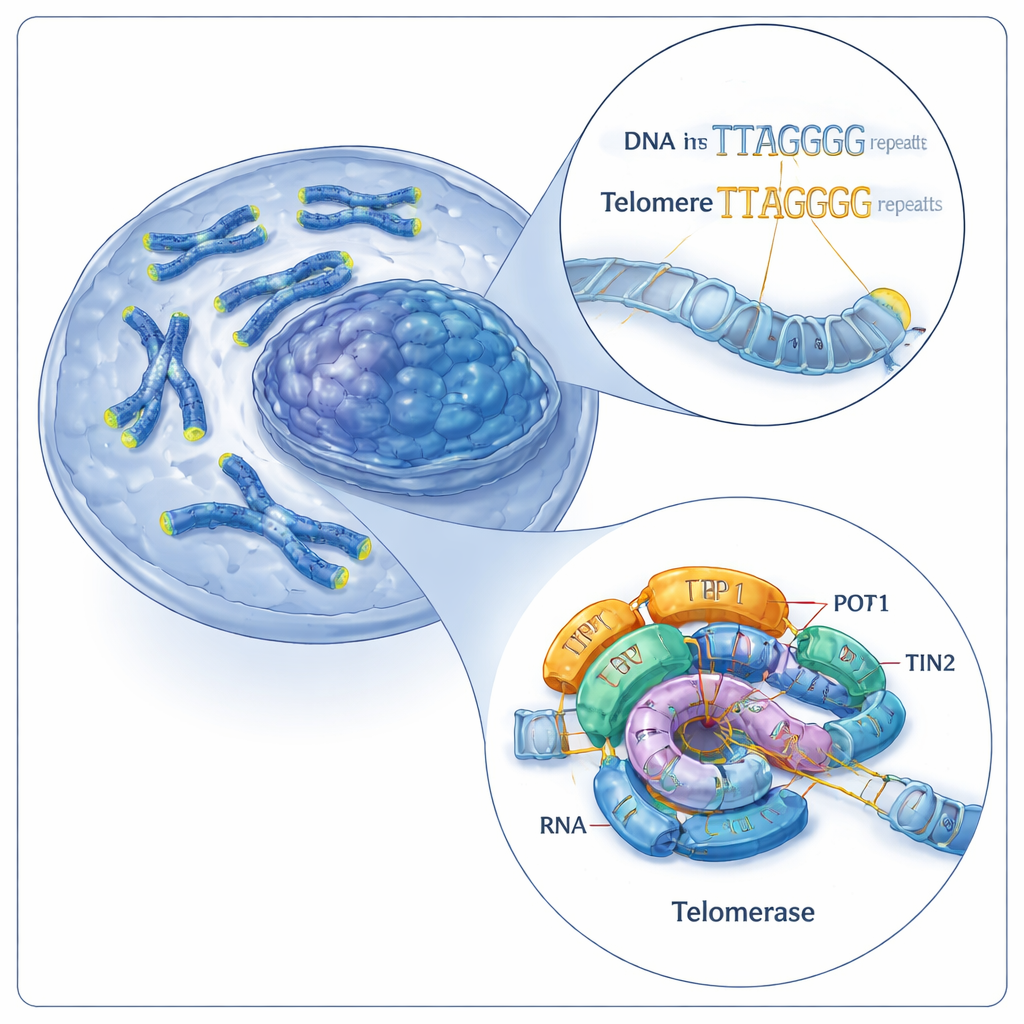
فريق إصلاح أغطية الكروموسوم في الخلية
التيلوميرات تتألف من تكرارات قصيرة من تسلسلات الحمض النووي (في البشر، نمط مكون من ستة أحرف: TTAGGG). يطيل التيلوميراز التيلوميرات بإضافة مزيد من هذه التكرارات إلى نهايات الكروموسومات. يفعل ذلك باستخدام مكوِّنين رئيسيين: بروتين يسمى تيلوميراز ريفيرس ترانسكريبتيز (TERT) وجزيء رنا مدمج (hTR) يعمل كقالب. معًا يشكلان نواة مَحفِزة، تُعينها بروتينات مساعدة تعرف بالشلترين، بما في ذلك ثلاثي TPP1–POT1–TIN2. كانت الأعمال السابقة قد صوّرت التيلوميراز البشري في حالة عمل واحدة فقط، تاركة سؤالًا رئيسيًا: كيف تضيف هذه الآلة تكرارات متتالية دون أن تنفصل عن الحمض النووي؟
تجميد التيلوميراز أثناء العمل
أعاد الباحثون بناء التيلوميراز البشري في خلايا بشرية ثم جمعوه مع قطع مصممة بعناية من الحمض النووي التيلوميري ونظائر نيوكليوتيد غير تفاعلية — جزيئات تشبه حروف الحمض النووي لكنها لا يمكن دمجها تمامًا. باستخدام مجهر إلكتروني بالتبريد عالي الدقة، التقطوا لقطات للتيلوميراز في ثلاث مراحل رئيسية من دورة إضافة التكرار: البداية (الاستهلال)، ووسط النسخ (الاستطالة)، وقبل إتمام التكرار مباشرة (ما قبل الإنهاء). أظهرت كل لقطة أن النواة المحفزة للتيلوميراز تحتضن هجينة قصيرة من الحمض النووي والرنا، مع وجود نيوكليوتيد وارد في الموقع الفعّال، جاهز للانضمام إلى السلسلة النامية من الحمض النووي.
سستة صغيرة تتحكم في عملية كبيرة
عبر المراحل الثلاث، ظهر نمط مفاجئ: الهجينة DNA–RNA داخل التيلوميراز تبقى بطول ثابت تقريبًا — أربعة أزواج قاعدية فقط، وتمتد مؤقتًا إلى خمسة عندما يدخل نيوكليوتيد جديد. حمض أميني محدد في TERT، لُقِّب بـ «رأس السستة»، يحدد باستمرار نهاية هذه الهجينة القصيرة ويمنعها من النمو أكثر. مع إضافة حروف DNA جديدة، يذوب زوج قاعدي واحد في الطرف البعيد، لذا لا تتجاوز الهجينة نافذة ضيقة من أربعة إلى خمسة أزواج. من المحتمل أن هذا التصميم المضغوط يسهل فصل السلاسل وتحريكها، ما يسمح للإنزيم بالتقدم وبدء التكرار التالي دون التخلي الكامل عن الحمض النووي. تفسر الاختلافات الطفيفة في الحروف التي يشغلها DNA وRNA داخل هذه الهجينة القصيرة سبب تماسك بعض نهايات التيلومير مع التيلوميراز أكثر من غيرها.
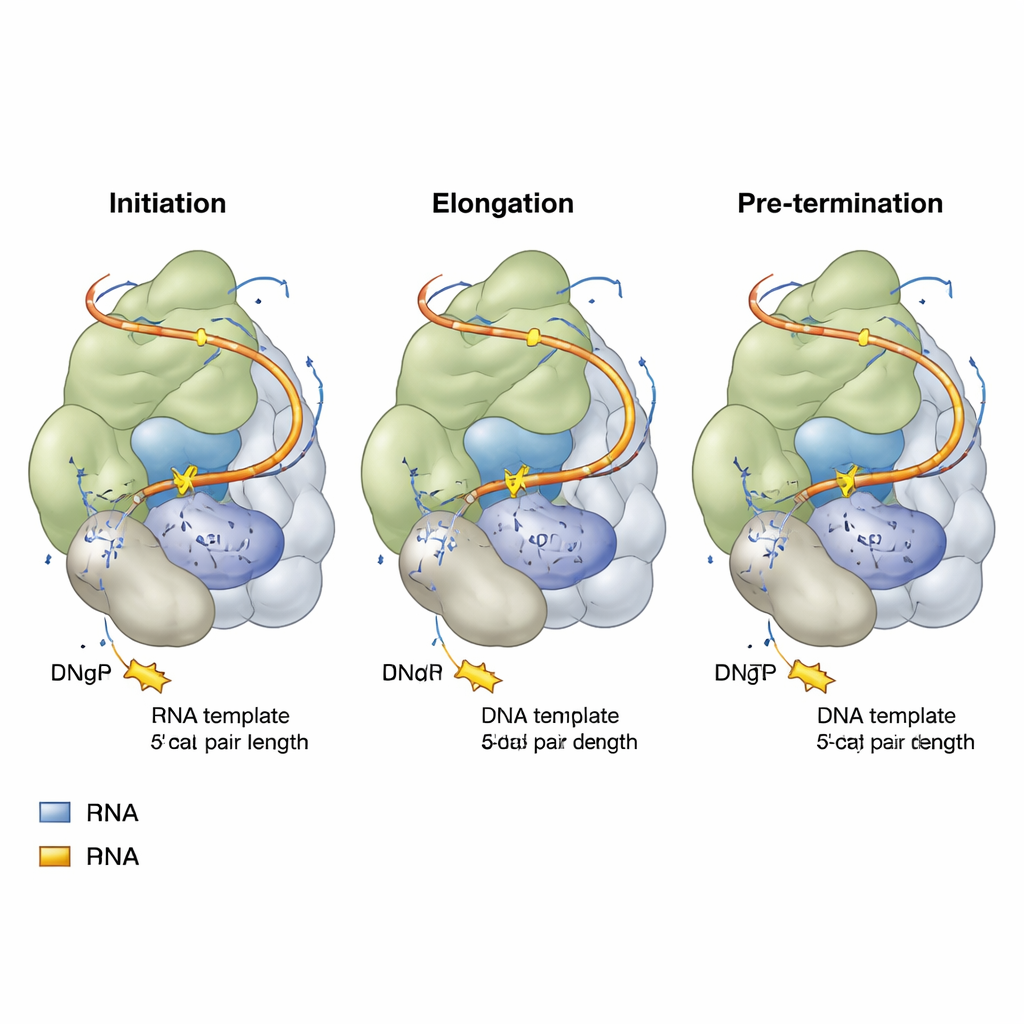
روابط رنا مرنة وأجزاء متحركة
القالب الرنوي داخل التيلوميراز لا يطفو بحرية؛ إنه مثبت بواسطة قطع مرنة على الجانبين، تُسمى روابط القالب 5′ و3′. مع تقدم التيلوميراز من الاستهلال إلى ما قبل الإنهاء، يُشَد الرابط العلوي (5′) مثل حبل مطاطي، ويصل في النهاية إلى حالة ممتدة بالكامل تساهم في إشارة نهاية التكرار. في الوقت نفسه، يُنتفخ الرابط السفلي (3′) إلى الخارج ويقترب من بنية رنا أخرى (حلقة جذع P6.1) ومناطق بروتينية قريبة. إذا أصبحت هذه الوصلات قصيرة جدًا أو طويلة جدًا، أو إذا تغيرت P6.1، تنخفض قدرة التيلوميراز على إضافة التكرارات بشدة. والأهم أن بعض مناطق البروتين — مجال TEN وإدخال خاص بالتيلوميراز يسمى إسفين TRAP — تعمل كمرشدات قابلة للتعديل، تلامس كلًا من الحمض النووي وهذه الوصلات الرناوية. الطفرات التي تقلل من حجم إسفين TRAP يمكن أن تجعل الإنزيم أكثر استمرارية في الواقع، مما يوحي بأن هذا الإسفين يعمل عادة كحاجز مضبوط يوقّت حركة القالب.
رؤى جديدة نحو هدف علاجي
من خلال الجمع بين لقطات هيكلية واختبارات وظيفية للطفرات المستهدفة، يقترح البحث نموذجًا ميكانيكيًا مفصّلًا لكيفية إطالة التيلوميراز البشري للتيلوميرات بشكل متكرر. يحتفظ الإنزيم بهجينة DNA–RNA قصيرة جدًا، ويستخدم بقاعدة تشبه السستة لفرض هذا الطول، ويعتمد على وصلات رنا مرنة وعناصر بروتينية متحركة لتقدم القالب وتثبيت الحمض النووي أثناء جولات نسخ متعددة. للغير متخصصين، الرسالة الأساسية هي أن التيلوميراز لا يعمل كآلة نسخ ثابتة بل كجهاز مضبوط بنابض، حيث تحدد هندسته وأجزاؤه المتحركة طول وكفاءة حفاظه على التيلوميرات. فهم هذا التنسيق يفتح الباب أمام أدوية قد تخفّض نشاط التيلوميراز في السرطانات أو تثبّت وظيفته في أمراض الشيخوخة المبكرة.
الاستشهاد: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
الكلمات المفتاحية: التيلوميراز, التيلوميرات, التبريد الإلكتروني بالمجهر, ثبات الجينوم, بيولوجيا السرطان