Clear Sky Science · ar
تنشيط ميكروبي لمستقبل GLP-2 يخفف الالتهاب المعوي
لماذا يهم البروتين الصديق للأمعاء
بينما يبحث العالم عن طرق مستدامة لإطعام تزايد السكان، يتجه العلماء أبعد من المزارع والحقول نحو خزانات فولاذية ضخمة تُنمى فيها الميكروبات لأغراض غذائية. تستكشف هذه الدراسة ما إذا كان أحد البروتينات المعتمدة على الميكروبات يمكنه أن يفعل أكثر من مجرد تغذيتنا. طرح الباحثون السؤال التالي: هل يمكن لبروتين مستخلص من بكتيريا غير ضارة أن يلبي الاحتياجات الغذائية وفي الوقت نفسه يحمي الأمعاء بنشاط من الالتهاب، وهي مشكلة جوهرية في حالات مثل داء الأمعاء الالتهابي والضرر المعوي الناتج عن العلاج الكيميائي؟
نوع جديد من البروتين من الميكروبات
البروتين الذي يقف في مركز هذا العمل مصدره بكتيريا تربة تُدعى Methylococcus capsulatus Bath (McB). بدلاً من تناولها ككائنات حية، تُجرى معالجة McB إلى مستحضر مخلخل ميكروبي — في الأساس مزيج مسحوق من خلايا بكتيرية مكسورة — يُنتَج تجارياً بالاسم التجاري FeedKind®. أُطعم الفئران حميات كان هذا المستحضر يوفر معظم البروتين فيها، سواء في حمية بسيطة أو في حمية «معقدة» تشبه البشر أكثر. ثم تتبعت الفريق كيف غيّرت هذه الحمية تركيبة الميكروبات المعوية، والخلايا المناعية التي تجوب الأمعاء، ومدى قدرة الأمعاء على مقاومة أنواع مختلفة من الإصابات.
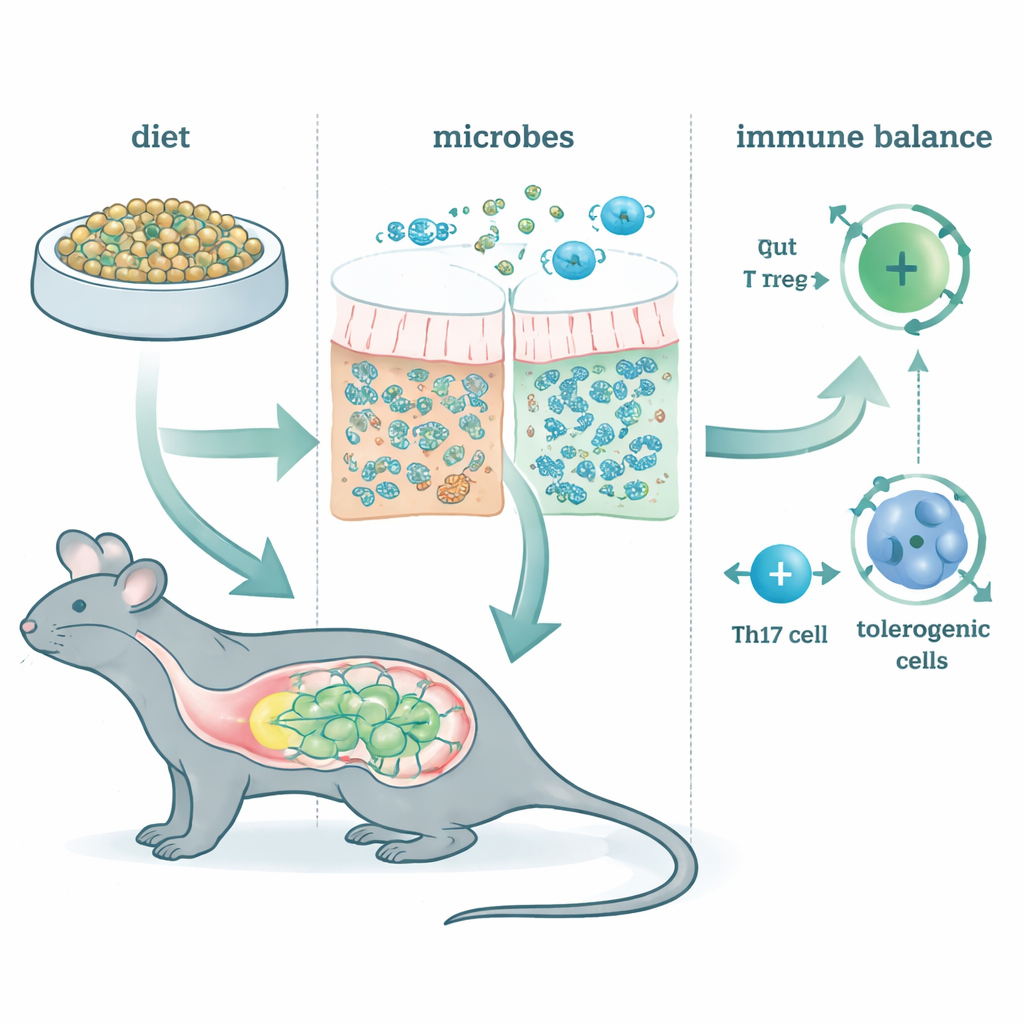
إعادة تشكيل الحي الميكروبي
أدى إطعام McB إلى تغيير سريع ومستمر في ميكروبيوتا الأمعاء، بغض النظر عن الحمية الخلفية التي تناولتها الحيوانات. ظهرت نسبة ضئيلة جداً من McB نفسها في البراز، ما يعني أن المادة استُهلكت تقريباً بالكامل في الأمعاء. بدلاً من ذلك، ازدهرت بعض أنواع البكتيريا من عائلات مثل Lachnospiraceae وBacteroidaceae. أظهرت التحليلات الجينية أن هذه المجتمعات كانت غنية بمسارات التخمر التي تنتج الأحماض الدهنية قصيرة السلسلة — جزيئات صغيرة معروفة بتغذية خلايا الأمعاء والتأثير على المناعة. بعبارة أخرى، عمل McB أقل كمسحوق بروتيني تقليدي وأكثر كوقود موجه يعيد تشكيل نشاط الميكروبات المقيمة.
تعليم الجهاز المناعي التسامح
فحص المؤلفون بعد ذلك أنواع الخلايا التائية الرئيسية التي تساعد في تقرير ما إذا كانت الأمعاء ستتجاوب بهدوء أو بعنف مع ما يمر عبرها. مجموعة واحدة، الخلايا التائية المنظمة المحفزة محيطياً (pTregs)، تساعد في منع المبالغة في الاستجابة للطعام والميكروبات الودودة. مجموعة أخرى، خلايا Th17، يمكن أن تدفع الالتهاب الضار أو تساعد في الحفاظ على حاجز صحي، اعتماداً على «مزاجها». أدى تغذية McB إلى زيادة قوية في pTregs عبر كامل الأمعاء، حتى عندما أُزيلت معظم الميكروبات المعوية بالمضادات الحيوية. بالمقابل، كانت تأثيرات McB على خلايا Th17 معتمدة على وجود ووظيفة الميكروبات المعوية الطبيعية. في الفئران ذات الميكروبيوتا السليمة، دفعت McB خلايا Th17 نحو حالة أكثر تهدئة، تُنتج IL‑10 وأقل التهابة. عندما حُجب التخمر، اختفى هذا التحول التوافقي، مما يبرز أن McB يعمل جزئياً عن طريق إعادة توجيه محادثات الميكروب–المناعة.
حماية الأمعاء أثناء الإصابة
لمعرفة ما إذا كانت هذه التغيرات تترجم إلى حماية في العالم الحقيقي، تحدى الباحثون الفئران بهجومين عنيفين على الأمعاء. الأول كان دواءً كيميائياً للعلاج الكيميائي، 5‑فلوروأوراسيل، الذي يسبب تلفًا واسعًا وتقلصًا للزُغابات الشبيهة بالأصابع التي تمتص المغذيات. الآخر كان مادة كيميائية (DSS) تحفز التهاب القولون، كنموذج لالتهاب الأمعاء الغليظة. فقدت الفئران على حمية McB وزناً أقل، حافظت على زُغابات وأطوال للقولون أطول، أبدت آفات نزفية أقل، وسجلت درجات ضرر مجهري أقل في كلا النموذجين. بقيت هذه الفوائد حتى حين أُزيلت خلايا CD4 تجريبياً، ما يوحي بأن أعمال McB الواقية للأمعاء لا تُعزى فقط إلى الخلايا المناعية التكيفية بل تشمل أيضاً تأثيرات مباشرة على بطانة الأمعاء.
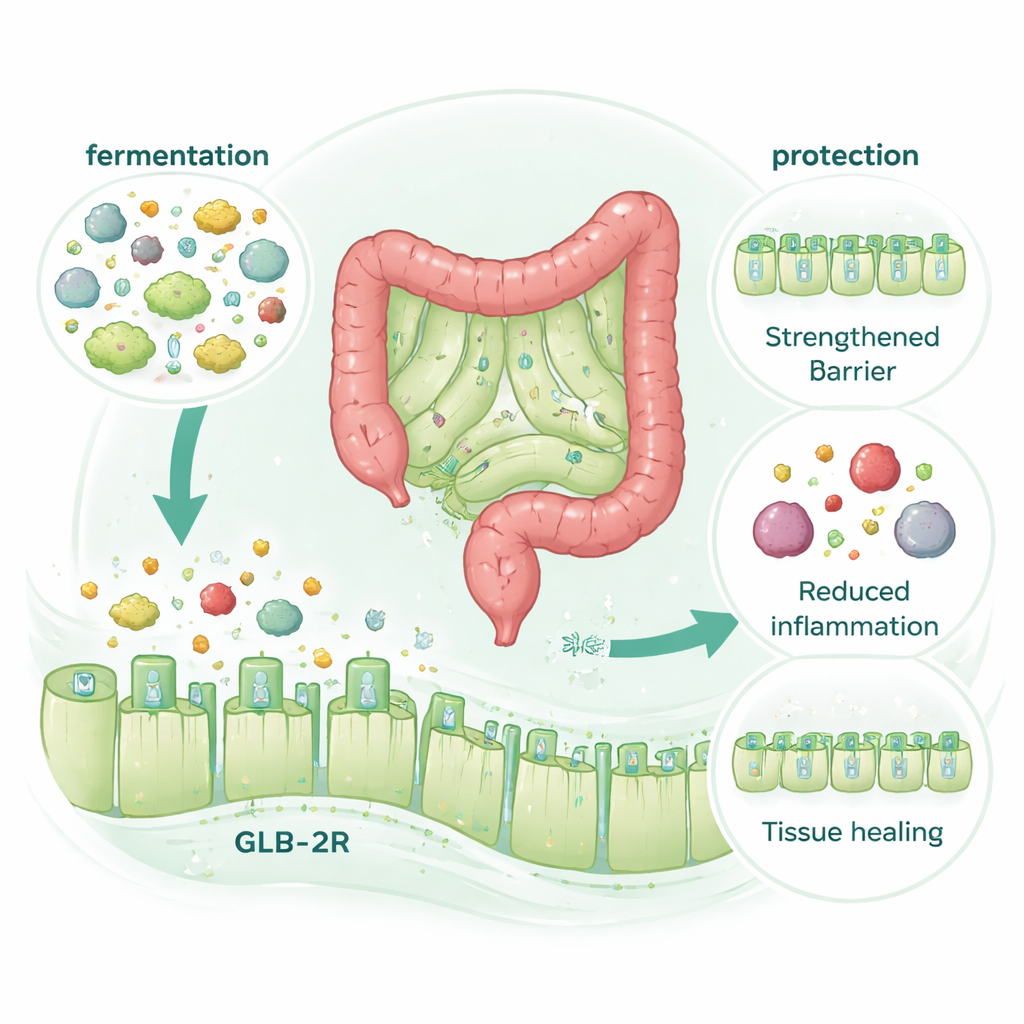
مستقبل هرموني، لكن بلا هرمون إضافي
كان من المفاجئ اكتشاف أن أثر McB الوقائي كان يتطلب قطعاً مستقبل GLP‑2 في الأمعاء — وهو مستقبل لهرمون يعزز الإصلاح — لكن ليس مستقبل GLP‑1 المرتبط به. عندما افتقرت الفئران إلى مستقبل GLP‑2، لم يعد McB يحميها من أضرار العلاج الكيميائي أو التهاب القولون. ومع ذلك لم يرفع McB نفسه مستويات GLP‑2 في الدم، حتى عندما أُحكمت السيطرة على الهضم وتحلل الهرمونات. بدلاً من ذلك، اختفت الفوائد عندما حُجب التخمر الميكروبي في القولون كيميائياً، رغم أن تركيبة الميكروبيوتا العامة تغيرت قليلاً جداً. يشير هذا إلى آلية تولدها تحلل McB الميكروبي لإنتاج مركبات صغيرة تتصرف كمحاكيات لـ GLP‑2، فتُفعّل مستقبله لتقوية الحاجز وتعزيز الإصلاح دون إفراز هرمون إضافي.
ماذا قد يعني هذا للأغذية المستقبلية
للقارئ العادي، الخلاصة هي أن بعض مصادر البروتين المستقبلية قد تُصمم ليس فقط لتكون صديقة للمناخ، بل أيضاً لدعم صحة الأمعاء بنشاط. في الفئران، أعاد مستحضر McB القابل للتصنيع تجارياً توجيه المناعة نحو التسامح وساعد الأمعاء على تحمل إصابات شديدة عبر مسارين مستقلين جزئياً: تعزيز مباشر للخلايا التائية المنظمة وتنشيط مستقبلات GLP‑2 عبر التخمر الذي يدعم إصلاح الأنسجة. بينما لا تزال هناك حاجة لدراسات بشرية، تشير النتائج إلى أن البروتينات المشتقة من الميكروبات قد تشكل فئة جديدة من الأغذية «الذكية» — القادرة على تغذيتنا، والتعاون مع ميكروباتنا، وتعزيز دفاعات الأمعاء الطبيعية ضد الالتهاب بهدوء.
الاستشهاد: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
الكلمات المفتاحية: التهاب الأمعاء, بروتين ميكروبي, الميكروبيوم, مستقبل GLP-2, الخلايا التائية المنظمة