Clear Sky Science · ar
بروتين FUNDC1 البطاني ينظّم إعادة برمجة الأيض والانتقال من السمنة إلى داء السكري عبر محور SIRT3/GATA2/إندوتيلين-1
لماذا تهم خلايا الأوعية الدموية في السمنة والسكري
عادةً ما تُحمّل السمنة وداء السكري من النوع الثاني اللوم للنسيج الدهني أو الكبد أو البنكرياس. لكن هذه الدراسة تكشف عن متهم مفاجئ: الطبقة الرقيقة من الخلايا التي تبطن أوعيتنا الدموية، المسماة الخلايا البطانية. يبيّن الباحثون أن بروتينًا صغيرًا في الميتوكوندريا داخل هذه الخلايا يدعى FUNDC1 يمكن أن يدفع الجسم من زيادة وزن بسيطة إلى سكري كامل عبر تغيير كيفية تواصل الأوعية مع الأعضاء الأيضية.
ضغط على «جلد» الجسم الداخلي
تشكل الخلايا البطانية شبكة واسعة ورقيقة تتحكم بتدفق الدم وتزويد المغذيات وإرسال إشارات إلى الأنسجة المجاورة. في الظروف الصحية، توازن بين عوامل الاسترخاء مثل أكسيد النيتريك وعوامل الانقباض مثل الإندوتيلين-1 (ET-1). في السمنة والسكري المبكر، ينحرف هذا التوازن لصالح ET-1، الذي لا يضيّق الأوعية فقط بل يخلّ أيضًا بطريقة تعامل الخلايا الدهنية والعضلية والكبدية مع السكر والدهون. بدأ المؤلفون بعرض نتائج في الفئران تشير إلى أن خللاً بوظيفية الأوعية يظهر بعد شهرين فقط من حمية عالية الدهون، قبل تطور مقاومة الأنسولين الواضحة، مما يوحي بأن إصابة البطانة قد تساهم في إطلاق المرض الأيضي بدلاً من أن تكون مجرد استجابة له.
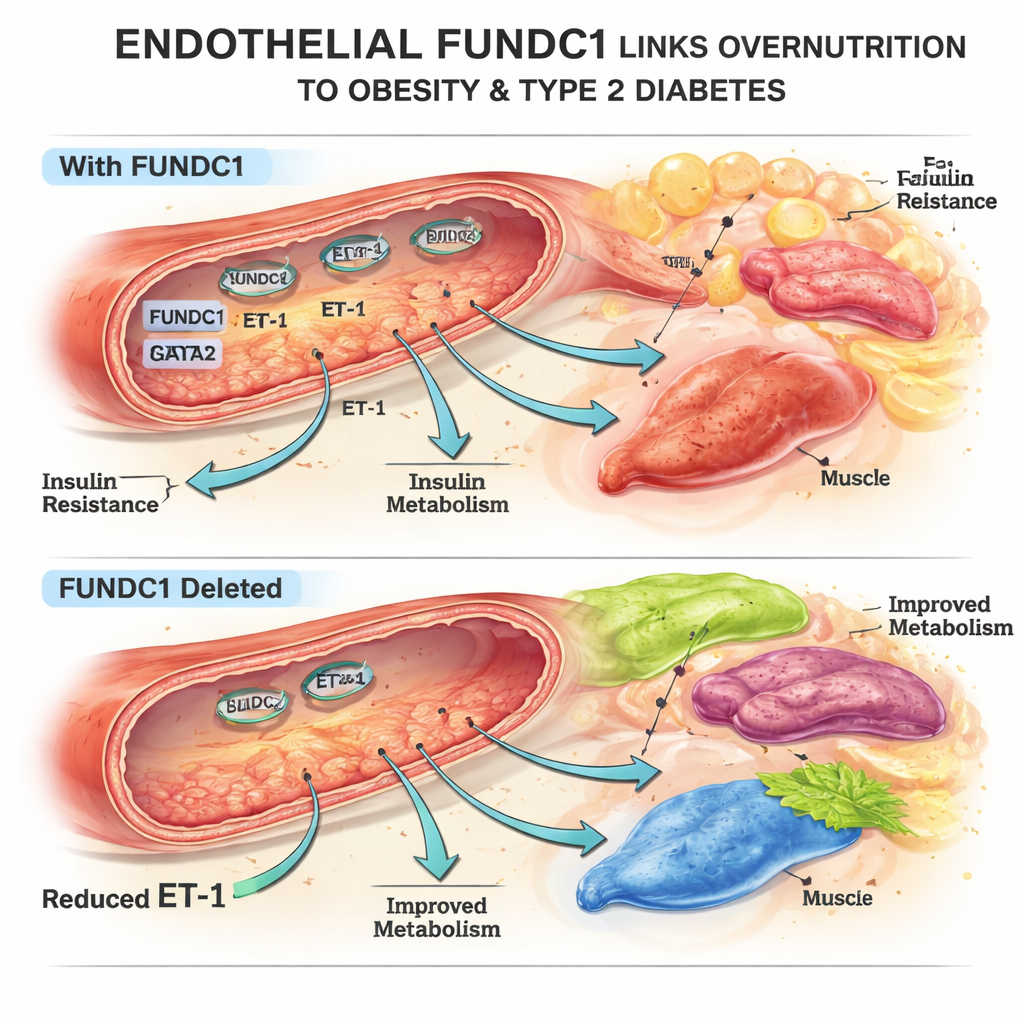
مفتاح ميتوكوندري يشكل دهن الجسم
ركز الفريق على FUNDC1، بروتين على سطح الميتوكوندريا، مصانع طاقة الخلية. في خلايا بطانية من الفئران والبشر المعرضة لفرط الدهون، تغيّرت مستويات FUNDC1 مع الزمن: انخفضت في البداية ثم ارتفعت بشدة مع التغذية المفرطة الطويلة الأمد. باستخدام فئران مهندسة وراثيًا تفتقد FUNDC1 فقط في الخلايا البطانية، اكتشف الباحثون أن هذه الحيوانات كانت محمية جزئيًا من زيادة الوزن الناجمة عن حمية عالية الدهون، وامتلكت دهونًا جسمية أقل وخلايا دهنية أصغر وتحكمًا أفضل بسكر الدم. استجابات أنسجة الدهن والكبد والأنسجة الدهنية البنية للإنسولين كانت أقوى، رغم أن مستويات الإنسولين نفسها لم تكن أعلى. ولا يمكن تفسير هذه التغيرات بالاختلافات في المدخول الغذائي أو النشاط، ما يشير بدلًا من ذلك إلى تأثير الأوعية على الأيض.
رسل كيميائي يدفع مقاومة الإنسولين
لاكتشاف كيفية تأثير FUNDC1 البطاني على الأعضاء البعيدة، فحص المؤلفون عدة مواد يفرزها الخلايا البطانية. برزت واحدة: ET-1. عند حذف FUNDC1 في الخلايا البطانية، انخفض إنتاج ET-1 في الأوعية ومقداره في مجرى الدم بشكل ملحوظ، سواء في ظروف عادية أو على حمية عالية الدهون. أظهرت تجارب في خلايا دهنية مزروعة وخلايا كبدية وعضلية أن ET-1 يعزز نمو ما قبل الخلايا الدهنية، ويغيّر تخزين وتحلل الدهون، ويزيد تراكم الدهون في الكبد والعضلات المعرضة للدهون — نمط معروف بتعزيز مقاومة الإنسولين. في الفئران الحية، محاليل ET-1 عند بدء الحمية العالية الدهن ألغت الفوائد الوقائية لحذف FUNDC1 البطاني: تدهور وزن الجسم وكتلة الدهون وضبط سكر الدم ووظيفة الأوعية، مما يؤكد دور ET-1 كحلقة وصل رئيسية بين البطانة والمرض الأيضي.
محور إشاري داخلي: FUNDC1 وSIRT3 وGATA2
بعد ذلك ترسم الدراسة سلسلة جزيئية مفصلة داخل الخلايا البطانية. تحت ضغط الدهون العالية، ينتقل شكل طويل من إنزيم SIRT3 (SIRT3-L)، القادر على التواجد في النواة والميتوكوندريا، من النواة إلى الميتوكوندريا بمساعدة FUNDC1 وبروتين مرافق يسمى HSC70. وبمجرد احتجازه في الميتوكوندريا، يصبح SIRT3-L أقل توفرًا في النواة لإزالة مجموعات الأسيتيل من GATA2، عامل نسخة يحفز نشاط جين ET-1. تكون GATA2 الأسيتيلية أكثر استقرارًا وتدفع إنتاجًا أكبر من ET-1. عند غياب FUNDC1، يبقى SIRT3-L في النواة حيث ينزع مجموعات الأسيتيل من GATA2، مما يؤدي إلى تدهور GATA2 وانخفاض إنتاج ET-1. ومن المثير للاهتمام أن SIRT3 يعزز بدوره تحلل FUNDC1، مكوّنًا حلقة تغذية راجعة تحد عادة هذا المسار لكنها تتعطل أثناء التغذية المفرطة المزمنة.
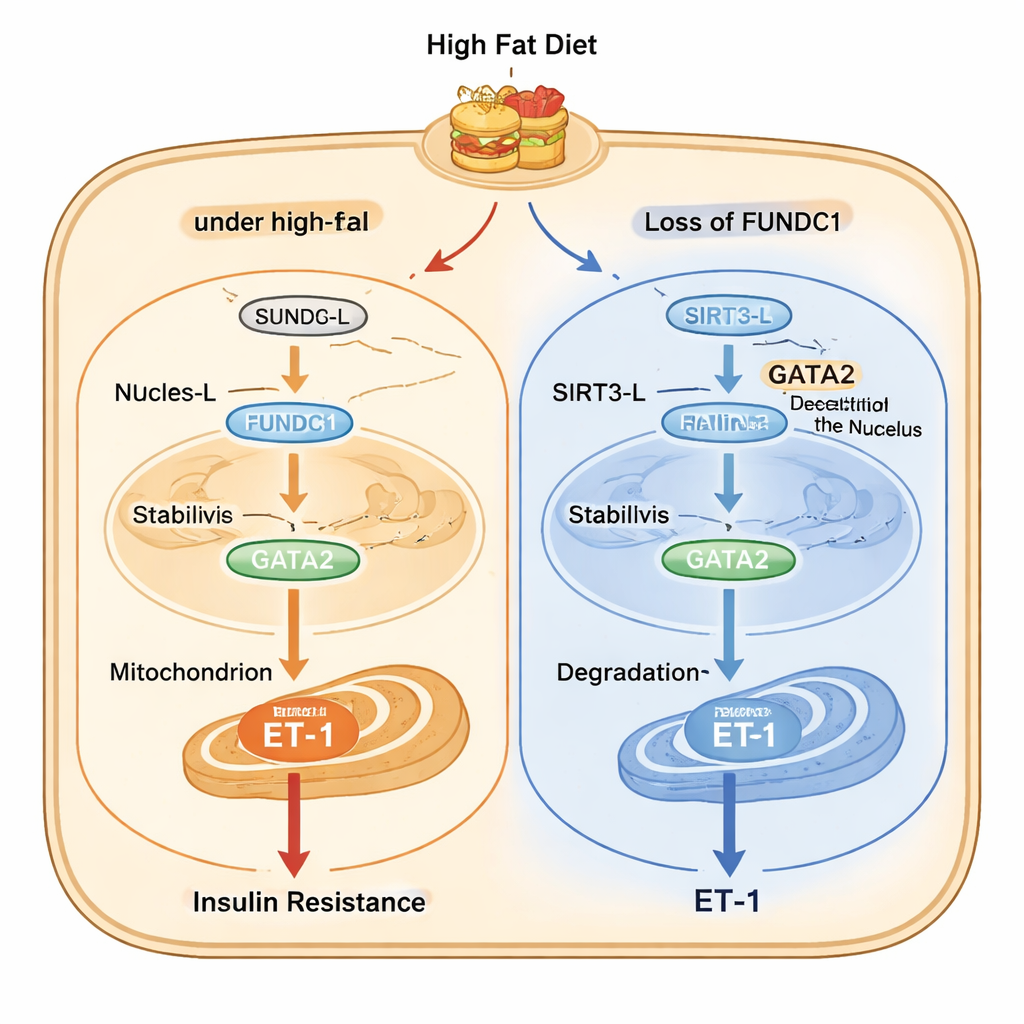
من نماذج الفأر إلى مرض الإنسان
لاختبار ما إذا كان هذا الآلية ذات صلة لدى البشر، فحص الباحثون الدم والشرايين الصغيرة من أشخاص مصابين بالسمنة وداء السكري من النوع الثاني ومن متطوعين أصحاء. كان لدى المرضى المصابين بالحالتين مستويات دم أعلى من ET-1 وتعابير أعلى لـ FUNDC1 وGATA2 وجين ET-1 في بطانة أوعيتهم. تتبع مقدار ET-1 في الدم ارتباطًا وثيقًا بمؤشر كتلة الجسم وبقياس سكر الدم على المدى الطويل (HbA1c)، وارتبطت مستويات جين ET-1 الوعائي بقوة مع FUNDC1 وGATA2. هذه الأنماط تعكس نتائج الفئران وتدعم فكرة أن محور FUNDC1–SIRT3–GATA2–ET-1 المفرط النشاط يعمل في النسيج الوعائي البشري تحت الضغط الأيضي.
هدف جديد في مكافحة السكري
لغير المتخصصين، الرسالة الأساسية هي أن الضرر الناتج عن الإفراط في الأكل قد يظهر أولًا في الخلايا التي تبطن أوعيتنا الدموية. هناك، يساعد بروتين ميتوكوندري، FUNDC1، على توجيه إنزيم تنظيمي، SIRT3، بعيدًا عن النواة، مما يسمح لعامل آخر، GATA2، بزيادة إنتاج ET-1، إشارة قوية تشبه الهرمون تروّج كلًّا لتصلب الأوعية ومقاومة الإنسولين. قد يساعد تعطيل هذا المسار — عن طريق تقليل نشاط FUNDC1 البطاني أو خفض ET-1 — في منع الانتقال من السمنة إلى السكري وحماية الأوعية الدموية في الوقت نفسه.
الاستشهاد: Li, J., Li, D., Zhao, F. et al. Endothelial FUNDC1 regulates metabolic reprogramming and the obesity-diabetes transition through the SIRT3/GATA2/endothelin-1 axis. Nat Commun 17, 1836 (2026). https://doi.org/10.1038/s41467-026-68548-4
الكلمات المفتاحية: خلايا بطانية, الميتوكوندريا, إندوتيلين-1, السمنة, داء السكري من النوع الثاني