Clear Sky Science · ar
الليبيدات الإيثرية تؤثر في مصير خلايا السرطان بتعديل مدخلات الحديد
كيف يمكن لدهون قليلة الشهرة أن تكشف نقطة ضعف السرطان
يوصف السرطان غالبًا بأنه «مرض الجينات»، لكن هذه الدراسة تُظهر أن الدهون المكونة للغشاء الخارجي للخلية قد تكون مهمة بنفس القدر. يكشف الباحثون كيف أن فئة خاصة من الدهون، تُدعى الليبيدات الإيثرية، تساعد الخلايا السرطانية الخطرة على سحب الحديد من محيطها—مما يغذي قدرتها على الانتشار ويزيد في الوقت نفسه قابليتها لنوع جديد من موت الخلايا. فهم هذا الارتباط الخفي بين أغشية الخلايا والحديد وسلوك الأورام قد يفتح أبوابًا لعلاجات تمحو على نحو انتقائي أكثر الخلايا السرطانية عدوانية.
طريقة مختلفة للتفكير بشأن الخلايا السرطانية
تركز معظم أبحاث السرطان على الطفرات في الحمض النووي والبروتينات التي تُشفّرها. تحوّل هذه الورقة الانتباه إلى غشاء الخلية—القشرة الدهنية الرقيقة التي تحيط بكل خلية. يعيش داخل تلك القشرة العديد من أنواع الليبيدات (الدهون)، لكل منها أشكال وخصائص فيزيائية مميزة. يركز المؤلفون على الليبيدات الإيثرية، التي تشكل حوالي خُمس الفسفوليبيدات في كثير من الخلايا الثديية ولكنها كانت أقل دراسة. يكتشفون أن الخلايا السرطانية عالية القدرة على الانتشار والمشابهة للخلايا الجذعية تملأ أغشيتها بالليبيدات الإيثرية، ما يمنح تلك الأغشية توترًا منخفضًا وسوائلية عالية. هذه الخصائص الفيزيائية، بدورها، تغير كيفية امتصاص الخلايا للحديد، ذلك المعدن الذي يمكن أن يدفع كلًا من نمو الورم وعملية مدمرة تُسمى الفروربتوزيس، شكل من أشكال موت الخلايا المعتمد على الحديد.
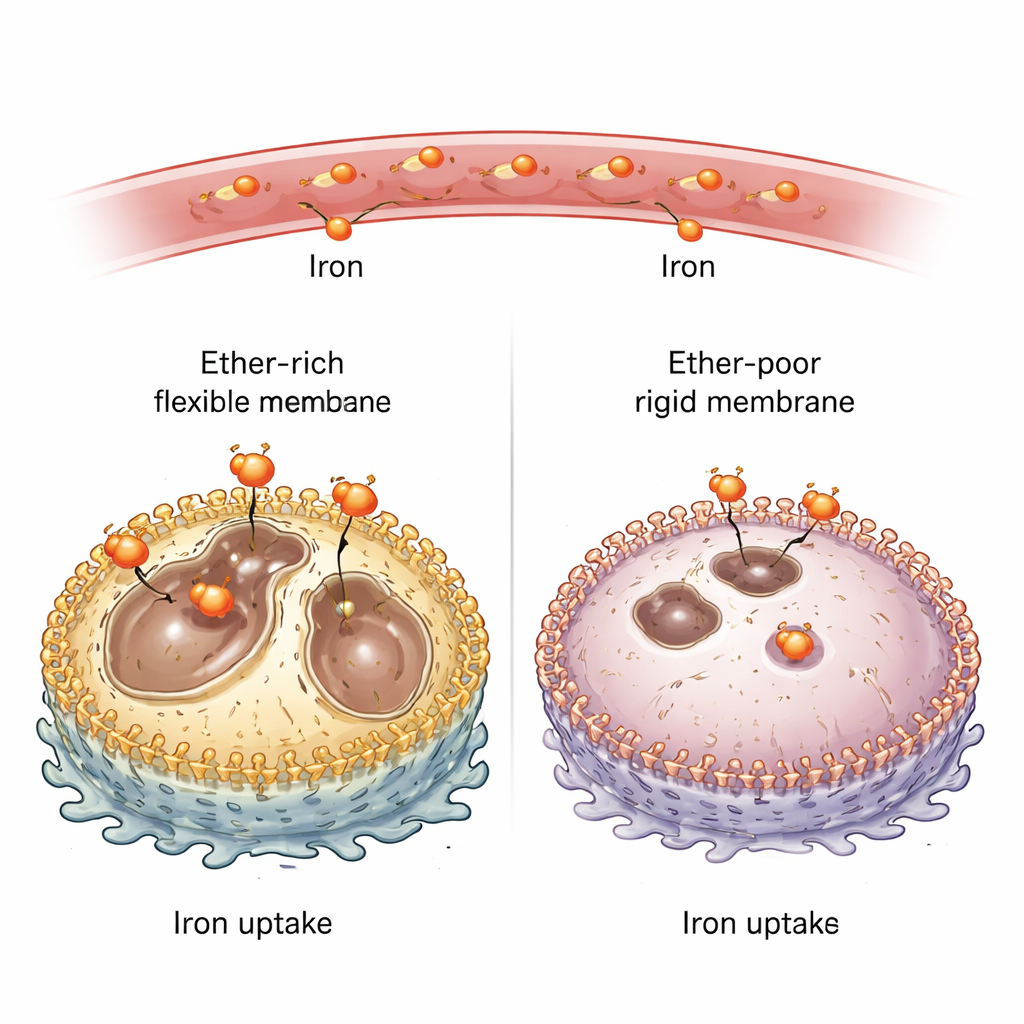
ربط دهون الغشاء بمدخلات الحديد
لاستكشاف الليبيدات الإيثرية، حذف الفريق إنزيمات رئيسية مطلوبة لصنعها في عدة خطوط خلايا سرطانية من الفئران والبشر. من دون هذه الإنزيمات، انهارت نسبة الليبيدات الإيثرية في غشاء البلازما من نحو ربع كل الدهون إلى بضعة بالمئات فقط. والمفاجئ أن هذه الخلايا الفقيرة بالإيثر حملت قدرًا أقل بكثير من «الحديد النشط أكسدة»—الشكل الكيميائي التفاعلي الذي يشارك في تفاعلات الأكسدة—سواء في المزرعة أو في الأورام المزروعة في الفئران. عندما زوّد العلماء الخلايا بحديد إضافي من الخارج، عادت مستويات الحديد في الخلايا وارتفعت حساسيتها لأدوية استحثاث الفروربتوزيس. أظهر ذلك أن الليبيدات الإيثرية تفعل أكثر من كونها مجرد وقود قابل للاحتراق في الأكسدة؛ فهي تتحكم بنشاط في كمية الحديد التي تدخل الخلية.
بوابة حديد متخصصة: مسار CD44
سأل الباحثون بعد ذلك كيف يغير تركيب الغشاء من عملية امتصاص الحديد. عادة ما تستورد الخلايا الحديد عبر بروتين معروف باسم مستقبل الترانسفيرين، لكن الخلايا السرطانية العدوانية الشبيهة بالجذعية تعتمد أيضًا على مسار آخر: بروتين سطحي مُسمى CD44 يسحب الحديد المرتبط بجزيء سكر يُسمى حمض الهيالورونيك. من خلال تتبع مجسات فلورية، أظهر الفريق أن حذف الليبيدات الإيثرية أثر بالكاد على امتصاص مستقبل الترانسفيرين لكنه أبطأ بشدة الابتلاع الخلوي الوسيط بواسطة CD44—وهو مسار بديل غير معتمد على الكلاترين لجلب المواد إلى داخل الخلية. إعادة الليبيدات الإيثرية، أو إضافتها مرة أخرى على شكل حويصلات دهنية، أعاد هذا المسار المعتمد على CD44. كما أدى تعطيل CD44 نفسه أو هضم حمض الهيالورونيك إلى خفض الحديد الخلوي، مما يؤكد أن هذا المسار المعتمد على الإيثر هو بوابة رئيسية للحديد في هذه الخلايا السرطانية.
كيف تغيّر الأغشية الأطرى سلوك الخلية
لماذا تهم الليبيدات الإيثرية كثيرًا بالنسبة إلى CD44 لكن ليس للمستقبل الكلاسيكي؟ يكمن الجواب في الفيزياء. باستخدام أدوات دقيقة تسحب خيوطًا صغيرة من سطح الخلية، أظهر المؤلفون أن الأغشية الغنية بالإيثر لها توتر أقل وأسهل في التشوّه. عندما أُزيلت الليبيدات الإيثرية، ازداد توتر الغشاء وضاق ترتيب الليبيدات، مما جعل الغشاء أكثر صلابة. هذه التغيرات أعاقت بشدة أشكالًا من الابتلاع الخلوي التي تعتمد على بقع غشائية مرنة تشبه الطوافات—وهو بالضبط النوع الذي يستخدمه CD44—بينما تركت الامتصاص المعتمد على الكلاترين سليمًا إلى حد كبير. كما ساعدت الليبيدات الإيثرية في تثبيت «طوافات ليبيدية»، جزر مرتبة صغيرة في الغشاء تتجمع فيها CD44 قبل أن تُسحب إلى الداخل. باختصار، تضبط الليبيدات الإيثرية المشهد الفيزيائي للغشاء لتفضيل امتصاص الحديد بقيادة CD44.
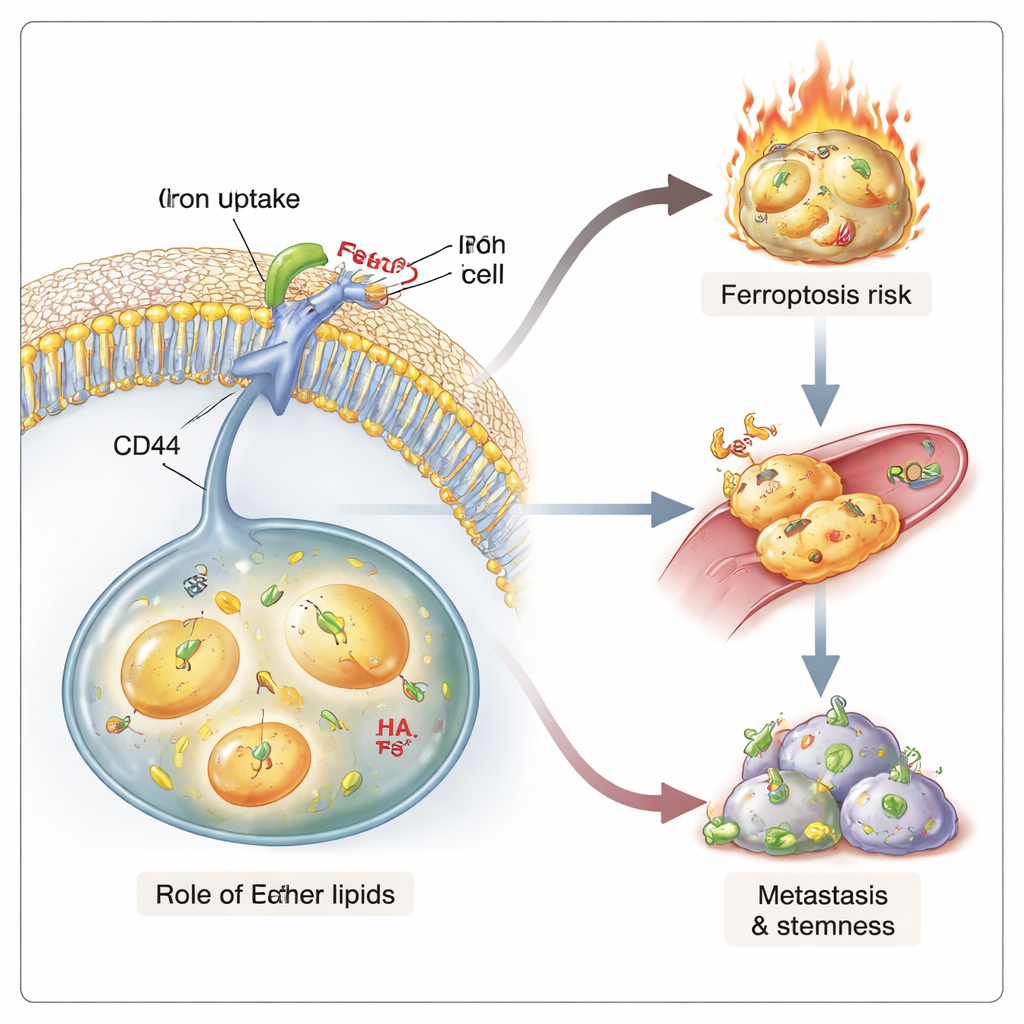
تغذية كل من الانتشار والتدمير الذاتي
ترتبط المستويات العالية من الحديد والتوتر المنخفض للغشاء بصفات تجعل السرطانات قاتلة: القدرة على غرس أورام جديدة والبقاء على قيد الحياة أمام العلاجات. في نماذج أوعية دقيقة ثلاثية الأبعاد، كانت الخلايا السرطانية الغنية بالإيثر أكثر ميلاً للخروج من هياكل تشبه الأوعية الدموية—وهي خطوة مبكرة في الانبثاث. في الفئران، شكّلت الخلايا السرطانية الناقصة بالإيثر نقائل أقل، رغم أن أورامها الأولية نمت بمعدلات مماثلة. كما أظهرت هذه الخلايا انخفاضًا في «الخصائص الجذعية»، قِيّمت بقدرتها المتناقص على تشكيل كُريات ثدي في المزرعة وعلى بدء أورام عند الزرع بجرعات محدودة. في الوقت نفسه، كانت الخلايا الغنية بالإيثر، بتحميلها الأعلى من الحديد والليبيدات الأكثر قابلية للأكسدة، أكثر عرضة للفروربتوزيس عند التحدي بأدوية محددة أو إشارات مناعية. هكذا تخلق الليبيدات الإيثرية حالة ذا حدين: فهي تدعم السلوك العدواني الشبيه بالجذعي في حين تجعل تلك الخلايا نفسها قابلة للقتل بوساطة تلف الدهون المعتمد على الحديد.
لماذا يهم هذا لعلاجات السرطان المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن ليس كل الخلايا السرطانية متشابهة في الخطر، وأن أغشيتها الخارجية تساعد في تحديد مدى تهديدها ودرجة قابليتها للاستهداف. تعيد الليبيدات الإيثرية تشكيل سطح الخلية بحيث يتدفق الحديد عبر باب متخصص، مما يمنح الخلايا الشبيهة بالجذعية قدرة أكبر على الانتشار ولكنه أيضًا يملأها بمكونات تهيئها لتدميرها الذاتي. قد تستهدف العلاجات التي تغيّر إنتاج الليبيدات الإيثرية، أو تعطل امتصاص الحديد المعتمد على CD44، أو تثير الفروربتوزيس بعناية هذه المجموعات الخلوية السرطانية الصعبة العلاج مع الحفاظ على الأنسجة الطبيعية. من خلال كشف كيف تربط فئة قليلة الشهرة من الدهون فيزياء الغشاء واستقلاب المعادن ومصير الخلية، تفتح هذه الدراسة مسارًا جديدًا نحو تدخلات سرطانية أكثر ذكاءً ودقة.
الاستشهاد: Mansell, R.P., Müller, S., Yang, JS. et al. Ether lipids influence cancer cell fate by modulating iron uptake. Nat Commun 17, 1835 (2026). https://doi.org/10.1038/s41467-026-68547-5
الكلمات المفتاحية: الليبيدات الإيثرية, خلايا جذعية سرطانية, امتصاص الحديد, الفروربتوزيس, الانبثاث