Clear Sky Science · ar
تحويل البلاعم في سمك الزرد للإشارات الفيزيائية الناتجة عن الجروح إلى نفاذية وعائية سريعة
كيف يعلّمنا سمك صغير عن تورّم الجروح
عندما تخدش ركبتك، يتحول المكان سريعًا إلى أحمر ومنتفخ ويتسرب منه سائل. هذا التغير السريع في الأوعية الدموية المجاورة ضروري لمحاربة العدوى وبدء عملية الإصلاح، لكن من الصعب رؤية كيف يشعر الجسم بالضرر ويتفاعل خلال ثوانٍ في الزمن الحقيقي. باستخدام يرقات سمك الزرد الشفافة وتصوير حي متقدم، تكشف هذه الدراسة كيف تقوم خلايا مناعية متخصصة ملفوفة حول الأوعية الدموية بتحويل الصدمة الفيزيائية للجُرح إلى تسرب وعائي شبه فوري، ما يقدّم فهماً جديداً للالتهاب والشفاء وحتى إصابات الرئة لدى البشر.
مراقبة انتشار الإصابة عبر الجسم
عمل الباحثون مع أسماك زرد صغيرة الجسم، إذ تتيح أجسامها الشفافة للعلماء مشاهدة الخلايا والأوعية الدموية قيد العمل تحت المجهر. قطعوا طرف زيل الزعنفة وملأوا الدورة الدموية بصبغة متألقة تبقى داخل الأوعية السليمة. عند إعادة الأسماك المصابة إلى ماء عذب عادي، أحدث التدفق المفاجئ للماء إلى الأنسجة «صدمة أسموزية» حول الجرح. خلال دقائق، اتسعت الأوعية القريبة وبدأت تتسرب الصبغة المضيئة إلى النسيج المحيط، محاكة التورّم والنزف اللزج الذي يحدث حول الجروح البشرية. عبر تبديل الأسماك بين محاليل ملحية وسكرية متوازنة خصيصًا ومحاليل عادية، بيّن الفريق أن هذه النفاذية الوعائية السريعة تعتمد بقوة على التغيرات الأسموزية أكثر من الاعتماد على تمزق الأنسجة وحده.
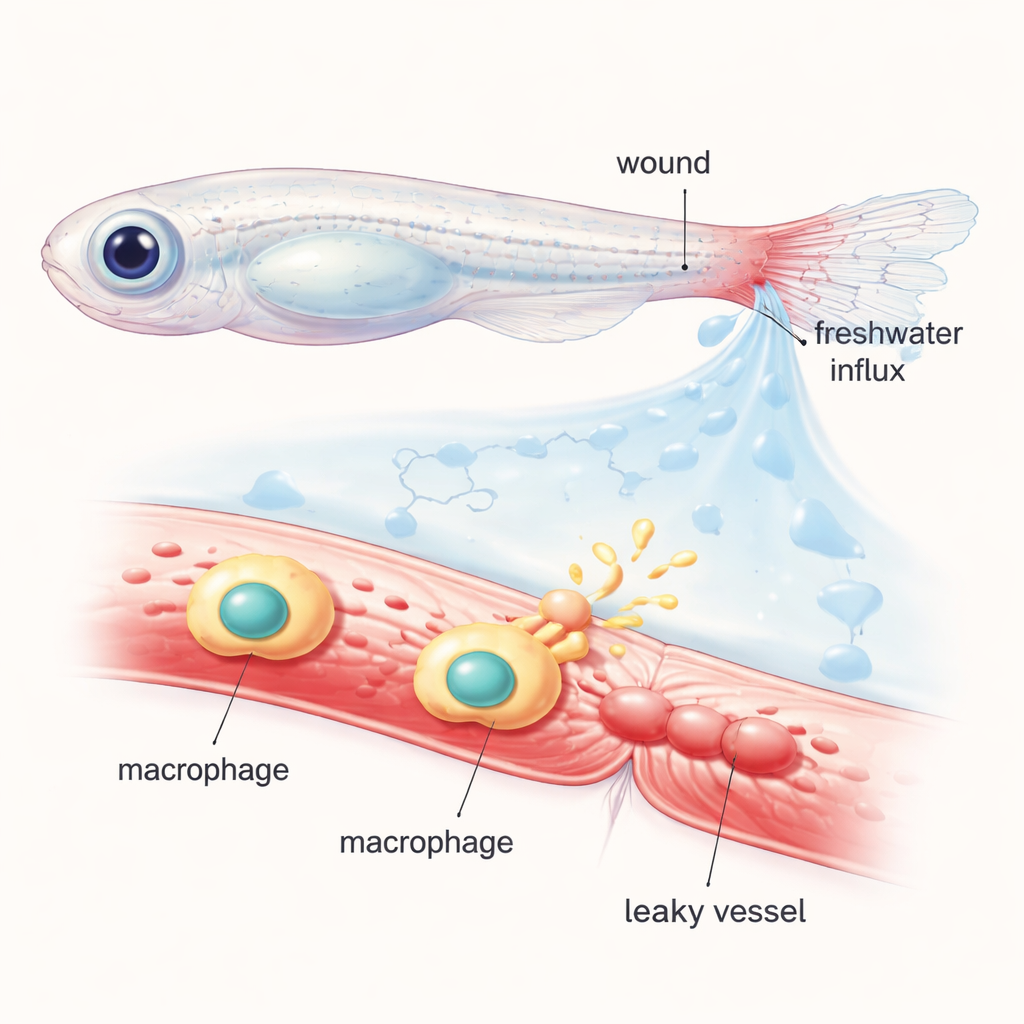
تعقب المرسلات الكيميائية وراء التسرب
لكي يكتشفوا أي الجزيئات تحول الصدمة الفيزيائية إلى إشارة تسرب، فحص العلماء عائلة من المركبات الدهنية تسمى الإيكوسانويدات، المصنوعة من حمض الأراكيدونيك. هذه الدهون معروفة جيدًا بدورها في الالتهاب وتدفق الدم. باستخدام طفرات جينية وأدوية، عطّلوا بشكل انتقائي إنزيمات مفردة في مسار الإيكوسانويد. أدى حظر إنزيم رئيسي يُدعى Alox5a (5-ليبوأوكسجيناز) أو شريكه Lta4h إلى تقليل حاد في مقدار الصبغة التي هربت من الأوعية بعد الصدمة الأسموزية، دون أن يوقف ذلك إغلاق الجرح نفسه. في المقابل، لم يكن للتداخل مع إنزيمات ذات صلة تأثير كبير. وأشار ذلك إلى فرع محدد من مسار الدهون كمحرك رئيسي للاستجابة السريعة للتسرب، يعمل تقريبًا مثل صمام كيميائي يمكن فتحه أو غلقه حسب الطلب.
الدور المُفاجئ للخلايا المناعية العانقة للأوعية
يحتوي الدم على أنواع مختلفة من الخلايا المناعية، وفي يرقات سمك الزرد تُعد الخلايا المتعادلة (النيتروفيلات) والبلاعم اللاعبين الرئيسيين. استخدم الفريق خدعة جينية ذكية لتدمير إما الخلايا المتعادلة أو البلاعم انتقائيًا قبل إحداث الجرح. لم يُحدث إزالة الخلايا المتعادلة فرقًا كبيرًا في تسرب الأوعية. لكن عندما أُزيلت البلاعم، انخفضت استجابة التسرب بحوالي النصف، مما عكس تأثير حظر مسار الدهون Alox5a–Lta4h. ومن المهم أن هذه التعديلات لم توقف إغلاق الجرح بسرعة، مما يبين أن استقطاب الكريات البيضاء وتسرب الأوعية يمكن التحكم فيهما إلى حد ما بشكل مستقل. وكشفت النتائج عن البلاعم المحيطة بالأوعية — البلاعم الجالسة بإحكام على سطح الأوعية الخارجية — كمترجمات أساسية بين الإصابة الفيزيائية وسلوك الأوعية الدموية.
من اجتذاب النواة إلى الإشارة الكيميائية
كيف تكتشف هذه البلاعم المحيطة بالأوعية جرحًا قد يكون على مسافة ما؟ يكمن الجواب في طريقة استجابة نوياتها للإجهاد الميكانيكي. عندما تنتشر الصدمة الأسموزية من الجرح عبر الأنسجة المجاورة، يسبب دخول الماء تورمًا خفيفًا للخلايا وتشوهًا نُويًّا. وسجل الباحثون إنزيمًا حساسًا للضغط الميكانيكي يُدعى cPla2 بعلامة فلورية وعبروا عنه خصيصًا في البلاعم. بعد الجرح في ماء عذب طبيعي، انتقل cPla2 سريعًا إلى السطح الداخلي لغشاء النواة في البلاعم على موجة اجتاحت النسيج بسرعة نحو 50 ميكرومتر في الثانية، متوافقة مع انتشار الأملاح المذابة. اعتمد هذا الانتقال على ظروف ناقصة التوتر وكان أضعف كثيرًا في محاليل متساوية التوتر. أظهرت البلاعم القريبة من الأوعية نبضات حادة وقابلة للانعكاس من ارتباط cPla2 النوي، والتي بدورها تُطلق حمض الأراكيدونيك ليُحوّل إلى الدهون المسببة للتسرب.
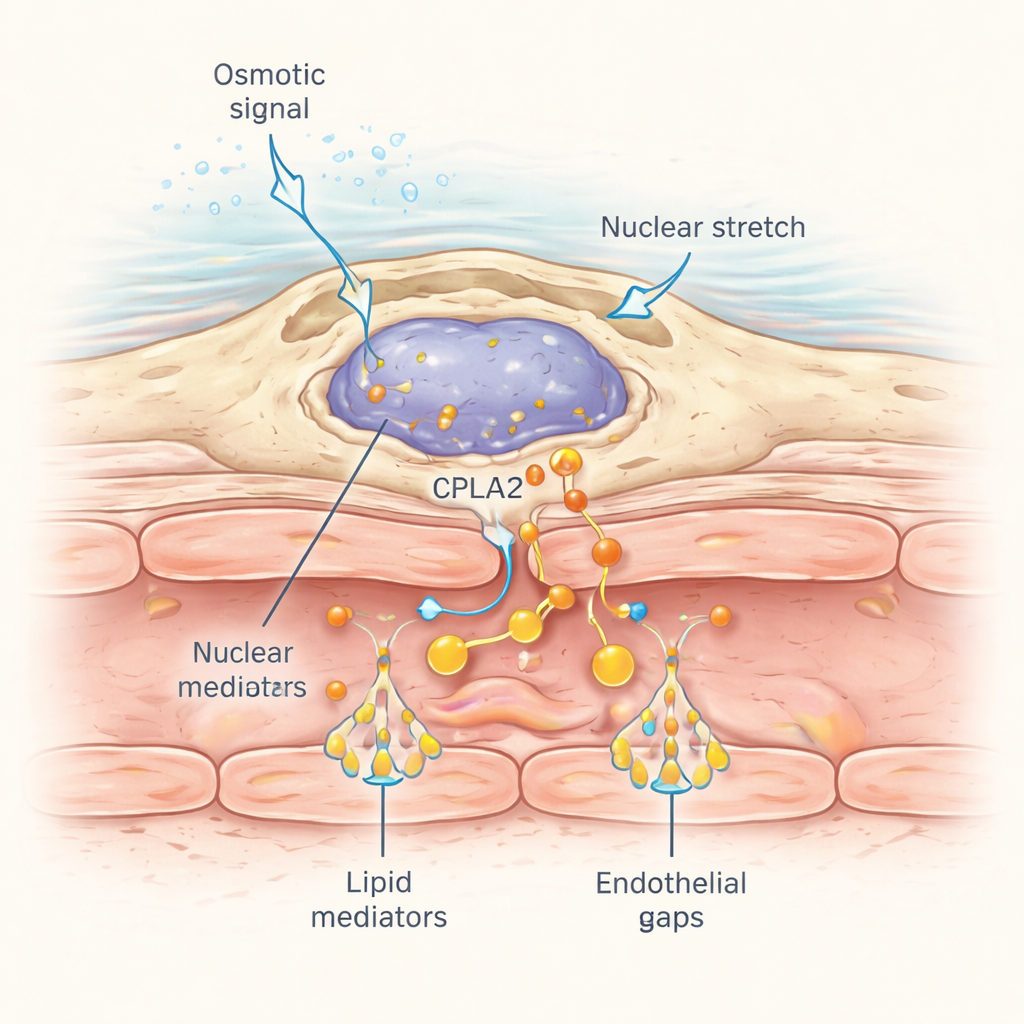
لماذا يهم هذا الأمر خارج نطاق الأسماك
ببساطة، تُظهر هذه الدراسة أن بلاعمًا معينة تعمل كحراس فيزيائيين: تشعر بتمدد الأنسجة والأغشية النوية الناتج عن التغيرات الأسموزية عند الجرح، تُفعّل cPla2 على السطح النووي، وتنتج سريعًا مرسلات دهنية تخبر الأوعية الدموية المجاورة "بفتح البوابات" والسماح بتدفق السوائل والعوامل المناعية. على الرغم من أن سمك الزرد يعيش في ماء عذب ويواجه تحديات أسموزية فريدة، فمن المحتمل أن تعمل مسارات حساسة ميكانيكيًا مماثلة في الأنسجة البشرية المعرضة لتقلبات الضغوط والتدفقات، مثل الرئتين خلال التهوية الميكانيكية. قد يؤدي فهم كيف يتحكم امتداد النواة والإشارات الدهنية في نفاذية الأوعية في الزمن الحقيقي إلى توجيه علاجات تضبط الالتهاب — إما تخفيف التسرب الضار في حالات مثل إصابة الرئة الحادة، أو تعزيز الاستجابات المفيدة لتسريع إصلاح الأنسجة.
الاستشهاد: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
الكلمات المفتاحية: التئام الجروح, الأوعية الدموية, البلاعم, الالتهاب, سمك الزرد