Clear Sky Science · ar
الصيام المتقطع يثبط الأورام الدبقية المدفوعة بـ Tp53 عبر تنظيم ميثيونين-m6A المتوسّط بواسطة ميكروبيوتا الأمعاء
لماذا قد يبطئ إعطاء الأمعاء استراحة الأورام الدماغية القاتلة
الورم الأرومي الدبقي من أشد سرطانات الدماغ عدوانية، والعلاجات الحالية—الجراحة والإشعاع والعلاج الكيميائي—تمنح المرضى غالبًا وقتًا إضافيًا ضئيلاً فقط. تطرح هذه الدراسة سؤالًا بسيطًا لكنه قويًا وله آثار كبيرة على الحياة اليومية: هل يمكن لطريقة أكلنا، وتحديدًا الصيام المتقطع، أن تغيّر بكتيريا الأمعاء وكيمياء الدم بما يكفي لإبطاء بعض أورام الدماغ بشكل ملموس؟
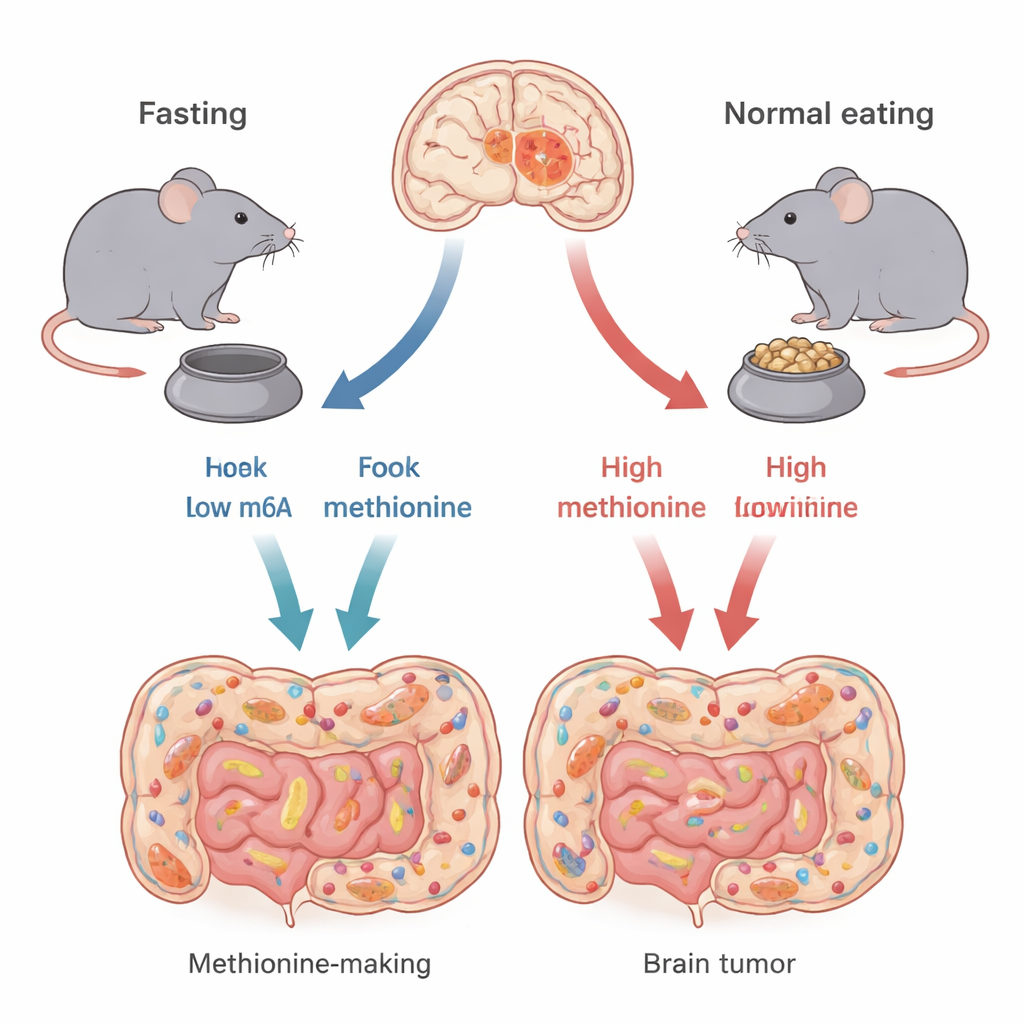
أنواع مختلفة من نفس سرطان الدماغ
ليست كل الأورام الأرومية الدبقية متشابهة. يركز المؤلفون على نوعين وراثيين رئيسيين، يُحددان بتغيُّرات في جينات تسمى TP53 و CDKN2A. هذه الجينات تساعد في تنظيم كيفية نمو الخلايا أو موتها. باستخدام نماذج فأرية تحاكي كل نوع بشري عن قرب، أظهر الباحثون أن الصيام المتقطع—24 ساعة دون طعام تليها 24 ساعة مع طعام—لا يفيد كل الأورام الدماغية بنفس الطريقة. عاش الفئران ذات الأورام من نوع TP53 لفترة أطول وكانت أورامها أصغر عندما صامتت، بينما لم تُظهر فئران النوع CDKN2A فائدة تُذكَر. هذا يشير إلى أن جدوى الصيام قد تعتمد بقوة على البنية الوراثية للورم.
من نمط الأكل إلى بكتيريا الأمعاء إلى كيمياء الدماغ
ثم تساءل الفريق كيف يمارس الصيام تأثيره الانتقائي. لأن إجمالي كمية الطعام ظلَّت مماثلة بين المجموعات، كان الاختلاف الأساسي هو توقيت الأكل. هذا التوقيت أعاد تشكيل ميكروبيوتا الأمعاء—المجتمع الهائل من البكتيريا في الأمعاء—بشكل قوي. في فئران TP53 الصائمة، تراجعت وفرة مجموعات بكتيرية معينة التي تصنع الميثيونين بكفاءة، مثل سلالات محددة من Alistipes و Prevotella. وبما أن الميثيونين هو حمض أميني أساسي يجب على الحيوانات الحصول عليه من الغذاء أو من ميكروبات الأمعاء، فإن هذا التحول الميكروبي أدى إلى تدفُّق أقل من الميثيونين من الأمعاء إلى مجرى الدم وفي النهاية إلى الدماغ.
كيف يضبط مغذٍ واحد إشارات تدفع السرطان
الميثيونين ليس مجرد مغذٍ؛ بل هو أيضًا مادة خام لتكوين S-adenosylmethionine (SAM)، المانح العام للميثيل في الخلية. يغذي SAM عملية وسم كيميائي على الـRNA تُسمى m6A. تساعد هذه الوسوم في التحكم بمدى تعبير جينات معينة. في نموذج ورم TP53، خفض الصيام مستويات الميثيونين وSAM في الدم وفي مناطق أورام الدماغ. باستخدام طبقات متعددة من تقنيات «أوميكس»—تسلسل RNA القياسي، وتوصيف RNA على مستوى الخلية الواحدة، وخرائط مكانية لنشاط الجينات والتمثّلات الأيضية—وجد الباحثون وسوماً أقل من نوع m6A على RNAs المرتبطة بالسرطان تحت الصيام. كان أحد الأهداف المهمة هو TGFB2، جين في مسار إشارات TGF‑β المعروف بأنه يحفز نمو الورم وغزو الأنسجة. مع الصيام انخفض كل من إنزيم METTL3 (الذي يكتب علامات m6A) وTGFB2، وضعفت إشارات TGF‑β.
إثبات السببية بتدخلات مستهدفة
للتجاوز على الارتباط فقط، أجرى العلماء تجارب «إنقاذ». حبسوا METTL3 بدواء، أو نقلوا بكتيريا من أمعاء فئران صائمة إلى فئران مُغذّاة بشكل طبيعي، فتباطأ نمو الورم حتى بدون الصيام—مما يدعم فكرة أن كلًا من الميكروبيوتا وآلية m6A هما لاعبان رئيسيان. وبالعكس، عندما مُنحت فئران الصيام ميثيونين إضافي أو عولجت بدواء يعزز علامات m6A، نمت أورامها بشكل أشبه بأورام الفئران المغذّاة واختفى ميزان البقاء على قيد الحياة. ومن المهم أن تعطيل بكتيريا الأمعاء بمضادات حيوية واسعة المدى محا العديد من التغيرات المرتبطة بالصيام، مما يؤكد أن مجتمع الأمعاء يشكل نقطة محورية في هذه السلسلة من الأحداث.
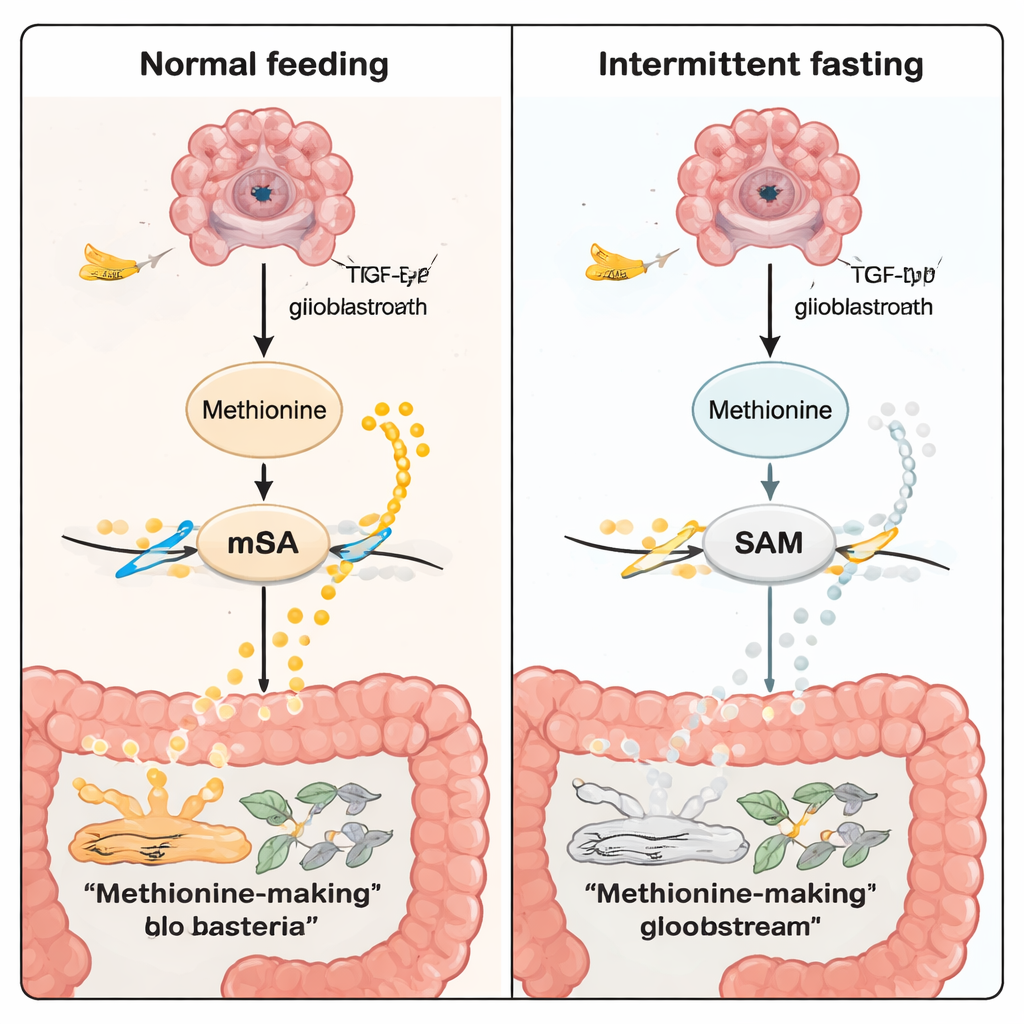
ماذا يعني هذا للناس والعلاجات المستقبلية
للقارئ العام، الرسالة الأساسية أن ليس كل السرطانات، بل حتى ليس كل الأورام الأرومية الدبقية، ستستجيب بنفس الطريقة لاستراتيجية غذائية مثل الصيام المتقطع. في أورام النوع TP53، يبدو أن الصيام «يتواصل» مع الدماغ عبر الأمعاء: يعيد تشكيل بكتيريا الأمعاء، مما يقلل بدوره إنتاج الميثيونين، ويخفض وسم الـRNA الكيميائي، ويكبت الإشارات القوية للنمو داخل خلايا الورم. وبينما أُجريت هذه الدراسة على الفئران وتحتاج إلى ترجمة سريرية حذرة، فإنها تشير إلى مستقبل قد تُخصّص فيه أنماط الحياة البسيطة، وعلاجات مستندة إلى ميكروبيوتا الأمعاء، وأدوية تستهدف مسارات الميثيونين أو m6A وفقًا للنمط الجيني لنوع ورم المريض.
الاستشهاد: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
الكلمات المفتاحية: الصيام المتقطع, الورم الأرومي الدبقي, ميكروبيوم الأمعاء, استقلاب الميثيونين, تعديل RNA m6A