Clear Sky Science · ar
إنزيم TET1 كمنظم رئيسي يتحكم بالمراقبة المعتمدة وغير المعتمدة على GPX4 لموت الخلايا بالنوعية الفيروبتوزية في اللوكيميا النخاعية الحادة
لماذا تهم هذه الدراسة لعلاج السرطان
تهدف العديد من الأدوية الجديدة ضد السرطان إلى دفع الخلايا الخبيثة نحو وضع تدمير ذاتي يُعرف بالفيروبتوزيس، وهو شكل من أشكال موت الخلايا تحركه الحديد وتلف الدهون. ومع ذلك، تقاوم بعض الأورام هذا النهج بعناد. تكشف هذه الدراسة كيف يساعد بروتين يعدل الحمض النووي يدعى TET1 خلايا اللوكيميا على اجتناب الفيروبتوزيس عبر نظامي دفاع كيميائي حيوي منفصلين—وتُظهر أن حجب هذين الدفاعين يمكن أن يجعل حتى السرطانات المقاومة عرضة له.
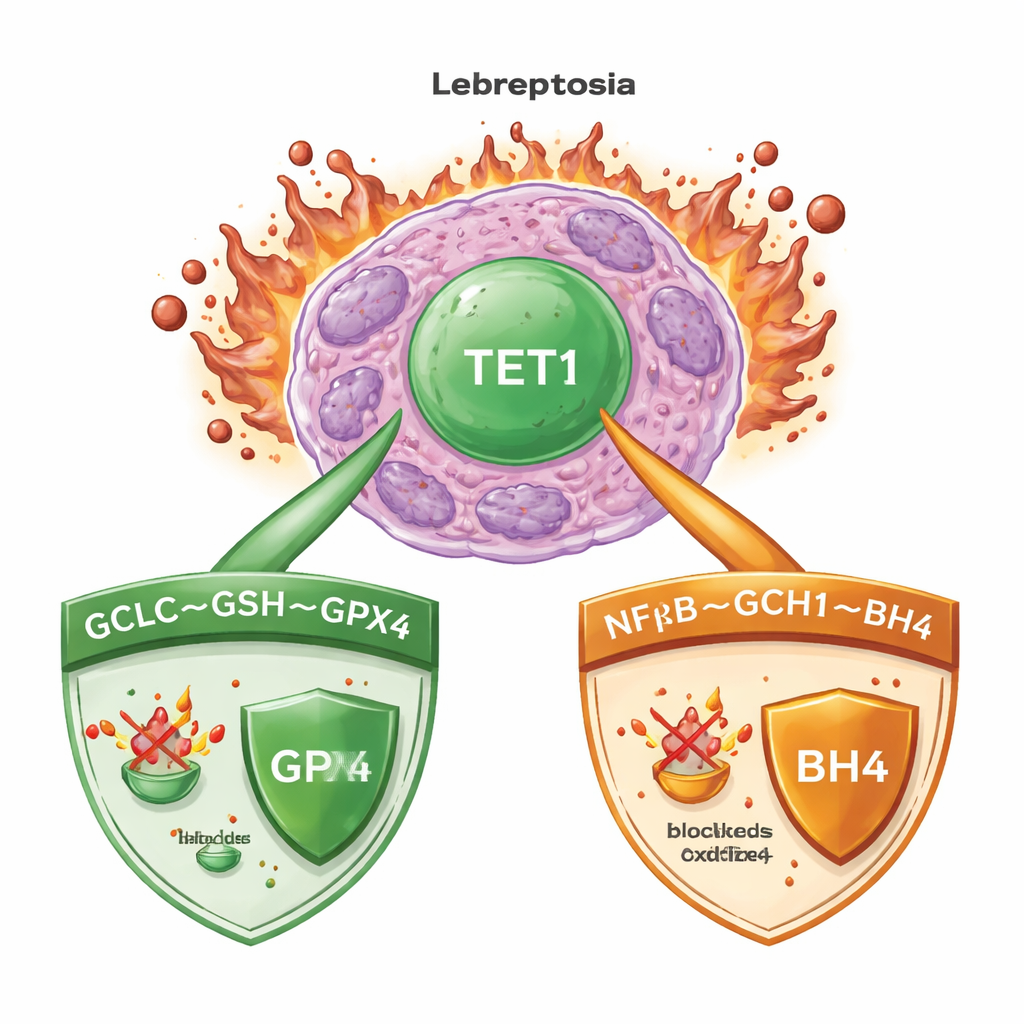
خليط قاتل من الحديد والدهون المتضررة
يحدث الفيروبتوزيس عندما يغذي الحديد أكسدةً خارجة عن السيطرة للدهون في أغشية الخلايا، ما يؤدي في النهاية إلى تمزق الخلايا. في اللوكيميا النخاعية الحادة (AML)، كما في كثير من السرطانات، تُشغّل الخلايا نظم مراقبة قوية لإبقاء هذه العملية تحت السيطرة. من الحراس الرئيسيين إنزيم GPX4، الذي يستخدم جزيئًا صغيرًا يسمى الجلوتاثيون لتحييد البيروكسيدات الدهنية الضارة. وتولد أنظمة احتياطية أخرى جزيئات مضادة للأكسدة يمكنها حجز الجذور الحرة الخطرة حتى عندما يتعرض GPX4 للخلل. إن فهم أي مفاتيح رئيسية تُنسق هذه الدفاعات أمر بالغ الأهمية لتصميم علاجات تُحدث الفيروبتوزيس بشكل موثوق في خلايا السرطان مع الحفاظ على الأنسجة السليمة.
يبرز TET1 كمركز تحكم محوري
قارن الباحثون عشرات من عينات الخلايا السرطانية، بما في ذلك العديد من خطوط AML وخلايا مشتقة من مرضى، ولاحظوا نمطًا واضحًا: الخلايا المقاومة للفيروبتوزيس كانت تتسم بمستويات أعلى من TET1، وهو إنزيم يغير علامات كيميائية على الحمض النووي ويؤثر في نشاط الجينات. عندما قللوا مستويات TET1 باستخدام أدوات جينية أو عطلوه بمركب صغير، أصبحت خلايا السرطان أكثر حساسية لأدوية المحفزة للفيروبتوزيس بشكل ملحوظ. وقد تحقق ذلك في أطباق المختبر ونماذج الفئران للـAML. وبالعكس، أدى تعزيز تعبير TET1 إلى حماية الخلايا من موت الفيروبتوزيس وتقليل تراكم أنواع الأكسجين التفاعلية، وهي المنتجات الجانبية الكيميائية العدوانية التي تُحدث تلف الأغشية.
تقوية الدرع المضاد للأكسدة الرئيسي
بتعمق أكبر، رسم الفريق خريطة مواقع عمل TET1 على الجينوم ووجد أنه ينشّط مباشرة جينًا باسم GCLC. يُشفّر GCLC إنزيمًا حاسمًا يطلق إنتاج الجلوتاثيون، الوقود لعمل GPX4. عبر زيادة علامة حمض نووي محددة (5-هيدروكسيميثيل سيتوزين) عند محفز GCLC، يعزز TET1 تصنيع الجلوتاثيون. في ظروف المغذيات العادية، يزيد هذا من مخزون الخلية المضاد للأكسدة الرئيسي. وفي ظل حرمان السيستين، يصنع نفس التعقيد الإنزيمي أيضًا ببتيدات غاما-غلوتاميل غير اعتيادية تساعد على امتصاص الغلوتامات الزائد، وهي طريقة أخرى لكبح الفيروبتوزيس. في كل من الخلايا المزرعية والفئران، أدى فقدان TET1 أو التثبيط الدوائي لتخليق الجلوتاثيون إلى خفض حاد لمستويات الجلوتاثيون وهذه الببتيدات الواقية، مما جعل خلايا اللوكيميا أكثر عرضة لمسببات الفيروبتوزيس.
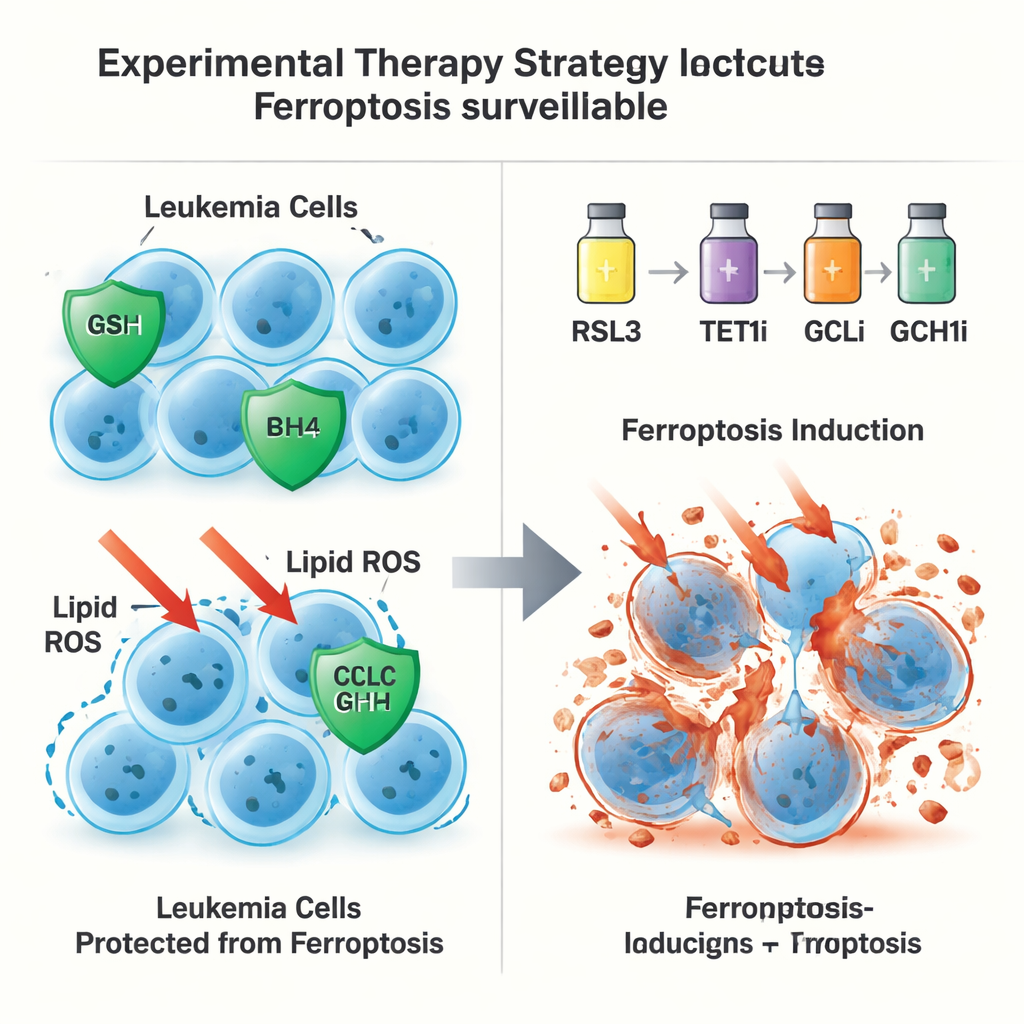
طريق هروب ثانٍ مستقل عن GPX4
على نحو مدهش، لم تنتهِ الحماية التي يوفرها TET1 بمحور الجلوتاثيون–GPX4. حتى عندما أُزيل GPX4 نفسه من خلايا اللوكيميا، كان بإمكان TET1 الزائد أن يمنع موت الفيروبتوزيس، مما يوحي بوجود خط دفاع ثانٍ. وتتبع المؤلفون ذلك إلى تنشيط TET1 لمسار إشارة NFκB، وبخاصة مكوّنًا يُدعى NFKB2. وهذا بدوره يعزز التعبير عن GCH1، إنزيم ينتج الجزيء المضاد للأكسدة BH4. يستطيع BH4 حماية دهون الأغشية من الأكسدة دون الاعتماد على GPX4. عندما سُلك طريق إسكات GCH1 جينيًا أو حُظِر كيميائيًا، فقد TET1 جزئيًا قدرته على حماية الخلايا من الفيروبتوزيس. معًا، تحدد هذه النتائج مسار TET1–NFKB2–GCH1 الذي يشكل نظام مراقبة للفيروبتوزيس مستقلًا عن GPX4.
تحويل نقطة ضعف إلى فرصة علاجية
مسلحين بهذه الخريطة ذات المسارين، اختبر الباحثون ما إذا كان تحفيز الفيروبتوزيس وإضعاف دفاعات TET1 في آن واحد يمكن أن يوفر ميزة علاجية. في نماذج فئران للـAML وزرعات لِقِطعِ لخلايا اللوكيميا المستمدة من المرضى في فئران، أدى الجمع بين جرعات منخفضة من دواء محرض للفيروبتوزيس ومثبطات لـTET1 أو لتخليق GSH (عبر GCLC) أو لـGCH1 إلى خفض كبير في عبء اللوكيميا، وإطالة مدة البقاء، واستنزاف مجموعات الخلايا المبدِئة لللوكيميا. ومن المهم أن المُحَرِّض للفيروبتوزيس استُخدم بكسور من الجرعات المذكورة في دراسات سابقة، مما يقلل المخاوف بشأن السمية لخلايا جذور الدم الطبيعية.
ماذا يعني هذا لعلاجات السرطان المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن خلايا اللوكيميا تنجو عبر تشغيل نظامي "درع" مضاد للأكسدة متداخلين، كلاهما منسق بواسطة TET1: أحدهما يرتكز على الجلوتاثيون وGPX4، والآخر قائم على GCH1 وBH4. تُظهر هذه العمل أنه من خلال تنشيط الفيروبتوزيس بشكل معتدل وفي الوقت نفسه حظر TET1 وشركائه السفليين، قد يتمكن الأطباء في المستقبل من تجاوز المقاومة ودفع خلايا السرطان إلى الانهيار بشكل انتقائي، دون إحداث ضرر مبالغ فيه للأنسجة السليمة. وعلى الرغم من أن هذه الاستراتيجيات لم تصبح جاهزة بعد للاستخدام السريري، فإن الدراسة تُحدد TET1 كنقطة تحكم قوية وهدفا واعدا للعلاجات التوليفية عبر AML وربما سرطانات أخرى يصعب علاجها.
الاستشهاد: Yang, L., Lu, J., Yun, W. et al. TET1 as a master regulator controlling GPX4-dependent and -independent ferroptosis surveillance in acute myeloid leukemia. Nat Commun 17, 1800 (2026). https://doi.org/10.1038/s41467-026-68509-x
الكلمات المفتاحية: الفيروبتوزيس, اللوكيميا النخاعية الحادة, TET1, الجلوتاثيون, علم الوراثة السرطاني الإبيجيني