Clear Sky Science · ar
خلية اصطناعية قادرة على نقل الإشارة بوساطة ADRB2 لتنظيم تحلل الجليكوجين
تعليم الفقاعات الصغيرة كيف تتكلم
تخيل فقاعة صابون مجهرية يمكنها أن تشعر بإشارة شبيهة بالهرمون من الخارج ثم «تقرر» حرق الوقود المخزن داخلها، تمامًا مثل خلية بشرية حقيقية. تبني هذه الدراسة بالضبط ذلك النوع من الخلية الاصطناعية، مُظهِرة كيف يمكن لنماذج الخلايا المصطنعة استقبال رسالة كيميائية وتحويلها إلى كيمياء متحكّم بها تتعلق بالطاقة. هذا العمل يقربنا من حاملات دوائية ذكية وأنسجة مصنّعة ومخلوقات تركيبية بسيطة قادرة على التفاعل مع محيطها.
بناء خلية من الخارج إلى الداخل
الخلايا الحقيقية تستمع باستمرار إلى بيئتها عبر مستقبلات في غشائها الخارجي. سعى المؤلفون إلى تقليد أحد هذه المسارات الطبيعية باستخدام مكوّنات منقّاة وفقاعات دهنية بسيطة، تسمى الحويصلات العملاقة. ركزوا على مستقبل بشري شائع، مستقبل β2 الأدرينرجي (ADRB2)، الذي يساعد في أجسامنا على تنظيم معدل ضربات القلب ووظيفة الرئتين واستخدام الوقود. عندما يلتقي هذا المستقبل بعقار مثل الإيزوبروترينول (ISO)، فإنه عادةً يُطلق سلسلة داخلية من الأحداث التي تُنتج جزيئًا رسولًا يسمى cAMP، والذي يتحكم بدوره في كيفية تفكيك الخلايا للجليكوجين — الشكل المخزن للجلوكوز في الجسم. لم يُنجز سابقًا استنساخ هذه التسلسل الكامل داخل خلية اصطناعية.
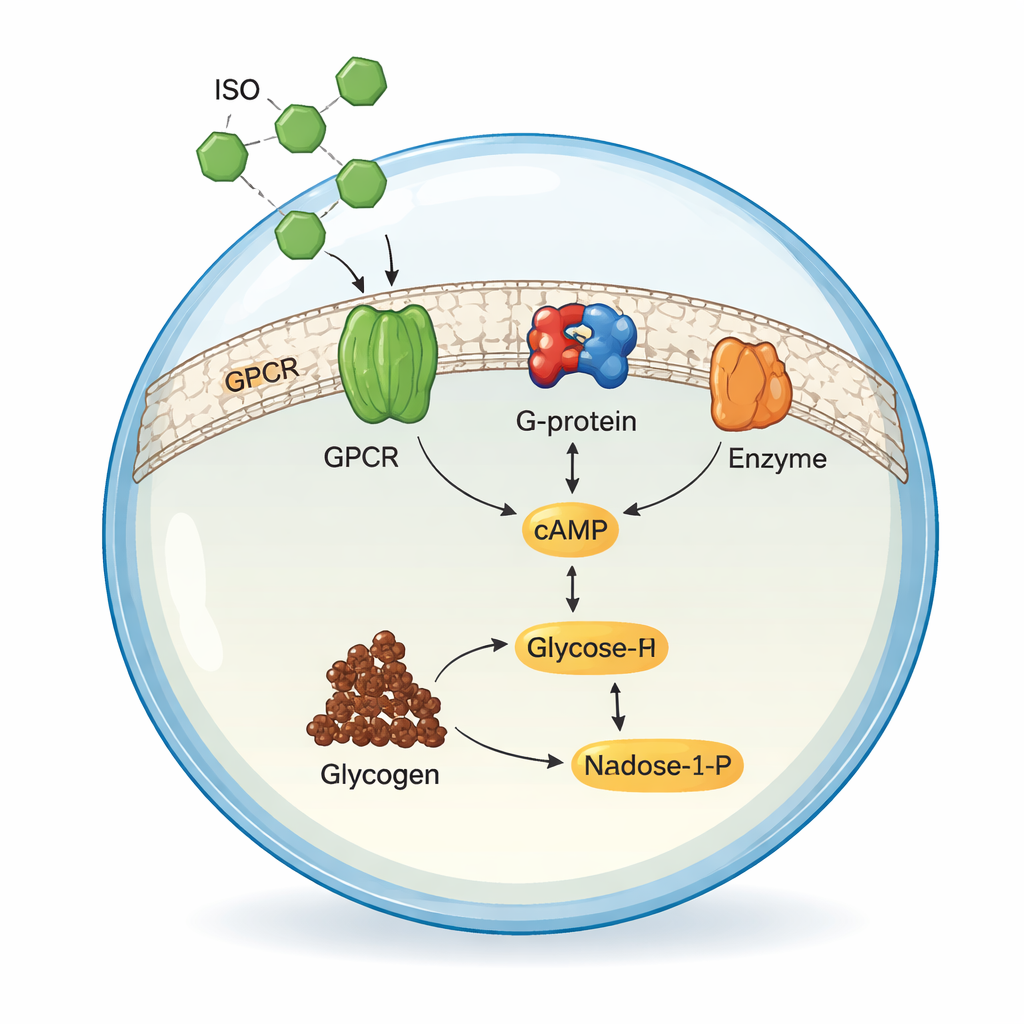
إعادة خلق أولى مراحل نقل الإشارة
بدأ الفريق بإعادة بناء المراحل المبكرة من مسار الإشارة في محلول، خارج أي غشاء. أنتجوا ثلاث بروتينات بشرية في خلايا حشرية: ADRB2، وشريكها من وحدات البروتين G (Gsα)، وإنزيم يدعى أدينيلات السيكلاز V (ADCY5)، الذي يصنع cAMP من ATP. عندما مزجوا هذه المكونات مع ISO تحت ظروف مضبوطة بعناية، أدت تنشيط مستقبل الأدرينالين إلى تحويل ADCY5 للـATP إلى cAMP. بقياس cAMP بواسطة كروماتوغرافيا عالية الأداء، أمكن للباحثين تحسين درجة الحموضة ودرجة الحرارة ومستويات المغنيسيوم، ووجدوا أن نظامهم المُعاد تركيبه عمل بكفاءة مساوية أو أفضل من العديد من التحضيرات السابقة، مما أكد أن كيمياء الإشارة الأساسية كانت متوفرة.
تركيب مستقبلات حقيقية في أغشية اصطناعية
بعد ذلك، غرس المؤلفون البروتينات الثلاثة في أغشية حويصلات أحادية الطبقة عملاقة — فقاعات دهنية بحجم الخلية تعمل كهيكل للخلية الاصطناعية. وضعوا علامات فلورية على ADRB2 وADCY5 للتحقق من أن البروتينات كانت في الغشاء، تتحرك بحرية، ومتواجدة بأعداد كبيرة، بحوالي 1.8 مليون مستقبل لكل حويصلة تقريبًا. أظهر العلاج الإنزيمي أن أكثر من 94% من هذه المستقبلات كانت متجهة بالاتجاه الصحيح، مع تعرّض مواقع الارتباط للخارج. وأكّد مسبار GTP الفلوري أن ارتباط ISO على الغشاء فعلاً نَشّط بروتينات G داخل الحويصلات. هذا يعني أن الخلايا الاصطناعية كانت، من حيث المبدأ، قادرة على نقل إشارة ISO الخارجية عبر غشائها كما تفعل الخلايا الطبيعية.
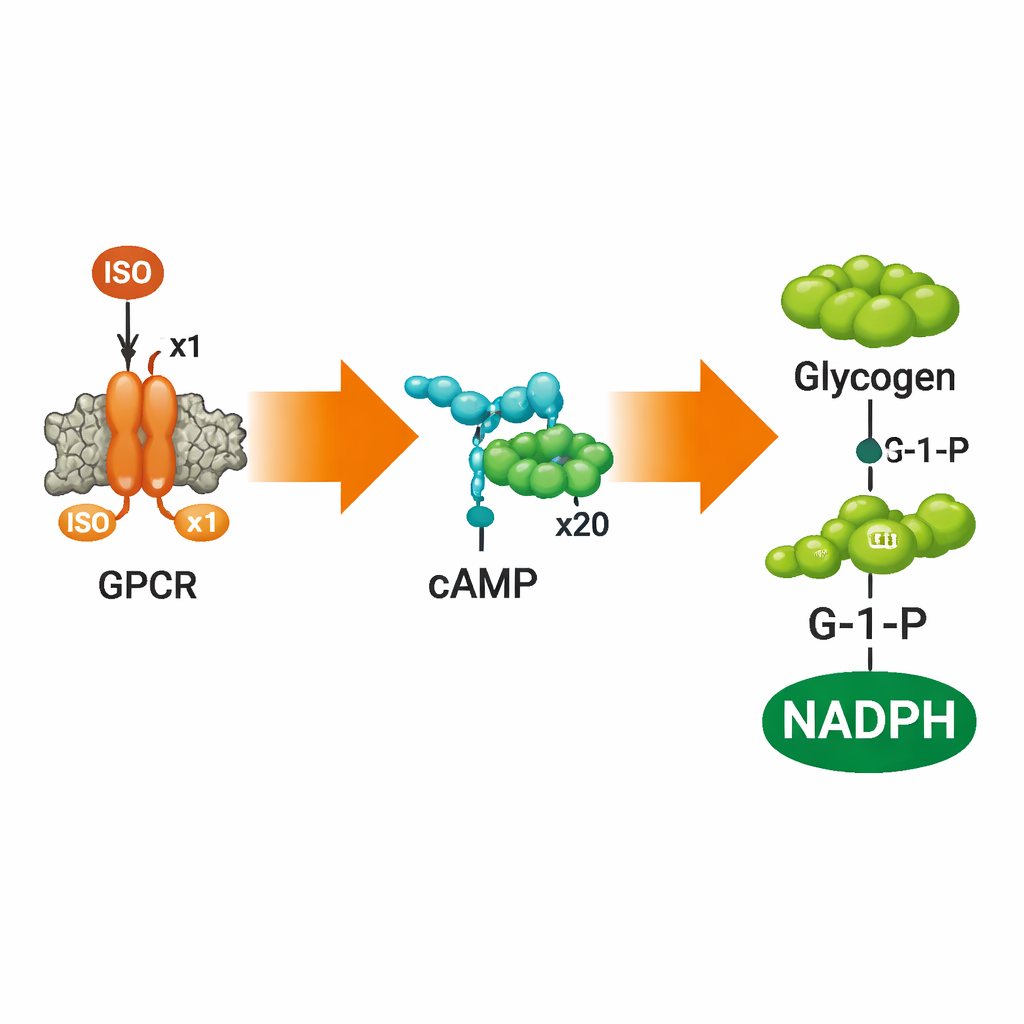
تحويل الإشارات إلى تحلل للوقود
لاختبار ما إذا كانت هذه الخلايا التركيبية قادرة على فعل شيء مفيد بالإشارة، أضاف الفريق جهازًا استشعاريًا لـcAMP ثم مسارًا كاملاً لتحطيم الجليكوجين داخل الحويصلات. باستخدام مسبار cAMP قائم على FRET، أظهروا أن إضافة ISO خارج الحويصلات أدت إلى ارتفاع مستويات cAMP داخلها بشكل يعتمد على الجرعة ثم استقرارها مع تشبع المستقبلات، مما يعكس السلوك الكلاسيكي لمستقبلات المرتبطة ببروتين G الطبيعية. العقاقير التي تحجب أو تُثبّت ADRB2 — مثل ألبيرنولول وكارازولول — أوقفت هذا الاستجابة تمامًا كما هو متوقع. عندما احتوى الباحثون أيضًا على خمسة إنزيمات تحول عادةً الجليكوجين إلى جلوكوز‑1‑فوسفات (G‑1‑P) ثم إلى NADPH، أدت تنشيط ISO إلى إنتاج قابل للقياس لكل من G‑1‑P وNADPH داخل الخلايا الاصطناعية، وتتبّعوا ذلك باستخدام مطيافية الكتلة والكروماتوغرافيا والفلورة.
تكبير همسة إلى صرخة
اكتشاف رئيسي هو مدى تضخيم الاستجابة الداخلية. كمية متواضعة من ISO خارج الحويصلات أنتجت نحو 22 ضعفًا من جزيئات cAMP مقارنة بعدد جزيئات ISO، واستمر هذا التضخيم في النمو في المراحل اللاحقة من المسار. عندما دفعت الإشارة تفكك الجليكوجين وتحويله إلى 6‑فوسفوجلوكونولاكتون مع إنتاج NADPH المصاحب، تجاوز التضخيم الإجمالي مئات المرات. هذا التعزيز المرحلي هو سمة مميزة لإشارات الهرمونات الطبيعية ويُظهر أن النظام الصناعي لا يكتفي بالكشف عن ISO فحسب، بل يعالج الرسالة ويضخمها إلى مخرج أيضي قوي.
لماذا يهم هذا لمستقبل الحياة التركيبية
بالنسبة لغير المتخصص، تتلخص التفاصيل التقنية في فكرة بسيطة: علّم الباحثون خلية بسيطة من صنع الإنسان أن تستمع وتتصرف مثل خلية حية. جزيء دوائي خارجي يرتبط بمستقبل بشري واقعي، تنتقل إشارة عبر غشاء تركيبي، وتستجيب شبكة إنزيمية داخلية بتحريك الطاقة الكيميائية المخزنة. إظهار هذه السلسلة الكاملة — من تنشيط المستقبل إلى الأيض المتحكم — في نظام اصطناعي مبسّط هو خطوة كبيرة نحو خلايا تركيبية مستقلة تستطيع الاستشعار والاتخاذ القرار والعمل بطرق مفيدة، مثل ضبط إمدادات طاقتها أو إيصال علاجات فقط عندما تكتشف الإشارات الكيميائية المناسبة.
الاستشهاد: Liu, Y., Zhao, W., Zhao, Y. et al. An artificial cell capable of signal transduction mediated by ADRB2 for the regulation of glycogenolysis. Nat Commun 17, 1795 (2026). https://doi.org/10.1038/s41467-026-68503-3
الكلمات المفتاحية: خلايا اصطناعية, نقل الإشارة, GPCR, تحلل الجليكوجين, علم الأحياء التركيبي