Clear Sky Science · ar
التحليل الكهربائي الانتقائي لصنع اليوريا من النترات وثاني أكسيد الكربون عند فرق جهد منخفض
تحويل النفايات إلى سماد
تعتمد الزراعة الحديثة بشكل كبير على سماد اليوريا، لكن إنتاجه بالطريقة التقليدية يستهلك الكثير من الوقود الأحفوري ويطلق كميات كبيرة من ثاني أكسيد الكربون. يستكشف هذا البحث مساراً أنظف: استخدام الكهرباء ومواد مصممة خصيصاً لتحويل ثاني أكسيد الكربون والنترات — وكلاهما ملوث شائع — مباشرة إلى يوريا تحت ظروف معتدلة. وإذا ما تم توسيع هذا النهج تجارياً، فقد يساعد على تغذية الناس مع تقليل انبعاثات غازات الاحتباس الحراري والاستفادة الأفضل من تيارات النفايات.
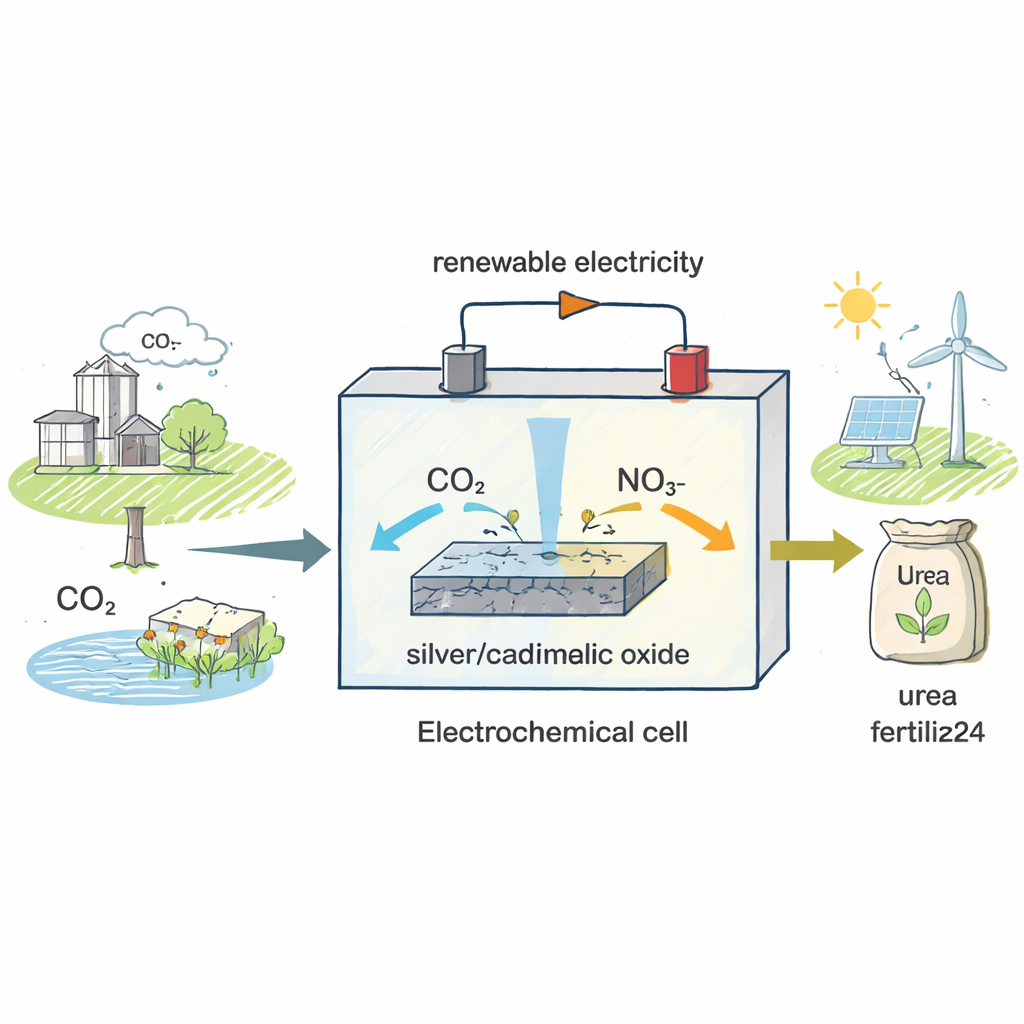
طريقة جديدة لصنع سماد قديم
تعمل مصانِع اليوريا الحالية عند درجات حرارة وضغوط عالية وتعتمد على تكوين الأمونيا أولاً من غاز النيتروجين، وهي خطوة تستهلك وحدها أكثر من 2% من الطاقة العالمية. سعى المؤلفون لتخطي هذا الطريق المرهق للطاقة. بدلاً من البدء من غاز النيتروجين، استخدموا النترات، وهو مركب نيتروجين يوجد في جريان المياه الزراعية ومياه الصرف الصناعي، وجمعوها مع ثاني أكسيد الكربون، غاز الدفيئة الرئيسي. تُغذى المادتان إلى خلية كيميائية كهربائية — جهاز تحفزه الكهرباء لإجراء تفاعلات كيميائية — بحيث، مع المحفز المناسب، يمكن ربطهما لتشكيل اليوريا في درجة حرارة الغرفة وبجهود كهربائية منخفضة نسبياً.
تصميم سطح مساعد
جوهر الجهاز هو محفز صلب مكوّن من جزيئات نانوية تجمع بين الفضة (Ag) وأكسيد الكادميوم (CdO). تُظهر تقنيات المجهر والأشعة السينية أن هذه الجزيئات تُكوّن «هياكل غير متجانسة» متقاربة، حيث تلامس الفضة المعدنية وCdO على مقياس النانو وتتبادل الإلكترونات. يغير هذا التفاعل الإلكتروني بشكل طفيف كيفية ارتباط كل مكون بالجزيئات الداخلة. في ظروف العمل، يتحول جزء CdO إلى كربونات الكادميوم (CdCO₃) التي تحتوي على ذرات أكسجين مفقودة، تُعرف بشواغر الأكسجين. تعمل هذه البقع الفارغة كمواقع ترسيخ صغيرة تساعد على التقاط وتنشيط ثاني أكسيد الكربون، بينما تكون مناطق الفضة القريبة جيدة بشكل خاص في التقاط أنواع تحتوي على نيتروجين مشتقة من النترات.
إنتاج اليوريا بكفاءة وانتقائية
عندما يتدفق ثاني أكسيد الكربون والنترات عبر هذا المحفز Ag/CdO في خلية مخبرية، يحولهما المادة إلى يوريا عند فرق جهد إضافي غير معتاد المنخفض، أي أن الجهد الإضافي فوق المتطلب الحراري المثالي صغير. في خلية بسيطة على شكل حرف H، يصل التركيب الأمثل المسمى Ag₀.₀₇/CdO إلى انتقائية لليوريا تبلغ نحو 50% عند −0.10 فولت مقابل مرجعية قياسية، وينتج كميات ضئيلة من الأمونياأو أول أكسيد الكربون كمنتجات ثانوية. في خلية تدفق متقدمة، حيث تُزود الغازات والسوائل باستمرار، يحقق نفس المحفز معدل إنتاج عالي لليوريا بنحو 112 مليمول لكل غرام من المحفز في الساعة عند −0.15 فولت. ومن خلال تحسين تصميم المفاعل وظروف التشغيل، يدفع الفريق معدل إنتاج اليوريا إلى نحو 427 مليمول لكل غرام في الساعة عند تيارات أعلى، مع الحفاظ على الأداء لمدة 1000 ساعة تشغيل مستمر — وهو مؤشر مهم على الاستقرار.
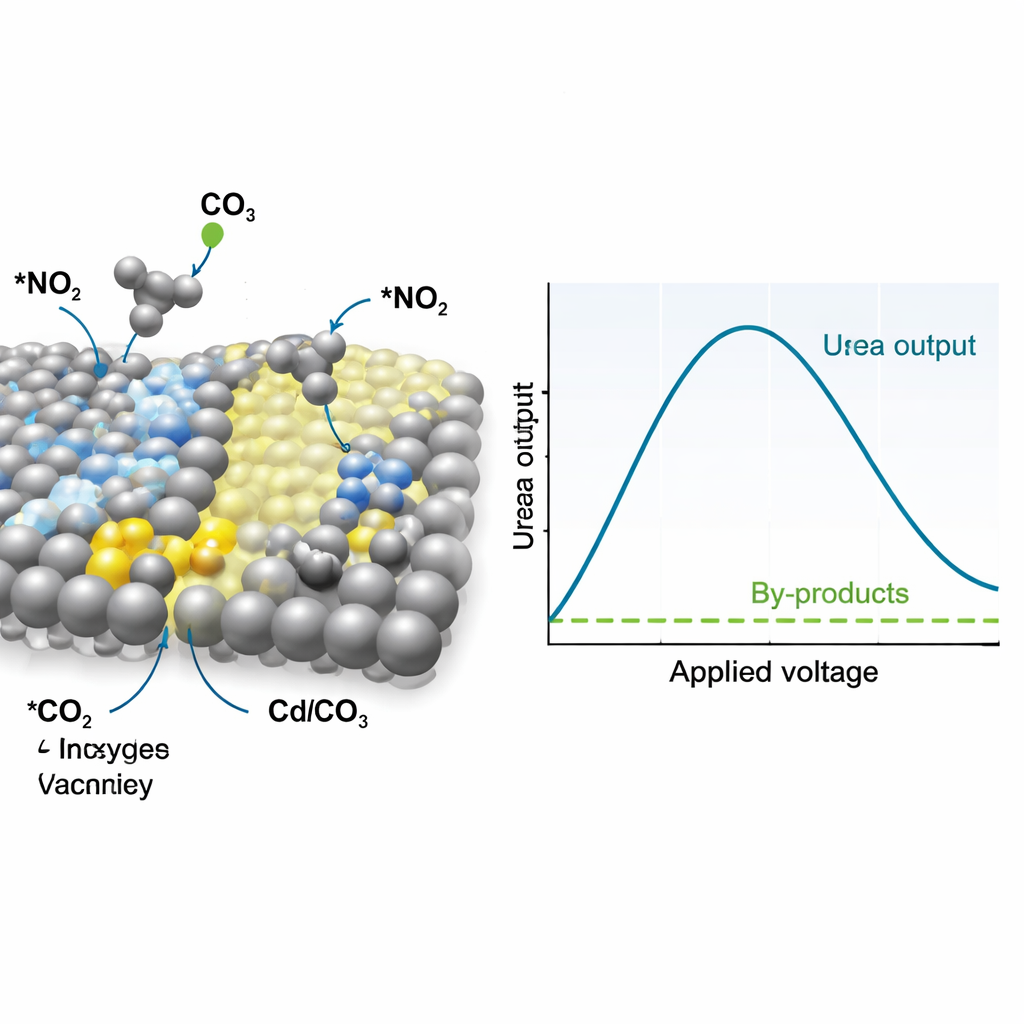
كيف يوجه المحفز التفاعل
لفهم سبب فاعلية هذه المادة، راقب الباحثون المحفز ووسائط التفاعل في الوقت الحقيقي باستخدام طيف رامان والأشعة تحت الحمراء، إلى جانب مجسات أشعة سينية متقدمة. تشير هذه القياسات إلى أن مواقع الفضة تحول النترات تفضيلياً إلى وسيط تفاعلي موصوف غالباً على أنه *NO₂، بينما يربط CdCO₃ المعاد تكوينه والمشحون بشواغر الأكسجين ثاني أكسيد الكربون ويحوّله إلى *CO، وهو وسيط قصير العمر آخر. تظهر إشارات مرتبطة بروابط الكربون–النيتروجين عند جهود التشغيل، مما يدل على أن *NO₂ و*CO يتزاوجان مبكراً في العملية لتشكيل مركب يشبه اليوريا بدلاً من الانحراف لتكوين الأمونيا أو أول أكسيد الكربون بشكل منفصل. تدعم المحاكاة الحاسوبية هذه الصورة، كاشفة أن الواجهة بين الفضة وCdCO₃ الغني بالشواغر تقلل حاجز الطاقة لخطوة ربط C–N الأساسية وتجعلها أكثر تفضيلاً مقارنةً بالتفاعلات المتنافسة.
ماذا قد يعني هذا للأسمدة والمناخ
بشكل عام، يبرهن العمل أن الأسطح المحفزة المصممة بعناية يمكن أن توجه جزيئات نفايات بسيطة مثل ثاني أكسيد الكربون والنترات على مسار فعال من حيث الطاقة نحو اليوريا، تحت ظروف معتدلة ومدة تشغيل طويلة. للناظر غير المتخصص، الخلاصة الأساسية هي أن الفريق بنى نوعاً من «المرشح الإلكتروني» الذي يفضّل ربط الكربون والنيتروجين في اليوريا بدلاً من السماح لهما بالهروب كمنتجات أخرى. وبينما سيتطلب النشر في العالم الحقيقي معالجة قضايا مثل تكلفة المواد، وهندسة المفاعلات، والحصول على الكادميوم بأمان، يقدم البحث مخططاً أولياً لإنتاج أسمدة مستقبلية يمكن تشغيلها بالكهرباء المتجددة وتنسجم مع دورة كربون ونيتروجين أكثر استدامة.
الاستشهاد: Liu, S., Wang, T., Liu, J. et al. Selective electrosynthesis of urea from nitrate and carbon dioxide with low overpotential. Nat Commun 17, 1787 (2026). https://doi.org/10.1038/s41467-026-68497-y
الكلمات المفتاحية: التحليل الكهربائي لليوريا, استخدام ثاني أكسيد الكربون, اختزال النترات, تصميم المحفز الكهربائي, أسمدة خضراء