Clear Sky Science · ar
حلقة التغذية الراجعة الإيجابية بين UFL1‑AKT تعزز تقدم سرطان الثدي عبر تعزيز تخليق الدهون
لماذا تهتم الخلايا السرطانية بالدهون إلى هذا الحد
تحتاج خلايا سرطان الثدي، كما الحال في جميع الخلايا سريعة النمو، إلى إمداد ثابت من اللبنات لبناء أغشية جديدة وجزيئات إشارات. الدهون، أو الليبيدات، تشكل جزءًا أساسيًا من هذا الإمداد. تكشف هذه الدراسة كيف يحول نظام بروتيني قليل الشهرة خلايا السرطان إلى "وضع إنتاج دهون مفرط"، ما يساعد الأورام على النمو والهروب من العلاجات. فهم هذا المصدر المخفي للوقود قد يفتح طرقًا جديدة لإبطاء أو تجويع سرطانات الثدي.
وسم بروتيني خفي بعواقب كبيرة
تعدل خلايانا سلوك بروتيناتها باستمرار باستخدام وسوم كيميائية صغيرة. أحد هذه الوسوم، المسمى UFM1، يُضاف بواسطة إنزيم يُدعى UFL1. رُبط وسم UFM1 (UFMylation) بإصلاح الحمض النووي واستجابات الإجهاد، لكن دوره في السرطان لم يكن واضحًا. تُظهر الدراسة أن نشاط UFL1 أعلى بكثير في أورام الثدي البشرية مقارنة بالنسيج الثديي الطبيعي، وعبر جميع الأنواع الفرعية الرئيسية. المرضى الذين تحمل أورامهم مستويات أعلى من UFL1 يميلون إلى الحصول على بقاء أقل. عندما قلل الباحثون من مستوى UFL1 في خلايا سرطان الثدي أو في أورام الفئران، تباطأ نمو السرطان، وانخفض الانقسام الخلوي، وزاد موت الخلايا، ما يشير إلى أن UFL1 يتصرف كعامل يروج للسرطان.
كيف يتحول محور الإشارات إلى وضع صنع الدهون
لفهم كيف يساعد UFL1 الأورام، بحث الفريق عن شركائه الجزيئيين ووجدوا بروتينًا محوريًا للتحكم بالإشارات يدعى AKT1. AKT1 هو مفتاح مركزي يخبر الخلايا بالنمو وتصنيع ليبيدات جديدة. تُظهر الدراسة أن UFL1 يرتبط ماديًا بـ AKT1 ويزيّنه بوسوم UFM1 في عدة مواقع محددة. يغيّر هذا الوسم شكل AKT1، مزيلاً "الفرامل" الداخلية التي تبقيه عادة في حالة خمول. كما يساعد ذلك AKT1 على الانتقال إلى حجرة غشائية داخل الخلية، الشبكة الإندوبلازمية، حيث يمكن لإنزيمات أخرى تنشيطه تمامًا عبر إضافة مجموعات فوسفات. بدون وسوم UFM1 في تلك المواقع، يصبح تنشيط AKT1 أصعب بكثير.
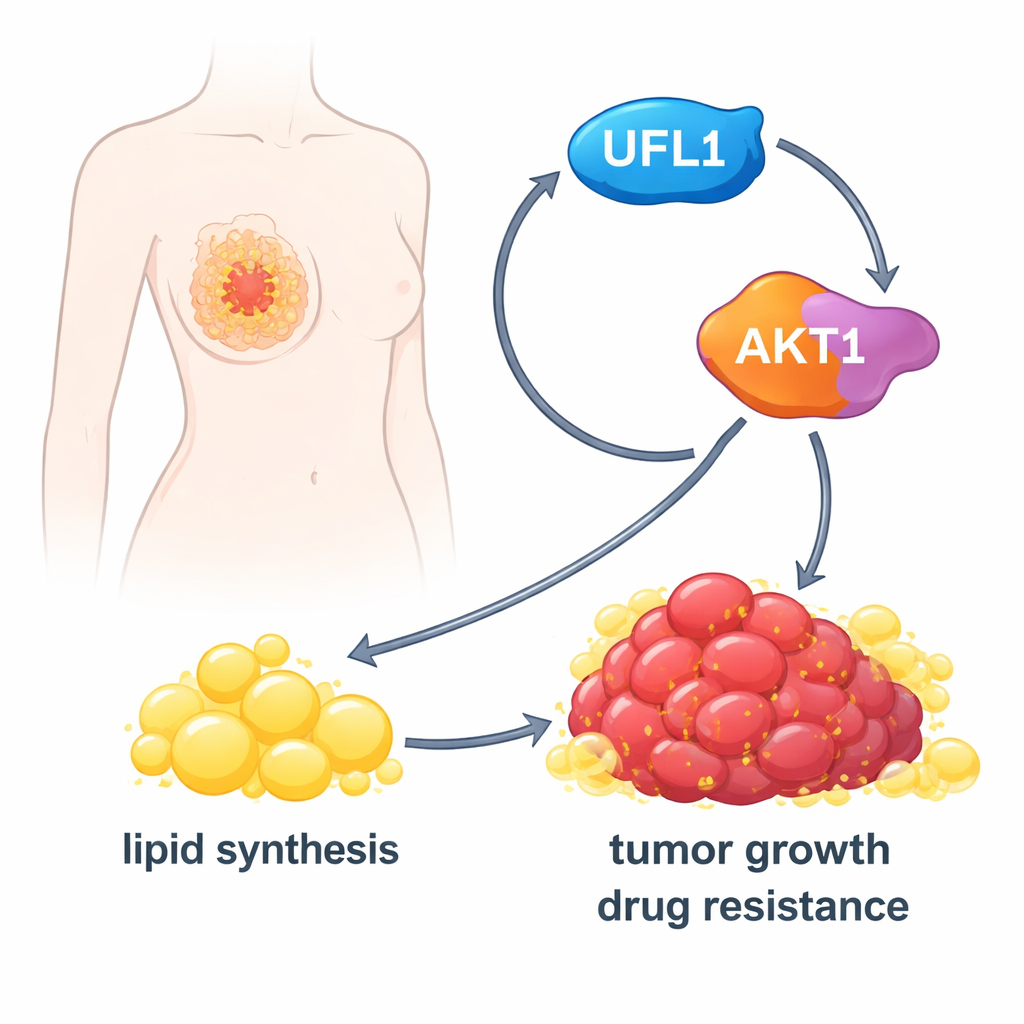
تشغيل مصنْع الدهون السرطاني
بمجرد تنشيطه، يدفع AKT1 الخلايا لزيادة إنتاج الدهون. يعزز نشاط إنزيم أيضي رئيسي، ACLY، ويرفع مستويات منظمات رئيسية مثل SREBP1 التي تشغل العديد من جينات تصنيع الدهون. في خلايا سرطان الثدي المزروعة مخبريًا، أدت زيادة UFL1 إلى تراكم قطرات دهنية وأحماض دهنية حرة وكولسترول أكثر. أدى إزالة UFL1 إلى تقليل حاد في مخزون الليبيدات هذا، سواء في الأطباق المخبرية أو في الأورام المزروعة في الفئران. وقد أدى تزويد الخلايا بأحماض دهنية إضافية من خارج الخلية إلى إنقاذ نمو الخلايا السرطانية الناقصة UFL1 إلى حد كبير، مما يشير إلى أن التأثير الرئيسي لـ UFL1 هو تأمين كمية كافية من الليبيدات لدعم توسع الورم.
حلقة تعزيز ذاتي تدفع نمو الورم
بشكل مفاجئ، العلاقة بين UFL1 وAKT1 تعمل في اتجاهين. اكتشف الباحثون أنه بمجرد أن ينشط AKT1، يضيف بدوره وسمًا فوسفاتيًا إلى UFL1 في موقع معين. تعزز هذه التعديل قدرة UFL1 على وسم AKT1 بـ UFM1، مكوّنة حلقة تغذية راجعة إيجابية: يفعل UFL1 AKT1، ويفعل AKT1 UFL1. يؤدي تحوير أي من مواقع وسم UFM1 على AKT1 أو موقع الفسفرة على UFL1 إلى كسر هذه الحلقة. في الفئران، نمت الأورام الحاملة لهذه النسخ المحورة بشكل ضعيف، واحتوت على دهون أقل، وأظهرت خلايا متوفية أكثر. في عينات مرضى سرطان الثدي ثلاثي السلبية، وجدت مستويات أعلى من UFL1 النشط وAKT1 النشط غالبًا معًا، مما يؤكد أن هذه الحلقة تعمل في الأورام الحقيقية.
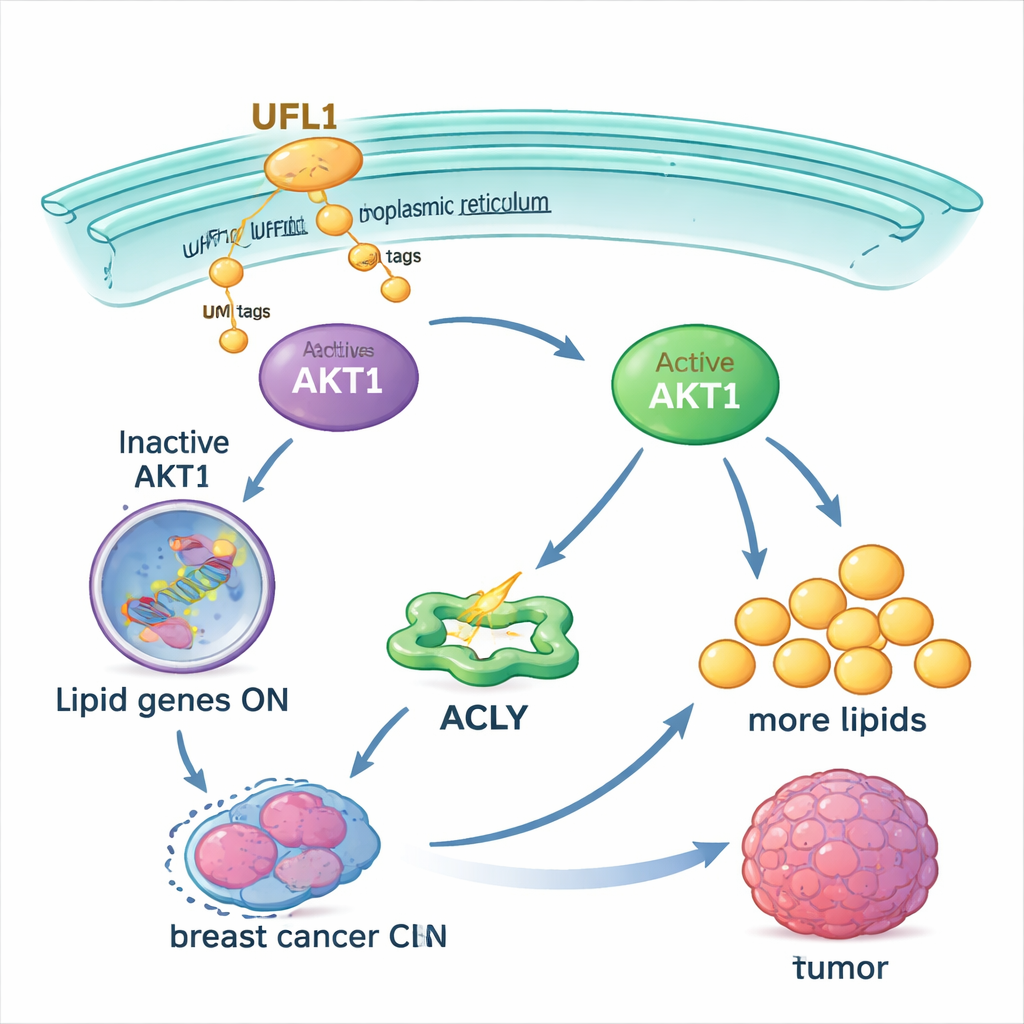
إضعاف الحلقة لمساعدة العلاجات على النجاح
نظرًا لأن تجارب دوائية عديدة تستهدف AKT بالفعل، اختبر المؤلفون ما إذا كان حظر UFMylation يمكن أن يجعل هذه العلاجات أكثر فاعلية. في خلايا سرطان الثدي، خفض كل من مثبط صغير لجزيئات UFMylation ومثبط AKT نشاط AKT1 وتراكم الدهون، لكن الجمع بينهما كان أفضل بكثير من أي منهما منفردًا. كما أبطأ المزيج نمو الأورام وقلل محتوى الدهون في أورام الفئران دون فقدان وزن ملحوظ لدى الحيوانات. كما جعل حظر UFMylation الخلايا السرطانية أكثر حساسية للعلاجات الكيميائية القياسية مثل السيزبلاتين والإيتوبوسيد، التي غالبًا ما تفشل عندما يكون AKT نشطًا بدرجة عالية.
ما الذي يعنيه هذا للمرضى
تُبيّن الدراسة للقارئ العام أن بعض سرطانات الثدي تُجهيز نفسها بحلقة تغذية راجعة تعزز نموها وإمدادها بالدهون. يعمل UFL1 وAKT1 معًا كالبدالين المضغوطين في آن واحد: أحدهما يوسم، والآخر يرسل الإشارات، ومعًا يقودان إنتاج الليبيدات وتوسع الورم. من خلال العثور على أدوية تتداخل مع هذه الحلقة—سواء عبر حظر UFMylation أو AKT1 أو تفاعلهما—قد تتمكن العلاجات المستقبلية من إبطاء نمو الورم وجعل العلاجات الحالية أكثر فاعلية، لا سيما في الأنواع العدوانية من سرطان الثدي.
الاستشهاد: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
الكلمات المفتاحية: سرطان الثدي, استقلاب الدهون, إشارات AKT, UFMylation, العلاج المستهدف