Clear Sky Science · ar
التصوير متعدد القياس على الحموضة المدفوعة بمضخات البروتون لتقييم تقدم الورم والنقائل
لماذا تهم حموضة الورم
السرطان لا ينمو بمعزل عن محيطه. تُعيد خلايا الورم تشكيل البيئة المحيطة بها، فتخلق محيطًا قاسٍ وحامضيًا يساعدها على الانتشار ومقاومة العلاج. تركز هذه الورقة على سرطان الكبد وتُظهر كيف أن قياس تلك الحموضة في الأنسجة الحية يمكن أن يكشف عن الأورام مبكرًا، ويتتبع تطورها، بل ويُرشد استراتيجيات علاجية جديدة تهاجم خلايا السرطان والبيئة الحمضية التي تخلقها على حد سواء.
توقيع كيميائي خفي للسرطان
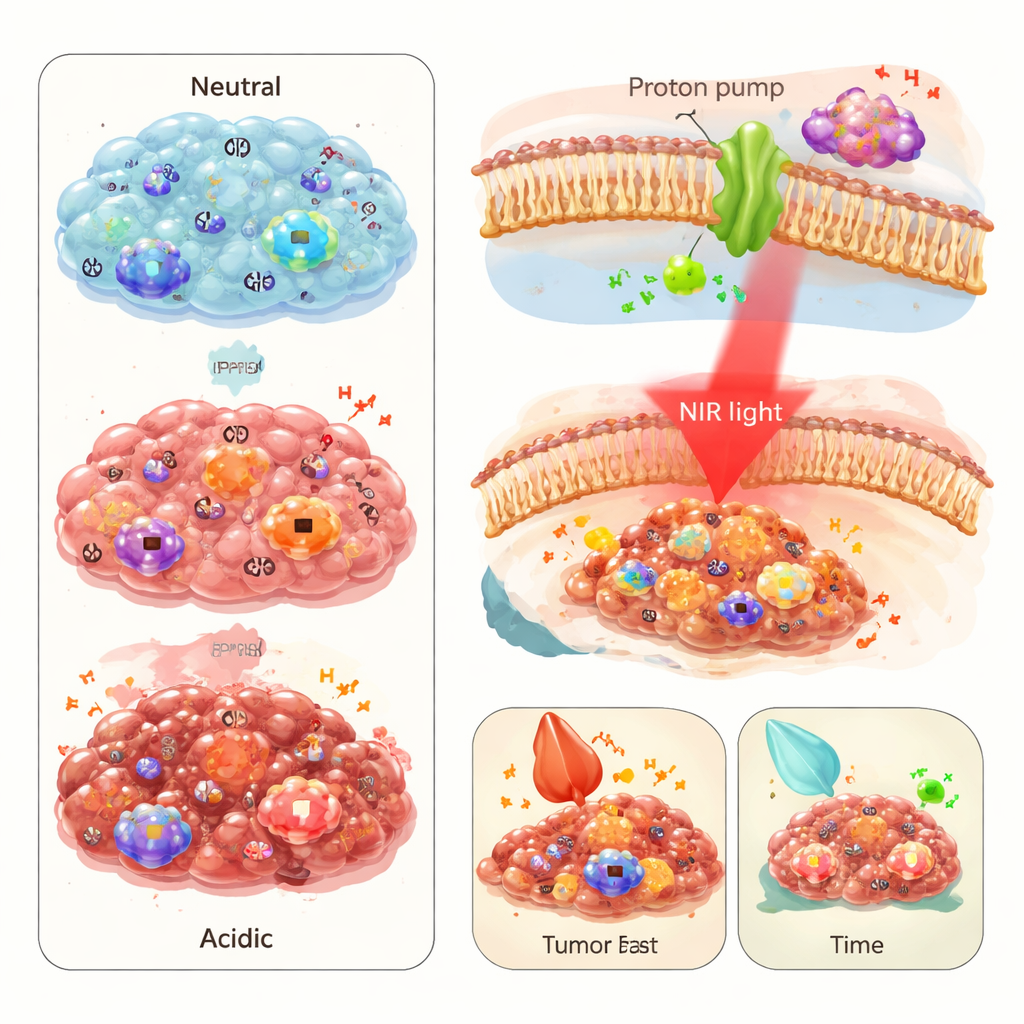
تعتمد العديد من الأورام، بما في ذلك سرطان الكبد الكَيتِليَّة (أحد سرطانات الكبد الشائعة)، على أيض جائع للسكريات يُنتج حمضًا فائضًا. تستخدم خلايا السرطان مضخات البروتون في أغشيتها لدفع أيونات الهيدروجين (H+) الزائدة إلى الخارج، مما يجعل المساحة حول الورم أكثر حموضة من النسيج الطبيعي. يحدد المؤلفون مكوّنًا واحدًا من هذه المضخات، ATP6V0C، على أنه ذو أهمية خاصة. في مجموعات بيانات مرضى كبيرة وعينات أورام حقيقية، كانت مستويات ATP6V0C أعلى في أورام الكبد مقارنة بالأنسجة السليمة المجاورة، وارتفعت مع تقدّم السرطان، وكانت مرتبطة ببقاء أسوأ. يشير هذا إلى أن إنتاج الحمض المدفوع بـATP6V0C ليس مجرد أثر جانبي للسرطان، بل محرك للنمو والغزو والانتشار.
تحويل الحموضة إلى صورة
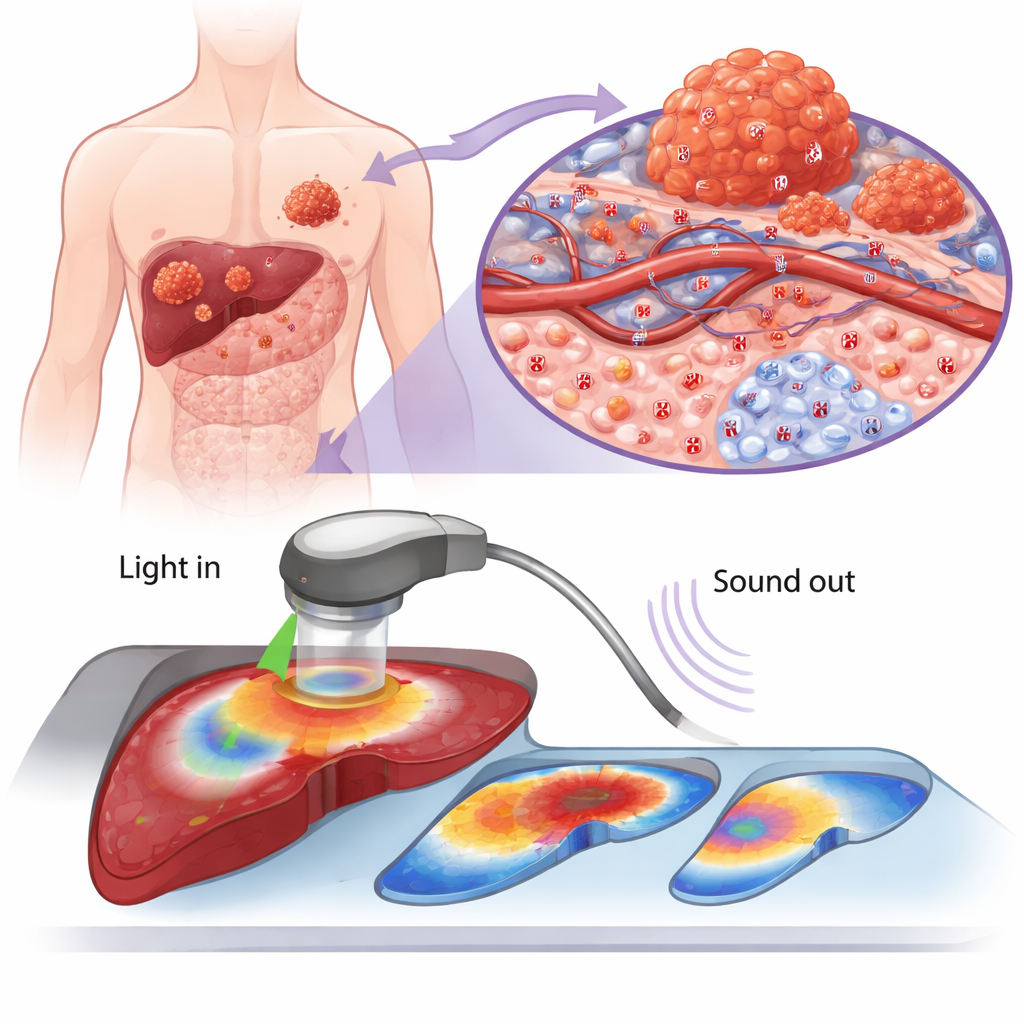
لتحويل هذا التغير الكيميائي غير المرئي إلى شيء يمكن للأطباء رؤيته، بنى الفريق مجسًا صغيرًا يسمى PPS (مستشعر فوتوأكوستي حساس للحموضة). PPS مصنوع من بوليمر موصل يغيّر سلوكه البصري اعتمادًا على الحموضة. في ظروف معتدلة، يكون PPS هادئًا نسبيًا؛ في البيئات الحمضية مثل تلك القريبة من الأورام، يتغيّر شكله ويمتص الضوء القريب من تحت الحمراء بقوة. عندما يصطدم ضوء نبضي بـPPS، يسخن ويتمدد مؤقتًا، مولدًا موجات فوق صوتية يمكن التقاطها من خارج الجسم. بقياس الإشارات عند طولين موجيين مختلفين وأخذ نسبتها، أنشأ الباحثون خريطة للحموضة حساسة وأقل تأثرًا بالضوضاء الخلفية.
مراقبة تطور الأورام في الأنسجة الحية
باستخدام هذا المجس في الفئران، تتبّع المؤلفون كيف تُحمض أورام الكبد بيئتها الميكروية مع مرور الوقت. حتى عندما كانت الأورام صغيرة جدًا بحيث لا تُرى بالعين، كشف التصوير الفوتوأكوستي المبني على PPS عن انخفاض تدريجي في الرقم الهيدروجيني المحلي مع تكاثر خلايا السرطان، وتشوه الأوعية الدموية، وهبوط مستويات الأكسجين. في كل من أورام الكبد المزروعة ونقائل الكبد من سرطان البنكرياس، أظهر PPS مناطق حمضية تطابقت مع مواقع الأورام التي رُصِدت في التصوير القياسي وفي شرائح النسيج تحت المجهر. يمكن أن يميز نفس النهج بين العقد اللمفاوية الحميدة والناقلة في نموذج فأري ويميّز بوضوح حدود أورام الكبد البشرية في عينات جراحية، مما يلمّح إلى استخدام مستقبلي لمساعدة الجراحين على استئصال كل النسيج السرطاني.
حجب مضخات الحموضة وتسخين الأورام من الداخل
تتجاوز الدراسة التصوير لتختبر كيف يمكن للتداخل مع ضخ البروتون أن يبطئ السرطان. أظهر الباحثون أن الإيزوميبرازول، مُثبِّط حمض شائع يُستخدم لحالات المعدة، يمكنه الارتباط بـATP6V0C، وتقليل نشاطه في خلايا سرطان الكبد، وجعل بيئة الورم أقل حموضة مؤقتًا في الفئران. أصبحت خلايا السرطان المعرضة لهذا الدواء أقل قدرةً على الحركة والغزو. في الوقت نفسه، يتصرف PPS نفسه كمسخن صغير في الظروف الحمضية: عندما يُضاء بضوء قريب من تحت الحمراء، يسخن أكثر في الأورام الحمضية منه في الأنسجة الطبيعية، مسببًا تلفًا لخلايا السرطان المجاورة. في نماذج الفئران، أدى الجمع بين العلاج الضوئي الحراري المعتمد على PPS والإيزوميبرازول إلى تقلص أقوى للأورام مقارنة بكل نهج بمفرده.
تداعيات لرعاية السرطان المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن الحموضة علامة مبكرة ويمكن اتخاذ إجراء بشأنها فيما يتعلق بنشاط السرطان. تُظهر هذه الدراسة أنه أصبح من الممكن الآن رسم خريطة تلك الحموضة في الأنسجة الحية بدقة عالية، وتتبع كيف تتغير أثناء نمو الأورام أو استجابتها للعلاج، وتصميم علاجات تُفعّل بواسطة الحموضة نفسها التي تجعل الأورام خطرة. وعلى الرغم من أن الطرق ما تزال في مرحلة تجريبية ومركزة على سرطان الكبد، فإن نهج تصوير واستهداف «التربة الحمضية» التي تغذي الأورام قد يساعد في النهاية على اكتشاف السرطانات مبكرًا، وتخطيط الجراحة بدقة أكبر، وضبط تركيبات الأدوية لتحقيق نتائج أفضل.
الاستشهاد: Zeng, S., Chen, J., Ren, Y. et al. Multiscale imaging on proton pump-driven acidity for assessing tumor progression and metastasis. Nat Commun 17, 1785 (2026). https://doi.org/10.1038/s41467-026-68491-4
الكلمات المفتاحية: البيئة الميكروية للورم, سرطان الكبد, التصوير الفوتوأكوستي, حموضة الورم, مثبطات مضخة البروتون