Clear Sky Science · ar
هيدروجيل خزانٍ خلوي يتجمع داخل الورم لتنسيق العلاج الإشعاعي-المناعي متعدد المراحل
تحويل الإشعاع إلى سلاح أكثر ذكاءً ضد السرطان
يعد العلاج الإشعاعي من أكثر العلاجات شيوعاً للسرطان، لكن الأورام غالباً ما تنجو بخداع الجهاز المناعي وتعيش في ظروف منخفضة الأكسجين (نقص التأكسج) التي تقلل من فعالية الإشعاع. تصف هذه الدراسة هيدروجيل «ذكي» يمكن حقنه ويتجمع مباشرة داخل الورم ويعمل كمصنع دوائي صغير ومولد للأكسجين. من خلال تزويد الورم بالإشعاع وإشارات منشطة للمناعة بترتيب زمني مدروس، يهدف النظام إلى تحويل سرطان يصعب علاجه إلى هدف يمكن لدفاعات الجسم التعرف عليه وتدميره.
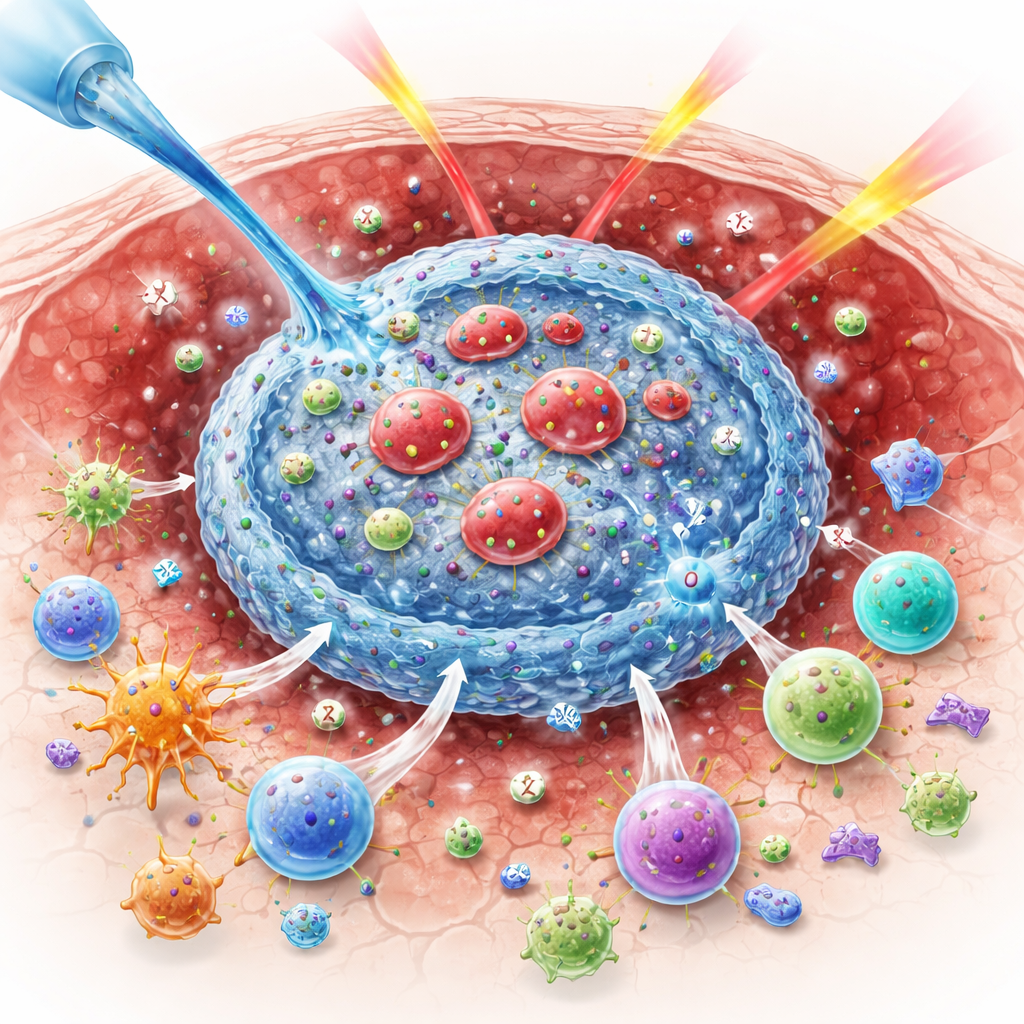
لماذا يهم الأكسجين في محاربة الأورام
يقتل الإشعاع الخلايا السرطانية جزئياً عن طريق توليد جزيئات أكسجين شديدة التفاعل تكسر الحمض النووي. عندما تُحرم الأورام من الأكسجين، يصبح هذا التفاعل الكيميائي أقل فعالية، فتبقى خلايا سرطانية أكثر على قيد الحياة. في الوقت نفسه، يرسل الإشعاع رسائل متضاربة إلى الجهاز المناعي. يمكنه كشف بروتينات الورم التي تصنف السرطان كمصدر خطر، لكنه قد يعزز أيضاً «مكابح» على الخلايا المناعية مثل بروتين نقطة التفتيش CTLA-4، ويُفضّل الخلايا التائية المنظمة التي تكبح الهجوم. تفسر هذه التأثيرات المتضاربة لماذا لم تؤدِ تراكيب الإشعاع مع أدوية مناعية دائماً إلى نتائج متوقعة لدى المرضى كما في تجارب الفئران.
هيدروجيل حي يبنى داخل الورم
صمم الباحثون مادة تتجمع ذاتياً فقط داخل البيئة الحمضية للورم. تتكون من ثلاث مكونات رئيسية: بوليمر طبيعي قائم على السكر يُدعى الألجينات، مسحوق غير عضوي يُدعى بيروكسيد الباريوم، وكريات دم حمراء مُعدّلة بلطف لحمل دوائين مناعيين. عند حقن الخليط داخل الورم، تحفز الظروف الحمضية تحلل بيروكسيد الباريوم مفرِجاً أيونات الباريوم وبيروكسيد الهيدروجين. تربط أيونات الباريوم الألجينات فوراً لتكوّن هيدروجيل ناعم، محصورةً كريات الدم الحمراء الهندسية وتمنع غسل الأدوية. في الوقت نفسه، تُحوِّل إنزيمات موجودة طبيعياً في كريات الدم الحمراء بيروكسيد الهيدروجين إلى أكسجين، مما يساعد على تخفيف نقص التأكسج في الورم وإعداد الورم لتأثير إشعاعي أكثر فعالية.
إطلاق متزامن بإيقاع زمني لإشارتين مناعيتين
تكمن القوة الحقيقية للنظام في كيفية تفريقه لإطلاق عاملين مناعيين: جسم مضاد يعيق CTLA-4 وسيتوكين يُدعى إنترلوكين-12 (IL-12). يُحمَّل الجسم المضاد داخل كريات الدم الحمراء، بينما يُثبَّت IL-12 على سطحها. مع توليد الأكسجين تفتح مسام في غشاء كريات الدم الحمراء، مما يسمح لهروب الجسم المضاد المانع لـCTLA-4 بسرعة. يؤدي هذا الطوفان المبكر إلى رفع القمع المناعي، ويشجع الخلايا التغصنية على نقل مولدات الضد الورمية إلى العقد اللمفاوية المجاورة، ويساعد في تنشيط الخلايا التائية الخاصة بالورم. أما IL-12 فينهَل تدريجياً مع تراخي بنية الهيدروجيل بمرور الوقت. تدفع هذه الإشارة المتأخرة الخلايا التائية والخلايا القاتلة الطبيعية لإنتاج إنترفيرون-غاما، وتعزز مزيداً من تجنيد الخلايا المناعية القاتلة إلى الورم، وتقوي حلقة تغذية راجعة إيجابية بين الخلايا المناعية الحارسة والمنفذة.
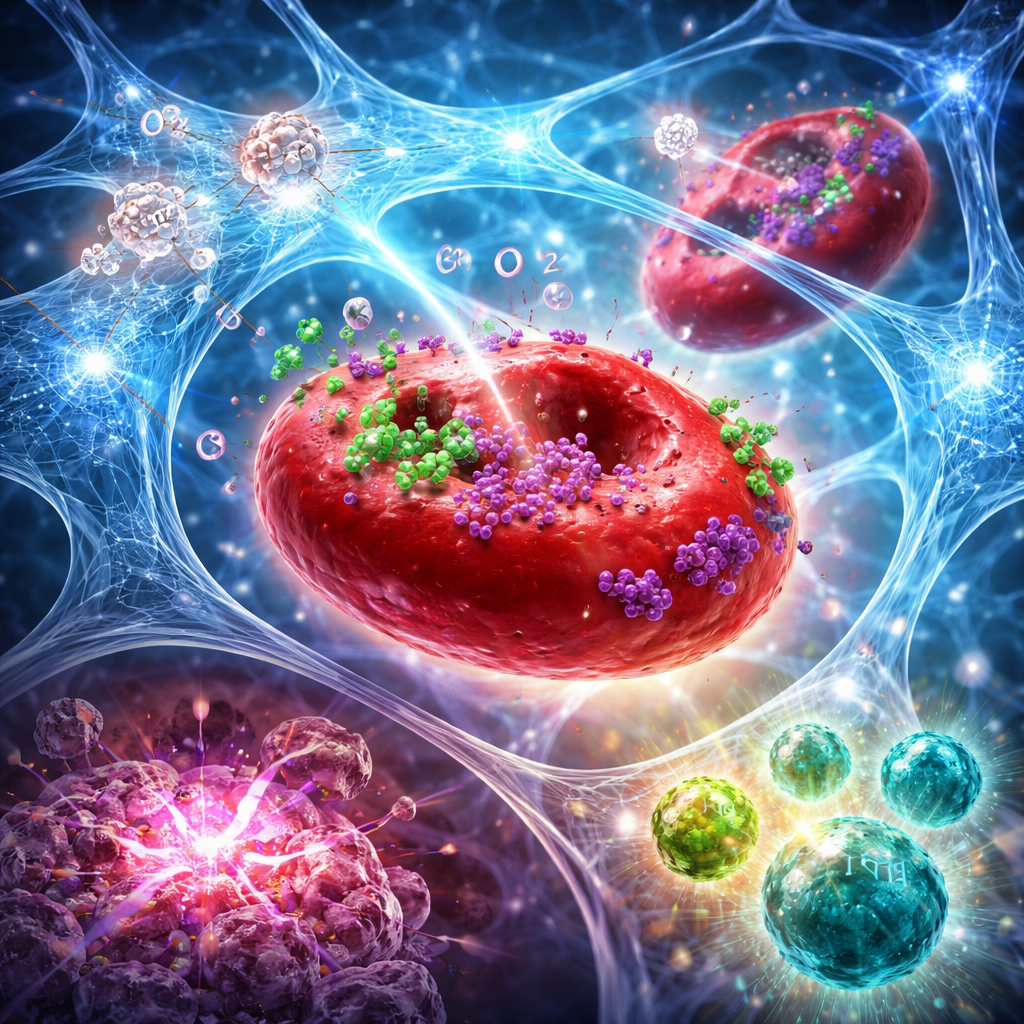
من الحقن الموضعي إلى هجوم مناعي جهازي
في نماذج فئران لأورام ثدي وبنكرياس عدوانية، لم يقتصر تأثير جمع هذا الهيدروجيل مع الإشعاع المركز على تصغير الورم المعالج فحسب. زاد النهج المزدوج من مستويات الأكسجين في الأورام لعدة أيام، وعزز الأضرار التي يُسببها الإشعاع للحمض النووي، وأثار شكلاً أقوى من موت الخلايا الذي يميّز الورم للانتباه المناعي. أظهرت قياسات التدفق وصبغات الأنسجة تحولاً واضحاً في البيئة الدقيقة للورم: مزيد من الخلايا التائية CD8 القاتلة والخلايا القاتلة الطبيعية، وخلايا تنظيمية أقل، ونسبة أعلى للخلايا «المنفذة» مقابل «الكابحة». كما ازداد عدد الخلايا التغصنية المتخصصة في العقد اللمفاوية، مما يدل على تحسين عرض المولدات المضادة. شهدت العديد من الفئران تراجعاً تاماً للأورام، وبعضها أصبح محمياً من إعادة نمو الورم عندما أعيد إدخال خلايا سرطانية أسابيع لاحقة، مما يشير إلى تكوين ذاكرة مناعية دائمة.
السلامة والعملية والاتجاهات المستقبلية
لأن الهلام يتكوّن محلياً ويتمسك بموادِه، يتسرّب كميات صغيرة فقط من IL-12 ومضاد CTLA-4 إلى مجرى الدم، مما يقلل خطر الآثار الجانبية الشديدة مثل عواصف السيتوكين أو تلف الأعضاء التي قيّدت استخدام هذه العوامل سابقاً. مكونات البناء — الألجينات، وكريات الدم الحمراء، وبيروكسيد الباريوم — منخفضة التكلفة نسبياً وقابلة للتوسيع، مما يثير الأمل في إمكانية تكييف هذه الاستراتيجية لأنواع سرطانات مختلفة. وبينما لا تزال هناك تحديات في التصنيع ومراقبة الجودة وتوصيل الهيدروجيل إلى أورام عميقة أو منتشرة على نطاق واسع، تُظهر الدراسة وسيلة واعدة لمزامنة الإشعاع مع تفعيل مناعي مُحدّد زمنياً بدقة، لتحويل علاج فيزيائي للسرطان إلى محفّز قوي لمناعة جهازية مضادة للأورام.
ماذا قد يعني هذا للمرضى
بعبارات بسيطة، تشير هذه الأبحاث إلى أنه بدلاً من إعطاء الإشعاع والأدوية المناعية بشكل منفصل مع الأمل بأن يتعاونا، يمكننا حزمها في مادة ذكية تجلس داخل الورم، تولّد أكسجينها الخاص، وتطلق إشارات مناعية بتسلسل مُنسَّق بعناية. في الحيوانات، لم يجعل هذا النهج الإشعاع أقوى في قتل الخلايا السرطانية فحسب، بل درّب أيضاً الجهاز المناعي على التعرف على الورم وتذكره، مما ساعد في منع عودته. إذا أمكن تحقيق نتائج مماثلة في البشر، فقد يحول هذا النوع من الهيدروجيل يومًا ما الأورام الصعبة إلى أهداف يمكن لدفاعات الجسم العثور عليها وتدميرها بشكل موثوق.
الاستشهاد: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
الكلمات المفتاحية: العلاج الإشعاعي-المناعي, هيدروجيل, المناعة ضد السرطان, البيئة الدقيقة للورم, العلاج الإشعاعي