Clear Sky Science · ar
تنبؤ قوي وقابل للتفسير لمؤشرات الجينات وأنواع الخلايا من بيانات النسخ المكانية
تحويل شريحة النسيج الروتينية إلى خرائط جزيئية
عند أخذ خزعة، يرى الأطباء عادةً فقط ما تكشفه المجهر: أشكال وأنماط الخلايا في صبغات وردية وبنفسجية. ومع ذلك، تحت تلك الألوان يكمن عالم خفي من الجينات التي يتم تشغيلها أو إيقافها، مما يؤثر على كيفية نمو السرطان واستجابته للعلاج. تُقدّم هذه الدراسة نظام STimage، وهو نظام ذكاء اصطناعي جديد يهدف إلى قراءة ذلك النص الجزيئي مباشرةً من صور علم الأمراض القياسية، مما قد يوفر رؤى أسرع وأرخص دون الحاجة لاختبارات مختبرية إضافية.
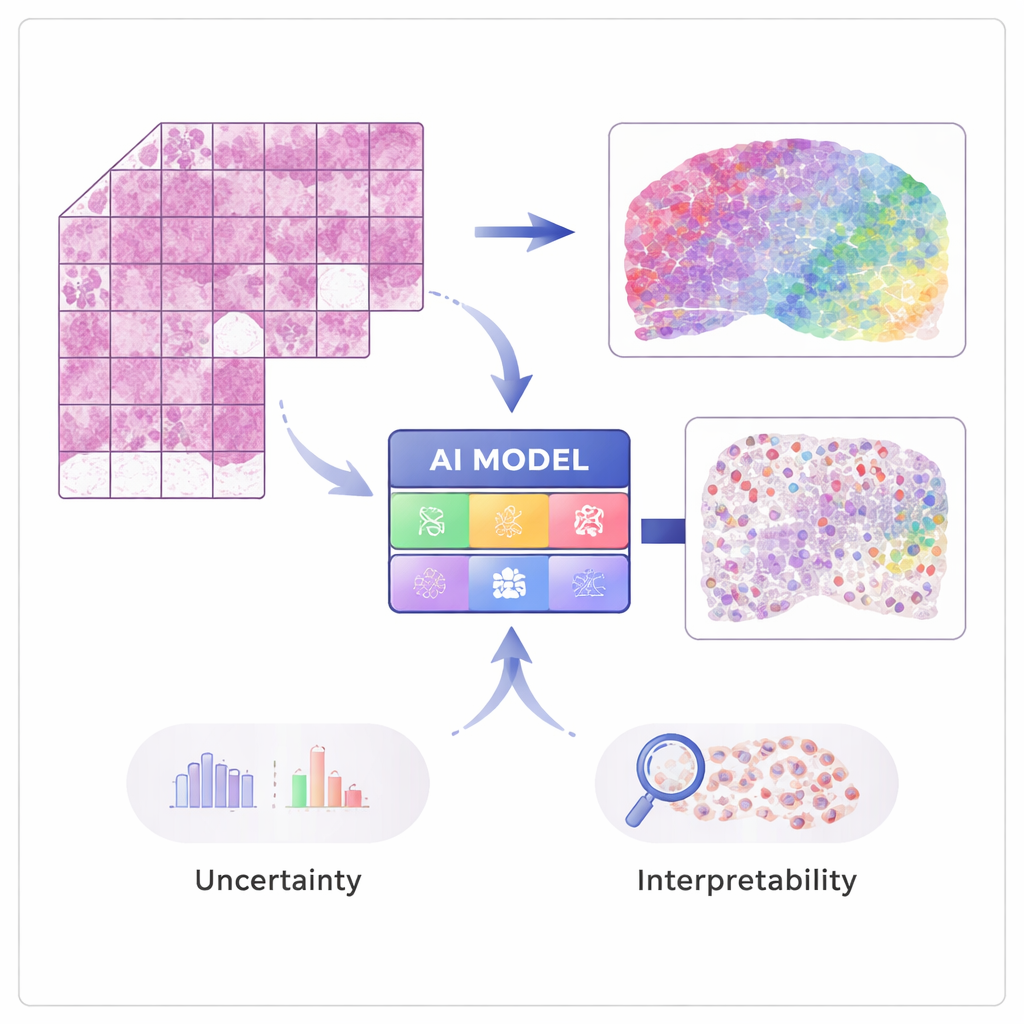
من الصور إلى نشاط الجينات
تستطيع التقنيات الحديثة في «النسخ المكاني» قياس نشاط عشرات الآلاف من الجينات مع الحفاظ على موضع كل إشارة داخل النسيج. هذه الطرق قوية لكنها مكلفة وليست روتينية بعد في المستشفيات. يتم تدريب STimage على عدد محدود من مجموعات البيانات المكانية، حيث تُطابق كل صورة نسيج بقياسات جينية مفصّلة في العديد من النقاط الصغيرة. يتعلم النموذج الربط بين الأنماط البصرية المحلية في شريحة الهيماتوكسيلين والإيوزين (H&E) — مثل مدى كثافة النوى أو عدم انتظامها — ونشاط الجينات الكامن، بحيث يمكنه لاحقًا التنبؤ بتعبير الجينات وأنواع الخلايا من الصور العادية وحدها.
بناء عالم آلي أكثر موثوقية وقابلية للتفسير في علم الأمراض
هدف أساسي في العمل ليس الدقة فحسب، بل الموثوقية وقابلية التفسير. بدلاً من إخراج رقم واحد لكل جين، يتنبأ STimage بتوزيع احتمالي كامل يصف نطاقًا محتملًا لنشاط الجين في كل موقع. كما يفرّق بين نوعين من عدم اليقين: أحدهما ناتج عن بيانات صاخبة أو متغيرة، وآخر يعكس قلة معرفة النموذج نفسه. من خلال تدريب نسخ متعددة متشابهة لكن مختلفة قليلاً من النموذج ومعدّل نتائجها — نهج «التحالف» أو التجميع — يحسّن الباحثون الأداء ويكتسبون فهمًا أوضح للمناطق التي يشعر فيها النظام بالثقة وتلك التي لا يشعر فيها، وهو أمر بالغ الأهمية لاتخاذ القرارات السريرية.
الاختبار عبر أنواع السرطان والتقنيات والمستشفيات
قيّم الفريق STimage على مجموعات بيانات متنوعة من سرطانات الثدي والجلد والكلى، بالإضافة إلى مرض كبدي ذي صلة مناعية. تعلّم النموذج التنبؤ بمؤشرات هامة للسرطان والمناعية، وغالبًا ما طابق الأنماط المكانية الحقيقية التي رُصِدت في تجارب مستقلة. ثبتت متانته عند مواجهته بيانات من مختبرات مختلفة، وطرق إعداد عينات مختلفة، وحتى تقنيات أساسية مختلفة، بما في ذلك منصات ذات دقة خلوية مفردة وأنظمة أقدم ذات دقة أقل. في مقارنات وجهًا لوجه مع عدة أدوات ذكاء اصطناعي موجودة، تفوّق STimage ونسخه التجميعية عادةً، خصوصًا عند تقييم مدى تطابق الأنماط المتوقعة مع التوزيع الحقيقي لنشاط الجينات عبر النسيج.
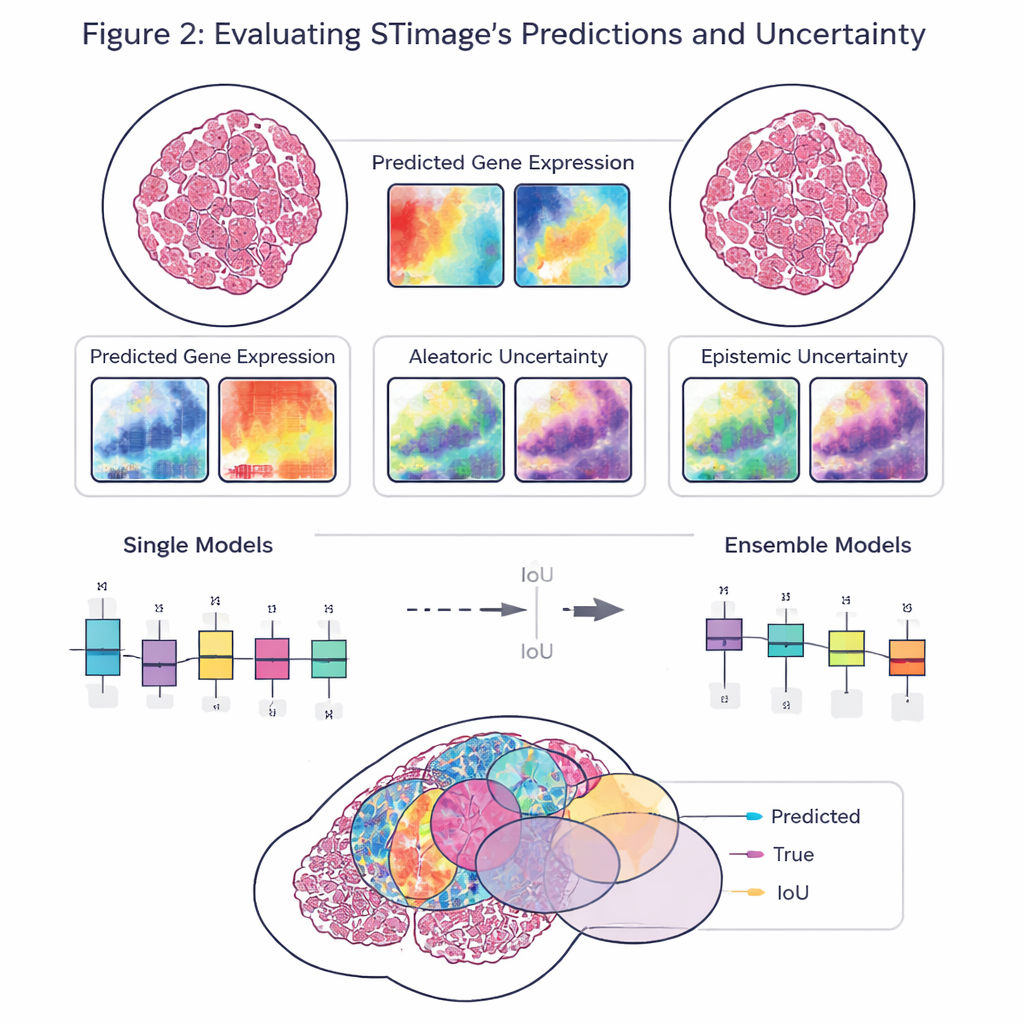
رؤية داخل الأورام: الخلايا والبقاء واستجابة الدواء
يتجاوز STimage التنبؤ بالجينات ليستدل على أنواع الخلايا الموجودة في كل منطقة، باستخدام مجموعات بيانات عالية الدقة حيث تُعرف هوية كل خلية. استطاع النموذج التمييز بين الخلايا السرطانية والخلايا المناعية والخلايا الداعمة ورسم خريطة لترتيبها عبر الشريحة. ثم طوّق الباحثون تطبيق STimage على مجموعات كبيرة من صور السرطان الروتينية من مشروع جينوم السرطان (TCGA). حتى من دون قياسات مكانية، كانت ملفات الجينات المتوقعة بواسطة الذكاء الاصطناعي متوافقة بشكل وثيق مع بيانات الجينومية الإجمالية الحقيقية. كانت هذه التنبؤات قوية بما يكفي لتجميع المرضى إلى فئات ذات مخاطرة أعلى وأدنى، والمساعدة في التمييز بين من هم أكثر احتمالًا لأن يستجيبوا استجابة كاملة لبعض علاجات سرطان الثدي.
لماذا يهم هذا للمرضى في المستقبل
بالنسبة للمرضى والأطباء، يعد وعد STimage نوعًا من «التراكب الجزيئي» على شريحة علم الأمراض المألوفة. بدلًا من طلب اختبارات مكلفة متعددة، قد تكشف صورة ممسوحة واحدة يومًا ما عن الأماكن التي تنشط فيها برامج جينية عدوانية، وكيف تتوزع الخلايا المناعية، وأي المؤشرات تشير إلى نتائج أفضل أو أسوأ أو استجابات دوائية مختلفة. بينما لا يزال الأسلوب في طور التحسين والتوافق مع القياسات الحقيقية ليس مثاليًا، فإن قدرته على التقاط الأنماط المكانية، وتقدير عدم اليقين الخاص به، وإبراز الخلايا التي تُحرّك تنبؤاته يجعلها خطوة عملية نحو علم أمراض رقمي أكثر إفادة وشفافية.
الاستشهاد: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
الكلمات المفتاحية: علم الأمراض الرقمي, النسخ المكاني, مؤشرات حيوية للسرطان, التعلّم العميق, البيئة الدقيقة للورم