Clear Sky Science · ar
التصوير المجهري الإلكتروني بالتبريد يكشف ترابط تكرار الفلافيفيروسات والانشقاق والنضج
كيف تستولي الفيروسات المهاجمة للمخ على أغشية الخلية
الفلافيفيروسات، مجموعة كبيرة من الفيروسات التي تضم مسببات حمى الضنك والتهاب الدماغ الناجم عن القراد، قادرة على غزو المخ والتسبب في أمراض شديدة. ومع ذلك، ظلّت التفاصيل حول كيفية نسخ هذه الممرضات الصغيرة لنفسها وتجميع جسيمات فيروسية جديدة داخل خلايانا إلى حد كبير مخفية. تستخدم هذه الدراسة تقنيات تصوير إلكتروني ثلاثي الأبعاد متقدمة عند درجات حرارة منخفضة للغاية لمراقبة الفلافيفيروسات المنقولة بالقراد أثناء عملها داخل خلايا بشرية ونسيج دماغ فأر، كاشفة ترابطًا غير متوقع بين نسخ الجينوم وتجميع الفيروس ونضجه.
مصانع فيروسية مخبأة في أغشية الخلية
الفلافيفيروسات لا تطفو ببساطة داخل الخلية أثناء تكاثرها. بل تعيد تشكيل نظام أغشية خلوي يُدعى الشبكة الإندوبلازمية لتكوّن جيوبًا متخصصة تُعرف بعضيات التكاثر. تبدو هذه كنتوءات صغيرة إلى الداخل على سطح الشبكة الإندوبلازمية وتعمل كحجرات محمية تُنسخ فيها جينومات الحمض النووي الريبي الفيروسي. باستخدام التصوير المجهري الإلكتروني المقطعي بالتبريد، وهي تقنية تولّد لقطات ثلاثية الأبعاد لخلايا مجمدة بسرعة وفي حالة قريبة من الأصلية، صور الباحثون هذه النتوءات في خلايا رئوية بشرية مُعدية بفلافيفيروس منقول بالقراد مرتبط بفيروس التهاب الدماغ الناجم عن القراد. وجدوا أن الشبكة الإندوبلازمية حول المناطق المصابة تتورّم وتصبح ممتلئة بتجمعات من هذه عضيات التكاثر، بعضها فارغ بينما البعض الآخر مملوء بحمض ريبوني خيطي كثيف.
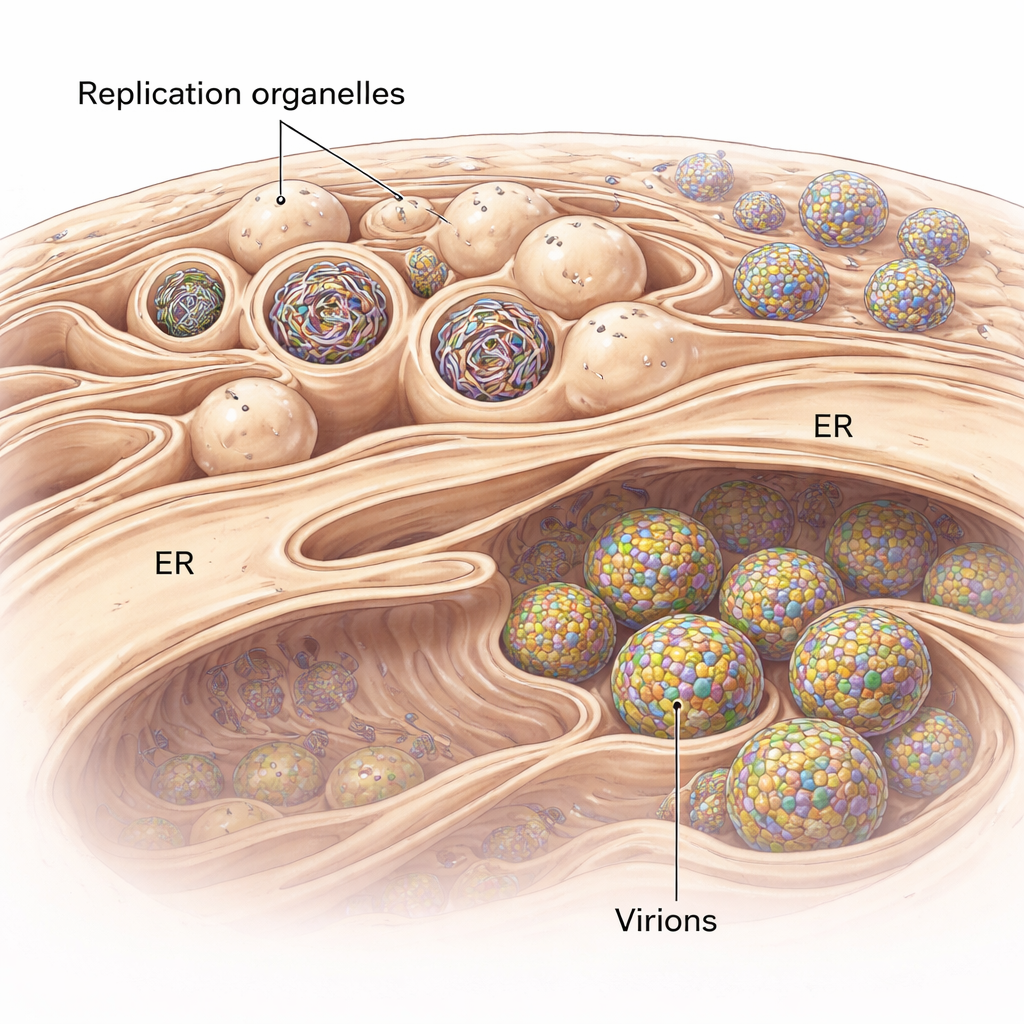
بناء الفقاعة الفيروسية المثالية
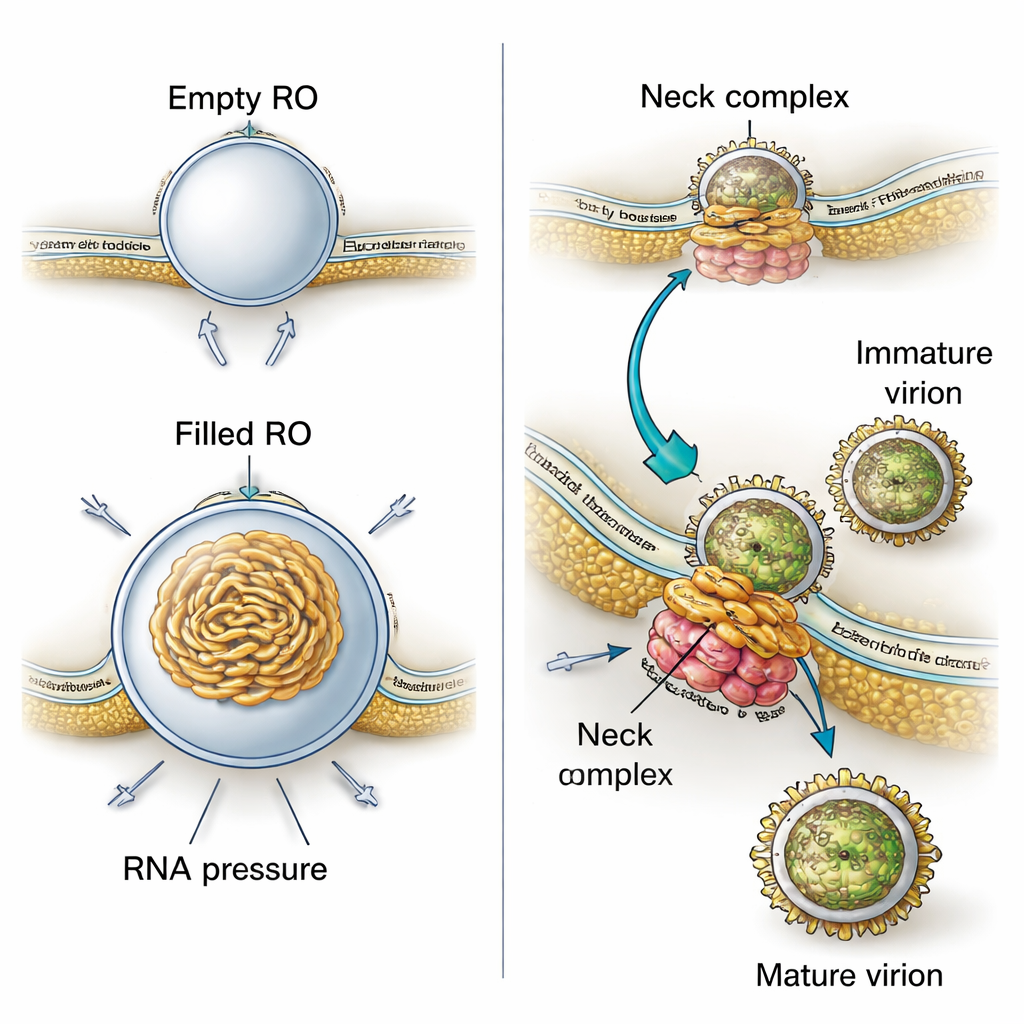
لماذا تتخذ هذه الجيوب الغشائية شكل نتوء دقيق؟ من خلال دمج صورهم ثلاثية الأبعاد مع نمذجة فيزيائية، يُظهر المؤلفون أن قوتين تعملان معًا. أولاً، غشاء عضيات التكاثر يكون باستمرار أكثر سمكًا من الشبكة الإندوبلازمية العادية، ما يشير إلى أن البروتينات الفيروسية أو الدهون المعدلة تجعل الغشاء أكثر صلابة وانحناءً إلى شكل نتوء مستقر حتى قبل دخول أي حمض نووي ريبوي. ثانيًا، عند وجود الحمض النووي الريبي الفيروسي، يلتف داخل الحجرة ويدفع خارجًا، مما يزيد من حجم النتوء. حسابات مبنية على الأحجام المقيسة تشير إلى أن كل عضية ممتلئة تحتوي على ضغط يعادل تقريبًا نسخة واحدة من الجينوم الفيروسي بصيغته مزدوجة الشريط. هذا يعني أن الفيروس يستخدم غشاءً مُشكّلًا مسبقًا ودفع مادته الوراثية ذاته لبناء وتثبيت مصانعِه الصغيرة.
خط التجميع: من نسخ الجينوم إلى فيروسات جديدة
تكشف الدراسة أيضًا مدى ارتباط إنتاج الفيروس بهذه المواقع التكاثرية. في مشاهدهم ثلاثية الأبعاد، لاحظ الباحثون كثيرًا جسيمات فيروسية جديدة تتكوّن بجوار عضيات التكاثر، تنبثق إلى مساحات شبيهة بالشبكة الإندوبلازمية المجاورة. الجسيمات غير الناضجة كانت ذات سطح شائك، بينما بدت الجسيمات الأكثر نضجًا ناعمة. قياسات المسافات في الصور المقطعية أظهرت أن الجسيمات غير الناضجة تجلس أقرب إلى عضيات التكاثر من الجسيمات الناضجة، مما يوحي بأنه أثناء انتقال الجسيمات لمسافة قصيرة عبر مقصورات غشائية متشابكة، تخضع للتغيرات الهيكلية المطلوبة لتصبح معدية. يُرى تجمّع بروتيني كبير عند «الرقبة» الضيقة حيث يتصل كل نتوء تكاثري بالسيتوبلازم يربط عضية التكاثر بغشاء مجاور يحدث فيه الانقسام. من المحتمل أن يعمل هذا المركب كمِزلاج جزيئي ينسق إنتاج الحمض النووي الريبي مع تغليف ذلك الحمض النووي الريبي في جسيمات فيروسية جديدة.
ضبط النضج بحمض أميني واحد
لاستكشاف كيفية التحكم في نضج الفيروس، قارن الفريق نسختين من فيروس هجيني يختلفان بحمض أميني واحد فقط في موقع تتعرف عليه إنزيمات المضيف المسمى فورين. هذا الإنزيم يقطع بروتينًا سطحيًا في الفيروس، ما يساعد على تحويل الجسيمات الشائكة غير الناضجة إلى أخرى ناعمة ناضجة. في تجارب القص في المختبر وفي خلايا مصابة، قُطع المتغير الذي يحتوي على أرجينين في هذا الموقع بسرعة أكبر من المتغير الذي يحتوي على غلوتامين. عند تصويرهما في الخلايا باستخدام التصوير المجهري الإلكتروني المقطعي بالتبريد، أنتج الفيروس الأسرع في القطع نسبة أعلى من الجسيمات الناضجة بالقرب من عضيات التكاثر. بالرغم من هذه الاختلافات المجهرية، أظهرت النسختان نموًا وأنماط مرضية متشابهة في نموذج فأري، ما يوحي بأن الفيروس يمكنه تحمل نطاق من كفاءات النضج مع بقائه معديًا.
مراقبة العدوى مباشرة في المخ
تعتمد معظم الدراسات الهيكلية للفيروسات على خطوط خلوية، لكن هذا العمل يمتد إلى الأنسجة الحية. عزل الباحثون تركيبًا دماغيًا يُدعى الضفيرة المشيمية من فئران مصابة وأعدّوها للتصوير المجهري الإلكتروني المقطعي بالتبريد باستخدام التجمد عالي الضغط وتشكيل الحزم الأيونية الموجهة. حتى في هذا البيئة المعقدة، لوحظت نفس السمات المميزة: تجمعات من عضيات التكاثر، أغشية سميكة، وحويصلات مجاورة ممتلئة بجسيمات فيروسية ناضجة. هذا يبرهن أن إعادة تشكيل الأغشية وتسلسل التكاثر–التجميع–النضج المترابط الذي رُصد في الخلايا المزروعة يعمل أيضًا في المخ، حيث تُسبب هذه الفيروسات المرض.
لماذا تهم هذه العمليات المخفية
لغير المتخصصين، الرسالة الأساسية هي أن هذه الفيروسات المهاجمة للمخ تشغّل خط تجميع منظم للغاية داخل خلايانا. تشكّل أغشية الخلايا فقاعات صغيرة مضغوطة تُنسخ فيها الجينومات، تربط تلك الفقاعات مباشرة بمواقع تنشأ فيها الجسيمات الجديدة، وتبدأ حتى خطوات النضج النهائية على مقربة من موقع التكاثر الأصلي. إن تحديد الأغشية التكاثرية السميكة، والمركب البروتيني العابر للرقبة، والمقصورات النضج المتشابكة عن كثب لا يفسر فقط كيف يتكاثر الفلافيفيروس بكفاءة، بل يشير أيضًا إلى أهداف جديدة للأدوية المضادة للفيروسات المصممة لتعطيل مصانع الفيروس ومسارات تجميعه المخفية.
الاستشهاد: Dahmane, S., Schexnaydre, E., Zhang, J. et al. Cryo-electron tomography reveals coupled flavivirus replication, budding and maturation. Nat Commun 17, 828 (2026). https://doi.org/10.1038/s41467-026-68483-4
الكلمات المفتاحية: الفلافيفيروس, التصوير المجهري الإلكتروني بالتبريد المجهري المقطعي, عضيات التكاثر, نضج الفيروس, التهاب الدماغ الناجم عن القراد