Clear Sky Science · ar
رؤية طيفية-كهروكيميائية لمحفزات النحاس-الكوفر لخفض CO2 والنترات إلى يوريا بالتناظر الكهربائي
تحويل غازات النفايات إلى سماد
السماد اليوريا هو أساس الزراعة الحديثة، لكن إنتاجه التقليدي يستهلك طاقة كبيرة وينطوي على كثافة انبعاثات كربونية عالية. تستكشف هذه الدراسة نهجًا مختلفًا تمامًا: استخدام الكهرباء لتحويل ثاني أكسيد الكربون (CO2) والنفايات المحتوية على النيتروجين (مثل النتريت من عوادم أو مياه الصرف) مباشرةً إلى يوريا. وللقارئ العام، تبدو الفكرة جذابة بوضوح: طريق نحو سماد أساسي يمكن أن يقلل الانبعاثات، ويستغل تيارات نفايات كمغذيات، وقد يعتمد في المستقبل على كهرباء متجددة.
لماذا إعادة التفكير في طريقة صنع اليوريا؟
اليوريا اليوم تُنتج في الغالب عبر خطوة أولى لإنتاج الأمونيا من النيتروجين والهيدروجين المشتق من الوقود الأحفوري (عملية هابر–بوش)، ثم تفاعل الأمونيا مع CO2 عند درجات حرارة وضغوط مرتفعة. هذه السلسلة من التفاعلات مركزية، مكلفة رأسماليًا، وتطلق نحو طن واحد من CO2 لكل طن يوريا مُنتج. مع تزايد الطلب العالمي على الأسمدة، تزداد التكاليف البيئية. البديل هو تخطي الوقود الأحفوري تمامًا عبر دفع الخطوات الكيميائية الرئيسية بالكهرباء، ويفضل أن تكون متولدة من مصادر متجددة، وباستعمال CO2 وأكسيدات النيتروجين (NOx) التي تُعامل اليوم كنفايات.
دور جديد للنحاس والكوفر
صمم الباحثون محرضات رقيقة تُحضّر بطلاءً مشتركًا للنحاس (Cu) والكوفر (Co) على ورق الكربون، مع ضبط نسبة Cu:Co بدقة. ركزوا على الاختزال الكهروكيميائي المتزامن لـ CO2 والنتريت (NO2⁻) في الماء عند درجة حموضة محايدة، وهو ظرف يمكن أن يُسهِم في تكوين روابط الكربون–النيتروجين (C–N) الدقيقة المطلوبة لليوريا. التركيبة المميزة هي خليط بنسبة 1:1 من Cu وCo، الذي يحقق معدل إنتاج يوريا يقارب 61 ميليمول في الساعة لكل غرام من المحفز عند فرق جهد معتدل. تُظهر الميكروسكوبات وقياسات الأشعة السينية أن المعادن مختلطة على مقياس ذري وتبقى في حالة معدنية إلى حد كبير أثناء التشغيل، مقدمة منصة متينة يمكن أن تتفاعل عليها كل من CO2 والنتريت بكفاءة. 
كيف يقسم المحفز العمل ويتقاسمه
إنتاج اليوريا بهذه الطريقة صعب لأن التفاعلات الأبسط — مثل توليد غاز الهيدروجين أو اختزال CO2 أو النتريت منفردة — تتنافس بقوة. المفتاح، كما يجد الباحثون، هو تقسيم الأدوار بين مواقع النحاس والكوفر التي تعمل معًا. تُظهر الاختبارات الكهروكيميائية أن النحاس بمفرده يحول CO2 في الغالب إلى وقود ومواد كيميائية كربونية، بينما الكوفر بمفرده يحول النتريت في الغالب إلى أمونيا، دون يوريا في كلتا الحالتين. فقط عندما تُخلط ذرات Cu وCo عن قرب تبرز كمية معتمدة من اليوريا. تلتقط صور مطيافية «للحظات» أثناء التفاعل شظايا مرتبطة بالسطح: أنواع كربونية مشتقة من CO2 (*CO و*COOH) تميل إلى النحاس، وأنواع نتروجينية مشتقة من النتريت (*NH2 ومجموعات ذات صلة) تميل إلى الكوفر. على الحدود بين Cu وCo، يمكن أن تلتقي هذه الشظايا وتتحد لتشكل العمود الفقري C–N لليوريا.
إيجاد الظروف المناسبة لبناء الروابط
تُظهر الدراسة أن التركيبة وحدها لا تكفي؛ يجب ضبط المحيط المحلول والغشاء أيضًا. تظهر اليوريا فقط في إلكتروليت بيكربونات محايد، الذي يحافظ على ما يكفي من CO2 المذاب ويزود الكمية المناسبة من البروتونات (أيونات الهيدروجين) لدفع خطوات «نقل الإلكترون المشارك مع البروتون» دون أن تغمر السطح بتطور الهيدروجين. في ظروف حمضية أو قلوية قوية، إما لا تتكون اليوريا أو تتحلل سريعًا إلى منتجات أبسط. تكشف تجارب بمصادر نيتروجين مختلفة أن النتريت فعّال بشكل خاص لتكوين اليوريا، متفوقًا على النترات والهيدروكسيلامين. تشير الاختبارات الطويلة إلى أن أفلام Cu–Co مستقرة نسبيًا، مع فقدان معدني طفيف وإنتاج يوريا مستمر.
نظرة تحت الغطاء باستخدام النظرية
لفهم سبب فاعلية هذا المحفز المتتابع، لجأ الفريق إلى محاكاة كمومية تعتمد على نظرية الدوال الكثافة. تدعم هذه الحسابات الفكرة القائلة بأن النحاس يفضل ارتباط الأنواع المشتقة من CO2، بينما يفعّل الكوفر النتريت ويثبت الشظايا التي تحتوي على نيتروجين بشكل أفضل. تشير المحاكاة إلى خطوة معينة كعنق زجاجة طاقي: اقتران شظية *NH2 (من النتريت) مع شظية *COOH (من CO2) لتشكيل وسيط يُكتب أحيانًا كـ *NH2CO. بمجرد تكوّن هذا الجزء، تصبح الخطوات المتبقية نحو اليوريا أسهل نسبيًا. يقلل واجه Cu–Co من تكلفة الطاقة لهذا الاقتران الحاسم مقارنةً بالنحاس النقي أو الكوفر النقي، ما يفسر الزيادة المرصودة تجريبيًا في عائد اليوريا للنظام الثنائي المعدن. 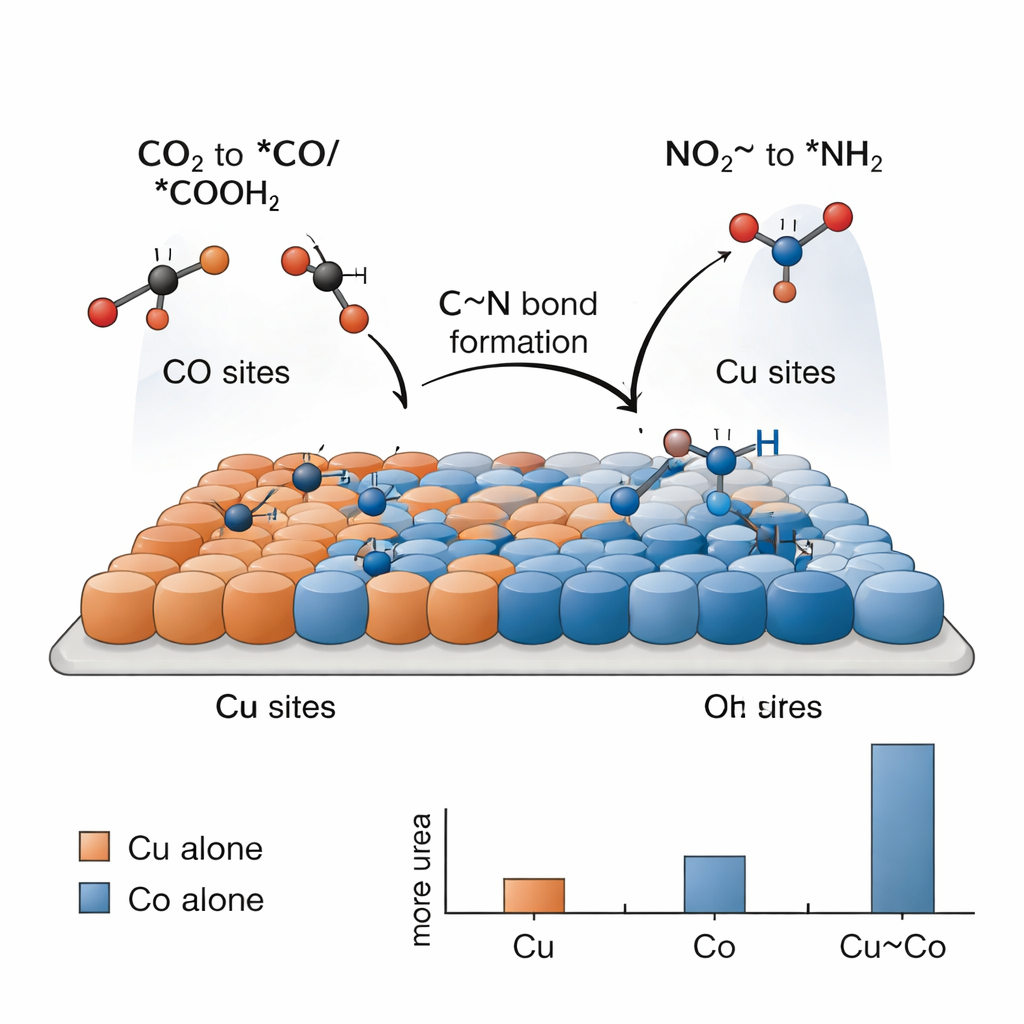
من بصيرة مخبرية إلى سماد أنظف
من الناحية العملية، لا تحل هذه الدراسة مكان مصانع اليوريا العملاقة اليوم، لكنها توضح كيف يمكن تصميم مسار كهروكيميائي مستقبلي. من خلال إظهار أن النحاس والكوفر يمكن أن يعملا بالتوازي — أحدهما يزوّد أنواع كربونية منشّطة، والآخر أنواع نتروجينية منشّطة، وكلاهما تحت شروط بروتونية محكومة بعناية — ترسم الدراسة مسارًا واقعيًا نحو إنتاج يوريا أنظف ويمكن توزيعه محليًا ويستخدم CO2 ونفايات النيتروجين كمصادر بدلًا من أن تكون ملوثات.
الاستشهاد: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
الكلمات المفتاحية: تصنيع يوريا بالكهروكيمياء, محفز نحاس-كوفر, استخدام CO2, اختزال النتريت, ربط C–N