Clear Sky Science · ar
الأساس البنيوي للتثبيط الانتقائي لناقل GABA البشري GAT3
لماذا تهم إشارات الدماغ المهدئة
يعتمد دماغنا على توازن دقيق بين الإشارات التي تثير والإشارات التي تهدئ. المرسل المهدئ الرئيسي هو GABA، مادة كيميائية تساعد في منع النشاط المفرط المرتبط بحالات مثل الصرع، وتلف السكتة الدماغية، ومرض ألزهايمر. تركّز هذه الدراسة على بروتين يُدعى GAT3، الذي يزيل GABA من محيط الخلايا العصبية. من خلال الكشف، بتفصيل ذري، عن كيفية ارتباط جزيء جديد بـ GAT3 وإيقافه، يقدّم الباحثون خريطة بنيوية لتصميم أدوية جديدة قد تعزز نظام الكبح الطبيعي في الدماغ بطريقة لطيفة.
دواسة المكابح الطبيعية في الدماغ
GABA هو الناقل العصبي الرئيسي المُثبِّط أو المهدئ في الجهاز العصبي المركزي. بعد إطلاق GABA من النهايات العصبية، يجب إزالته بسرعة حتى تتمكن الدوائر الدماغية من إعادة الضبط. تقوم بروتينات الناقل هذه بعملية التنظيف عبر ضخ GABA مرة أخرى إلى الخلايا. يهيمن ناقلان على الدماغ: GAT1، الموجود بشكل أساسي على الخلايا العصبية، وGAT3، الموجود على الخلايا الداعمة المسماة الخلايا النجمية. بينما استُخدم دواء يثبط GAT1 (تياغابين) لعقود لعلاج الصرع، تأخرت الأدوية المماثلة المستهدفة لـ GAT3. مع ذلك، يكتسب GAT3 أهمية خاصة لأنه يتحكم في مستويات GABA خارج المشابك ويشكّل تثبيطاً طويل الأمد وخلفياً يمكنه ضبط نشاط الدماغ بدقة. 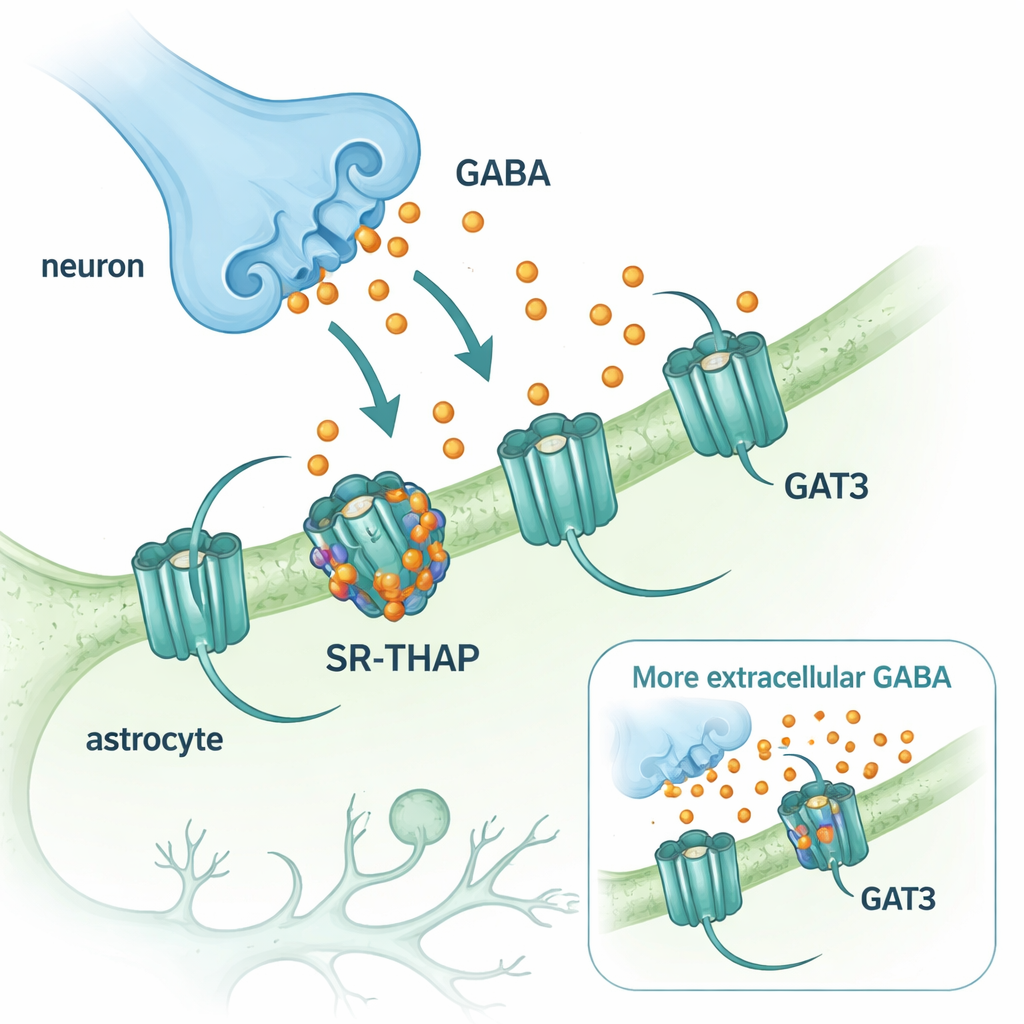
تصميم قفل جزيئي أكثر دقة
عرقلت محاولات تثبيط GAT3 قلة المعلومات البنائية التفصيلية. الكثير من المركبات السابقة طُورت بالتجربة والخطأ، غالبًا عبر صنع متغيرات ضخمة لمواد شبيهة بـ GABA المعروفة. أحد أشهر هذه المركبات، (S)-SNAP-5114، تبين أنه غير مستقر كيميائياً وصعب الاستخدام في الحيوانات الحية. استناداً إلى قريب أكثر متانة من هذا المركب، طور المؤلفون SR-THAP، جزيئاً صغيراً جديداً مصمماً ليتناسب مع GAT3 بشكل أوثق ويقاوم التفكك. أظهرت التجارب في مزروعات خلايا بشرية أن SR-THAP يثبط GAT3 بقوة وبطريقة غير تنافسية: فبدلاً من التنافس ببساطة مع GABA في الموقع المعتاد، يغيّر كيفية عمل الناقل، مخفضاً سعته القصوى للنقل.
رؤية GAT3 بدقة قريبة من الذرية
لفهم بالضبط كيف يعمل SR-THAP، لجأت المجموعة إلى الميكروسكوب الإلكتروني بالتبريد، تقنية تُصوّر البروتينات المجمدة فجأة باستخدام إلكترونات وتعيد بناء شكلها ثلاثي الأبعاد. حلّوا ثلاث نسخ من GAT3 البشري: مرتبط بـ SR-THAP، مرتبط بـ GABA، وفي حالة خالية من الركيزة. تكشف الثلاثة عن البنية النمطية الموجودة في ناقلات النواقل العصبية ذات الصلة: 12 حلزوناً مغزلياً متراصاً يعبر غشاء الخلية ويكوّن ممرّاً مركزياً لـ GABA وأيوناته المرافقة، الصوديوم والكلوريد. في البنية المرتبطة بـ GABA، يوجد الناقل في حالة «مغلق للداخل»—حيث يُثبت GABA وأيون الصوديوم في الوسط، معزولين عن الخارج والداخل. حمض أميني عطري أساسي يشكل تداخلًا متخصصًا مع مجموعة الأمين في GABA، ما يساعد في تفسير كيفية تعرف GAT3 على ركيزه.
كيف يثبت SR-THAP الناقل في وضعية مفتوحة
بالمقارنة اللافتة، تلتقط البنية المرتبطة بـ SR-THAP GAT3 في حالة «مفتوحة إلى الداخل»، مع جانب داخلي من البروتين متسع نحو داخل الخلية. يستقر SR-THAP عميقاً في هذه التجويف الداخلي، محشوراً بين عدة حلزونات تتحرك عادة أثناء دورة النقل. يشغل ثلاث جيوب صغيرة ذات خصائص كيميائية مختلفة، مشاركاً شبكة من روابط الهيدروجين والتماسات الدهنية. هذا التموضع يعيق الناقل بفعالية بحيث لم يعد بإمكان GABA والآيونات إكمال رحلتهم. يوضح المؤلفون أن بعض الأحماض الأمينية المحددة المبطّنة لهذا التجويف تختلف بين GAT3 وأقاربه القريبين؛ تبادل أحد هذه البقايا يغير كل من نشاط النقل وقدرة SR-THAP، مما يساعد على تفسير لماذا يكون المثبط أكثر انتقائية بكثير لـ GAT3 مقارنةً بـ GAT1 أو الناقلات المرتبطة.
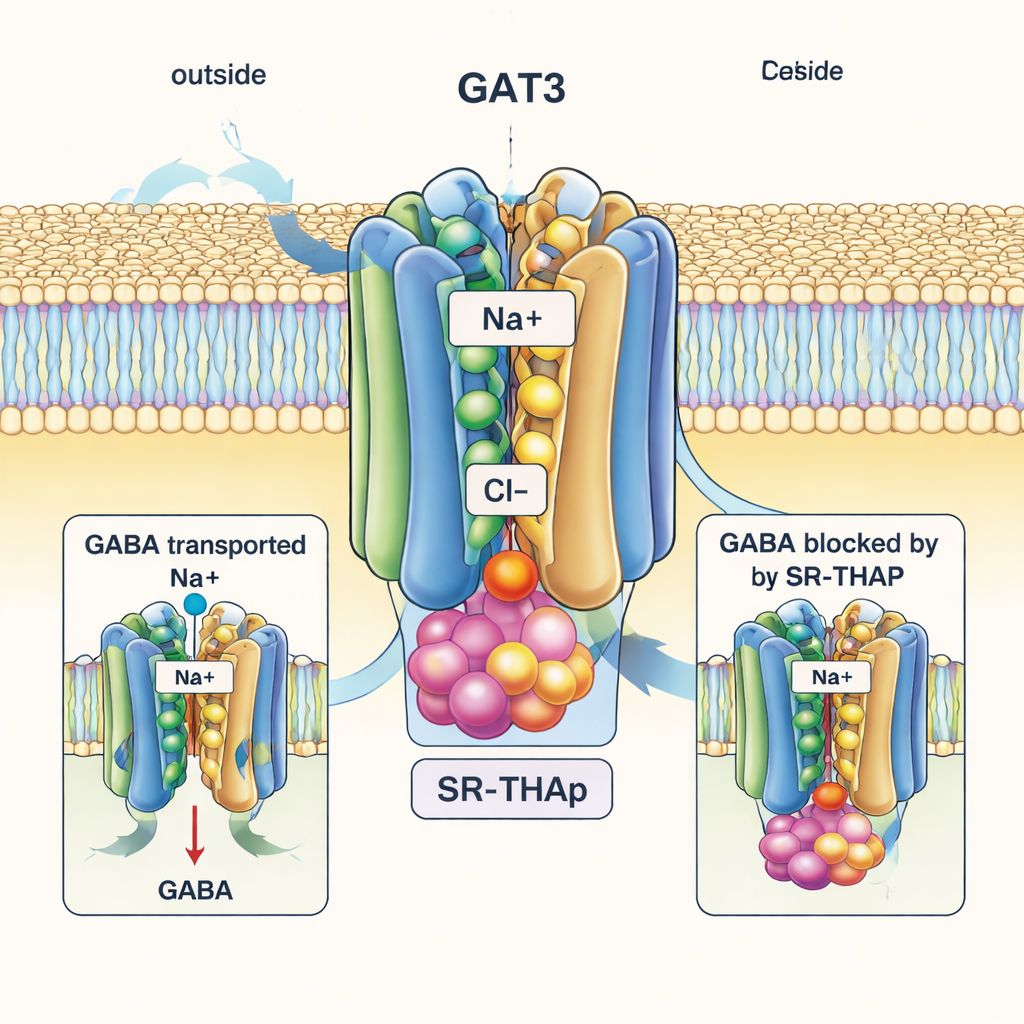
فتح أبواب لأدوية جديدة للصرع وصحة الدماغ
تُظهر هذه الهياكل معاً كيف ينتقل GAT3 بين أشكال مختلفة لنقل GABA، وكيف يستغل SR-THAP جيباً داخلياً أقل حفاظاً لتجميد تلك الدورة. للقراء غير المتخصصين، الخلاصة الرئيسية هي أن الدراسة تقدم مخططًا جزيئيًا مفصلاً لإيقاف GAT3 بطريقة عالية الانتقائية. قد ترفع مثل هذه المركبات مستويات GABA المهدئة بطريقة أكثر دقة من الأدوية الحالية، مما قد يؤدي إلى علاجات أو أدوات بحثية جديدة للصرع، والتعافي من السكتة الدماغية، ومرض ألزهايمر، وحالات أخرى تتعرّض فيها الإشارات المثبطة للاضطراب.
الاستشهاد: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
الكلمات المفتاحية: ناقلة GABA, GAT3, الصرع, التصوير المجهري الإلكتروني بالتبريد, تثبيط الناقل العصبي