Clear Sky Science · ar
بنية فيروس بكتيري Brochothrix thermosphacta تكشف آلية التصاق بجدار الخلية في السيفوفاجات المهاجمة للبكتيريا موجبة الجرام
فيروسات تحافظ على طعامنا طازجًا
الفيروسات القاتلة للبكتيريا، المسماة بالعاثيات (بكتريوفاجات)، تشكل بهدوء صحتنا وإمداداتنا الغذائية. بعضها يسبب إصابات مهدِّدة للحياة، لكن البعض الآخر يمكن تسخيره لمكافحة الجراثيم المسببة للتسمم الغذائي ولفساد الطعام. تكشف هذه الدراسة، بتفصيل ذري ملفت، كيف يلتصق فيروس واحد يُدعى NF5 ويخترق الغلاف الخارجي الصلب لبكتيريا تفسد اللحوم. فهم هذه المعركة المجهرية قد يساعدنا على تصميم طرق أكثر أمانًا لحفظ الطعام ومكافحة البكتيريا المقاومة للمضادات الحيوية.
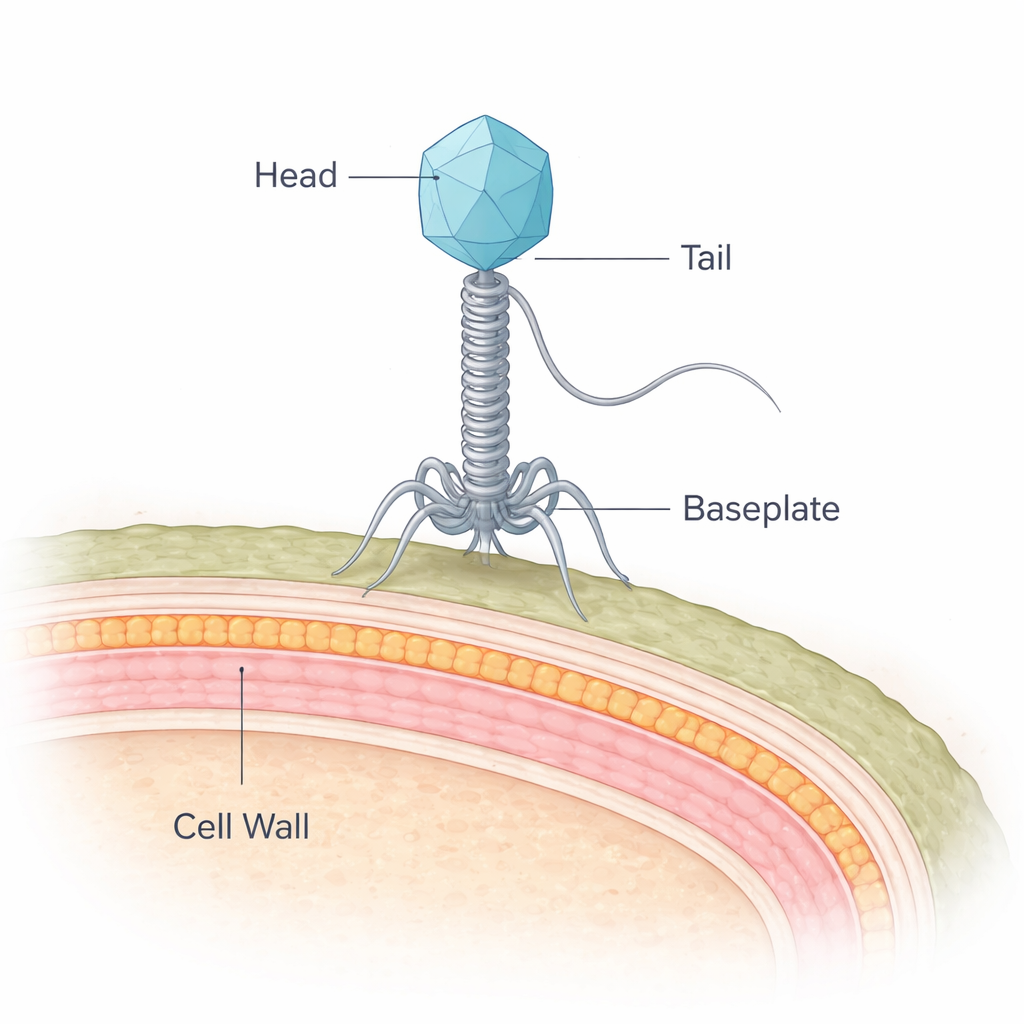
مُفسد للحوم يلتقي عدوه الطبيعي
البكتيريا في قلب هذا العمل، Brochothrix thermosphacta، هي سبب شائع للرائحة الكريهة واللعاب اللزج الذي يتكون على اللحوم المبردة. NF5 هو فيروس يصيب هذه البكتيريا وينتمي إلى مجموعة تُسمى السيفوفاجات، التي تحمل حمضها النووي داخل غلاف بروتيني وتوصِّله عبر ذيل طويل ومرن. بينما وصف العلماء هياكل العديد من الفيروسات التي تصيب ما يُسمى البكتيريا سالبة الجرام بتفصيل، كانت تلك التي تستهدف البكتيريا موجبة الجرام مثل B. thermosphacta أقل فهمًا بكثير. تشكل البكتيريا موجبة الجرام لغزًا خاصًا لأنها محمية بجدار خلوي سميك متعدد الطبقات بدلًا من جدار رقيق وغشاء خارجي.
بناء محقنة جزيئية، ذرة بذرة
باستخدام أحدث تقنيات المجهر الإلكتروني بالتبريد، جَمَّد الباحثون ملايين الجسيمات من NF5 وأعادوا بناء بنيتها ثلاثية الأبعاد بدقة قريبة من الذرية. حدَّدوا 11 بروتينًا فيروسيًا مختلفًا تتجمع معًا لتكوّن الرأس والرقبة وأنبوب الذيل ولوحة القاعدة المعقدة عند طرف الذيل، بمجموع 643 سلسلة بروتينية. يشكّل الرأس غلافًا عشرينيًا متينًا حول الحمض النووي الفيروسي، بينما يمتد ذيل بطول 135 نانومتر إلى الأسفل مثل محقنة مرنة. حلقات من البروتينات المكررة تشكّل أنبوب ذيلي أجوفًا، وسطحه الداخلي مشحون بشحنة سالبة قوية — ترتيب قد يساعد الفيروس على طرد حمضه النووي بسرعة إلى داخل العائل.
الحفار الذكي عند طرف الذيل
أعقد جزء في NF5 هو لوحة القاعدة، بنية متعددة الطبقات تعمل كمستشعر ومثقاب ومرساة في آن واحد. قرب المركز يقع بروتين «مقياس الشريط» الذي يملأ أنبوب الذيل وبروتين ليسين مرتبط بالذيل يسد الأنبوب حتى تبدأ العدوى. تحيط بهذا النواة بروتينات تتعرف على سطح البكتيريا وتمسك به. بعضها يعمل كأذرع نابضة يمكن أن تنثني بشكل دراماتيكي، مما يساعد اللوحة على الميل ثم النقر لتصبح عمودية على جدار الخلية. تشبه أخرى أليافًا موجودة في فيروسات قريبة ويُعتقد أنها ترتبط بجزيئات محددة في الجدار السميك لموجبات الجرام وتُقدِم حتى على نخر أجزاء من شبكة السكريات في الجدار الخلوي. ومن المثير للاهتمام أن أحد بروتينات الألياف الجانبية في NF5 يبدو أنه يجمع وظائف موزعة عبر عدة بروتينات في فيروسات موجبة الجرام الأخرى، مما يشير إلى تصميم فعال ومبسط بفعل التطور.
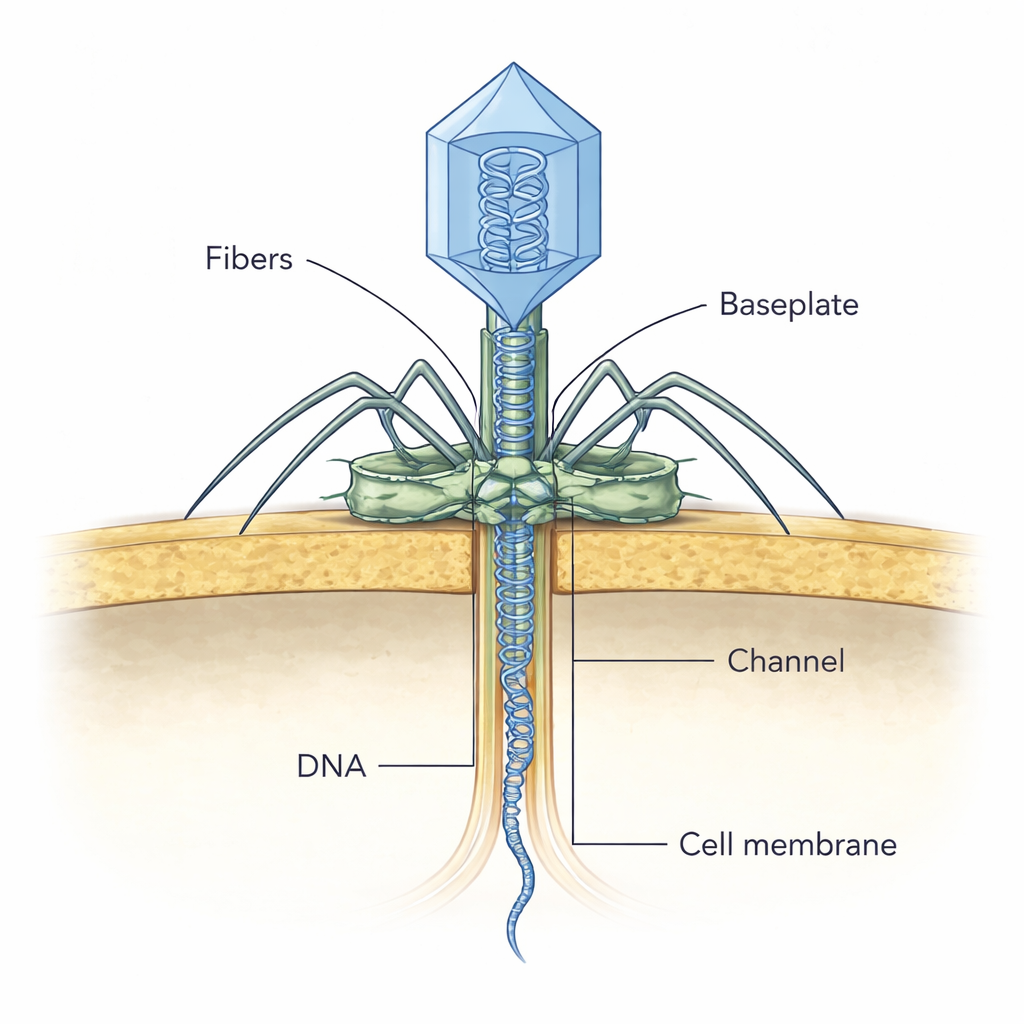
رصد الفيروس أثناء الفعل
لمعرفة كيف تتعاون هذه الأجزاء أثناء العدوى، استخدم الفريق التصوير المقطعي الإلكتروني بالتبريد على شرائح رقيقة من البكتيريا المصابة. التقطوا جسيمات NF5 في مراحل هجوم تبدو مختلفة. في اللقطات المبكرة، يلتصق الفيروس بالجدار الخلوي بزاوية، على الأرجح مستخدمًا أليافه الخارجية للعثور على مستقبلات مناسبة. لاحقًا، تصطف لوحة القاعدة عموديًا على سطح الخلية، ويبدو أن الرأس الملحق ما يزال ممتلئًا بالحمض النووي. في المراحل التالية، يتلاشى محتوى الرأس مع تحرر الحمض النووي، ويظهر كثافة رفيعة تشبه القناة تعبر الجدار البكتيري نحو الغشاء الخلوي. يقترح المؤلفون أنه بمجرد أن يلامس إنزيم طرف الذيل الجدار الخلوي ويهضمه، يعيد تنظيم نفسه، فاتحًا السد ويسمح لبروتين مقياس الشريط بالانزلاق للخارج وتشكيل هذا النفق المؤقت الذي يعبره الحمض النووي الفيروسي بأمان إلى داخل الخلية.
لماذا يهم هذا أبعد من فيروس واحد
من خلال مقارنة NF5 بفيروسات تصيب بكتيريا أخرى، يوضح الباحثون أن بروتينات الذيل ولوحة القاعدة الأساسية تطورت بشكل مختلف في العاثيات المهاجمة لموجبات الجرام مقابل سالبة الجرام للتعامل مع بنى الأسطح المختلفة جدًا لدى مضيفيها. تبدو هذه التعديلات الهيكلية — نطاقات إضافية، أذرع أطول، أو دمج وظائف في بروتينات مفردة — تكيفات مُتقنة للجدران السميكة والأكثر تعقيدًا. تقدم هذه الدراسة مخططًا تفصيليًا لكيفية تعرف الفيروس وربطه وخترق حاجزًا بكتيريًا قويًا، مما يوفر أساسًا لتصميم عاثيات أو أدوات مستوحاة من العاثيات لمكافحة فساد الطعام وربما مكافحة مسببات الأمراض موجبة الجرام الضارة.
الاستشهاد: Peng, Y., Pang, H., Zheng, J. et al. Structure of a Brochothrix thermosphacta bacteriophage reveals cell wall adsorption mechanism in Gram-positive infecting siphophages. Nat Commun 17, 1772 (2026). https://doi.org/10.1038/s41467-026-68477-2
الكلمات المفتاحية: بنية الفيروس البكتيري, البكتيريا موجبة الجرام, المجهر الإلكتروني بالتبريد, السيطرة على فساد الطعام, آلية عدوى الفاج