Clear Sky Science · ar
اضطراب هجرة وخلايا جذعية مقسمة في مرض الضمور العضلي الدوشيني يكشفه التصوير الحي
لماذا تهمنا هذه القصة العضلية
الضمور العضلي الدوشيني (DMD) هو مرض مميت يصيب الأطفال ويدمّر العضلات تدريجيًا. لعقود، ركزت معظم الأبحاث على الألياف العضلية الكبيرة التي تتحلل في DMD. تُظهر هذه الدراسة أن هناك لاعبًا ثانويًا أقل ضجيجًا لكنه متضرر أيضًا: خلايا العضلات الجذعية نفسها التي عادةً ما تصلح الضرر. من خلال مراقبة هذه الخلايا حيّة داخل عضلات الفئران وعلى ألياف فردية، يكشف الباحثون كيف تضيع خلايا الجذعية في DMD، مما يطرح أفكارًا علاجية جديدة قد تساعد العضلات على التجدد بشكل أكثر فعالية.
فريق الإصلاح المدمج في العضلات
كل ليف عضلي هيكلي محاط بعدد قليل من الخلايا الجذعية المقيمة، المعروفة بخلايا ساتلايت العضلة. في العضلات السليمة، تبقى هذه الخلايا في حالة سكون معظم الوقت. عند حدوث إصابة، تصحو هذه الخلايا، وتنقسم، وتنتج إما خلايا جذعية جديدة لإعادة ملء المخزون أو خلايا متخصصة تندمج في الألياف المتضررة. هذا التوازن الدقيق بين التجدد والتمايز يحافظ على قوة النسيج العضلي مدى الحياة. في DMD، ومع ذلك، تتمزق الألياف العضلية مرارًا لأنها تفتقر إلى الديستروفين، وهو بروتين بنائي أساسي، مما يثير السؤال عما إذا كان فريق الإصلاح نفسه يستنفد أو ينحرف عن المسار الصحيح.
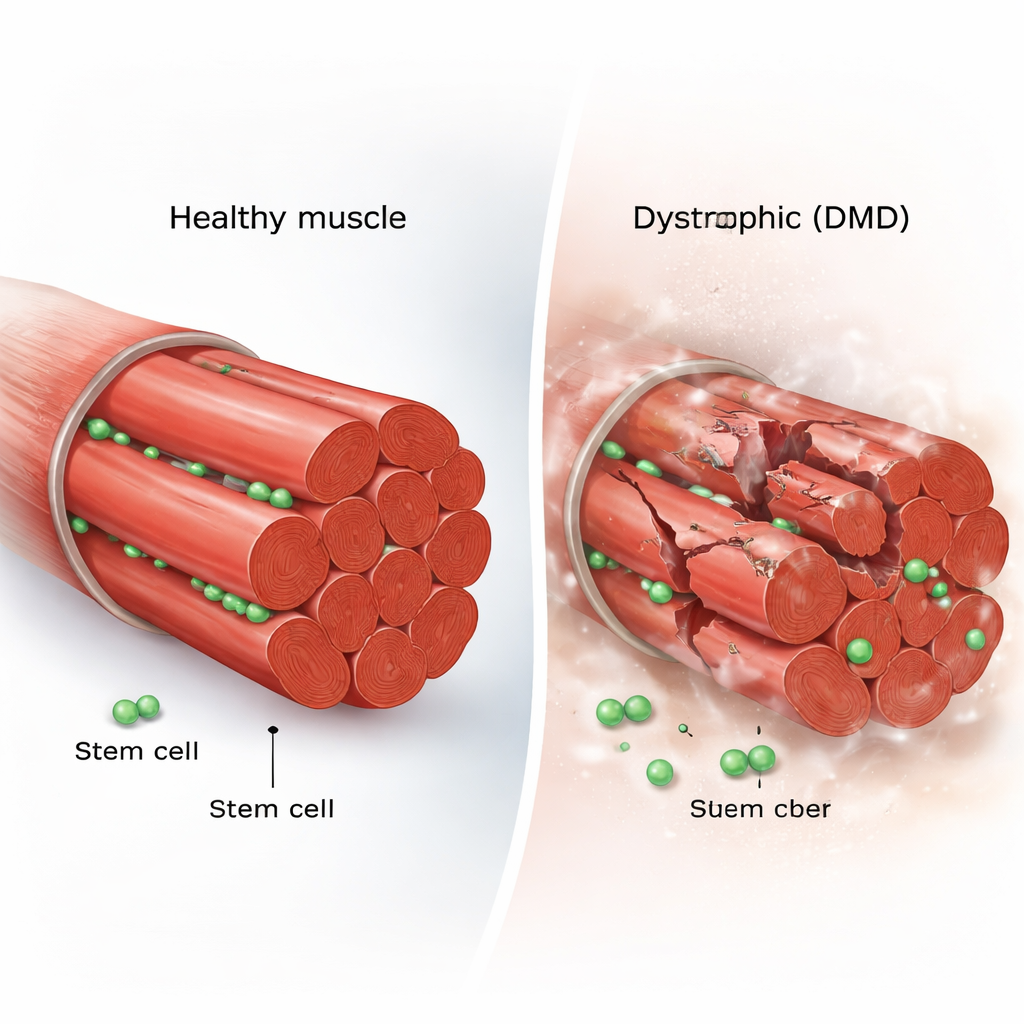
تصوير الخلايا الجذعية أثناء العمل
للإجابة عن ذلك، استخدم الباحثون فأر mdx، النموذج القياسي لـDMD، وهندسوا خلايا الجذعية العضلية فيه لتتوهج تحت المجهر. ثم أجروا تصويرًا حيًا داخليًا (intravital imaging)، وهي تقنية تُمكّن العلماء من تصوير الخلايا الحية داخل حيوان مخدَّر لساعات عديدة. كما طوروا نظامًا مخصّصًا من "الآبار الدقيقة" لاحتجاز ألياف عضلية مفردة في مزرعة أثناء تتبّع كل انقسام وحركة للخلايا الجذعية. سمح لهذين النهجين المتوازيين بتعقب خلايا فردية من حالة السكون مرورًا بانقسامات متكررة وهجرات وأخيرًا اندماج في عضلة جديدة، والتقاط سلوك قد يفوته التصوير الثابت.
عندما يتعجل وتتعثر خلايا الإصلاح
داخل العضلات المصابة السليمة، امتدت الخلايا المشتقة من الخلايا الجذعية وتزلقت على طول الألياف بمسارات مستقيمة وموجهة نسبيًا، وانقسمت وانتشرت بكفاءة. بالمقابل، غالبًا ما أصبحت خلايا mdx مستديرة وبطيئة. تحركت ببطء أكبر وباتجاه أقل تحديدًا، وبقيت نسبة ملحوظة منها شبه جامدة. كما وجد الفريق أن خلايا mdx اندمجت في ألياف جديدة في وقت أبكر من الطبيعي، وهربت العديد من الخلايا الوليدة معًا بدل أن تنفصل بعد الانقسام. بشكل عام، أظهرت العضلات mdx علامات "تمايز سابق لأوانه": تسارعت الخلايا الجذعية نحو أن تصبح خلايا عضلية وتشكل أليافًا، بدلًا من الحفاظ على مخزون قوي للإصلاح المستمر.
انقسامات خلوية غير متوازنة وبيئة قشارة مشوشة
على الألياف المعزولة، تمكن الباحثون من تصنيف طريقة انقسام كل خلية جذعية. في العضلات السليمة، كانت معظم الانقسامات متماثلة لكنها متوازنة — كثير منها أنتج ابنتين قابلتين للتكاثر يمكنهما توسيع مخزون الإصلاح، وعدد أقل أنتج خليتين متميزتين نهائيًا. كانت الانقسامات غير المتماثلة، حيث تبقى إحدى الابنتين خلية جذعية وتلتزم الأخرى بالإصلاح، نادرة نسبيًا لكن موجودة. في عضلات mdx، تحوّل النمط بشكل كبير: انحرفت الانقسامات المتماثلة نحو إنتاج خليتين متميزتين، مع عدد أقل بكثير من الانقسامات التي تولّد خليتين متجدِّدتين. أظهرت تجارب الزراعة المتبادلة، حيث وُضعت خلايا جذعية سليمة على ألياف مرضية والعكس، أن عيوب الهجرة تُحدَّد بدرجة كبيرة ببيئة الليف التالفة، بينما سلوك التمايز المفرط لخلايا mdx يتبع الخلايا نفسها، متشكلًا جزئيًا بفعل تاريخها الالتهابي.
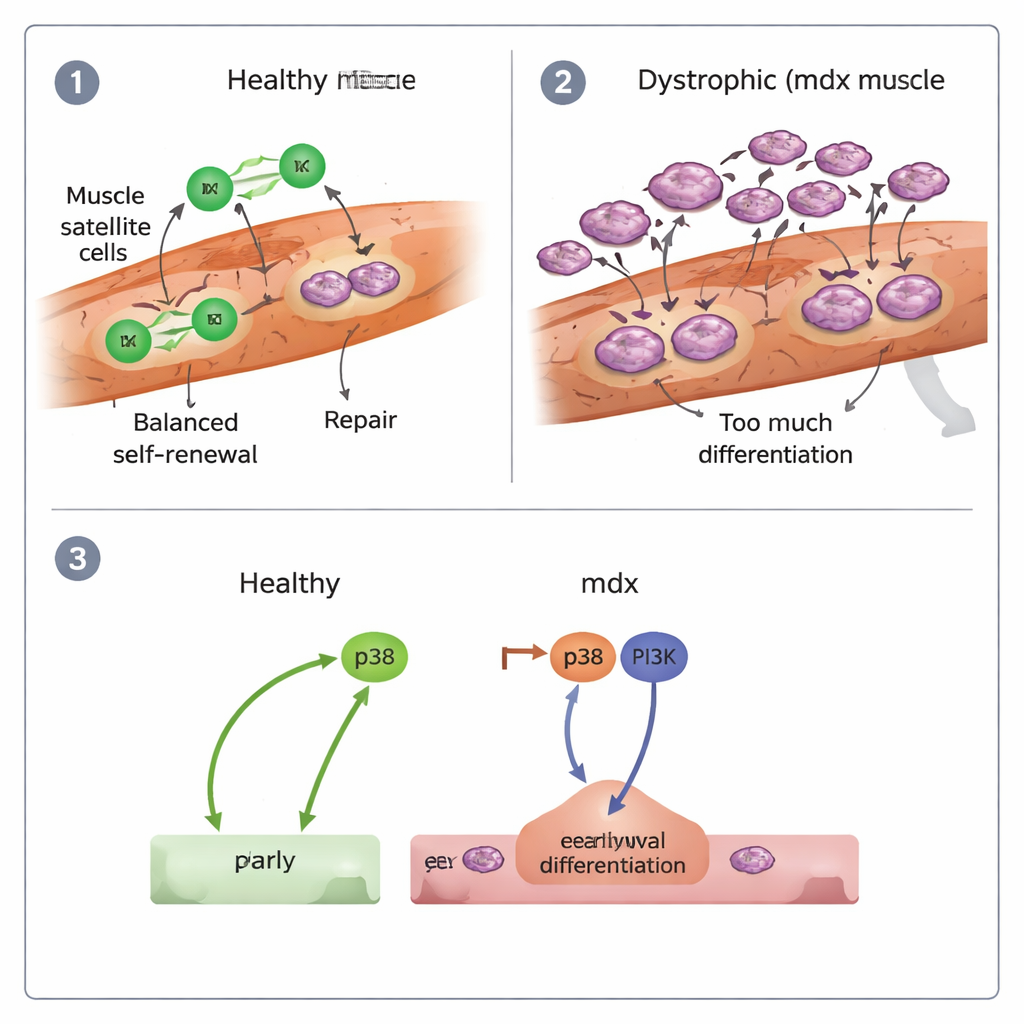
إشارات مشوشة وماذا يعني ذلك للعلاج
تفحص المؤلفون أيضًا المفاتيح الجزيئية التي تدفع الخلايا الجذعية نحو التمايز. ركزوا على مسارين إشاريين معروفين، هما p38 وPI3K. في الخلايا السليمة، أدى حجب p38 إلى تقليل التمايز بشدة، بينما كان تثبيط PI3K ذا تأثير ضئيل. في خلايا mdx، مع ذلك، كان لابد من حجب كلا المسارين معًا لكبح الاندفاع المفرط نحو التخصص، وحتى عندها بقيت قدرتها على التكاثر ضعيفة. هذا يشير إلى أن خلايا الجذعية في DMD تُدفع نحو "الاحتراق المبكر" بواسطة نشاط p38 وPI3K المشترك، مما يسهِم في تجدد يبدأ بسرعة لكنه لا يمكن استمراره.
رؤية جديدة للدوشين: مرض للخلايا الجذعية أيضًا
بالنسبة للقارئ العادي، الرسالة الأساسية هي أن DMD ليس مجرد مشكلة ألياف عضلية هشة؛ إنه أيضًا مشكلة في نظام الإصلاح المخصص لإصلاحها. في العضلات المصابة بالضمور، تتحرك الخلايا الجذعية بكفاءة أقل، وتنقسم بشكل يستنزف الاحتياطي، وتستجيب بصورة غير طبيعية لإشارات النمو الرئيسية. من خلال تحديد أي الجوانب ناجمة عن بيئة العضلة التالفة وأيها متأصل في حالة الخلايا الجذعية المعدلة، تقترح هذه الدراسة استراتيجيات جديدة: علاجات تخفف إشارات p38 وPI3K، تستعيد توازن الانقسامات الخلوية، أو تحسّن الموئل المحلي قد تساعد على إعادة بناء العضلات بشكل أكثر فعالية وتطيل فوائد العلاجات الجينية أو المعتمدة على الخلايا للأشخاص المصابين بالضمور العضلي الدوشيني.
الاستشهاد: Sarde, L., Letort, G., Varet, H. et al. Impaired stem cell migration and divisions in Duchenne muscular dystrophy revealed by live imaging. Nat Commun 17, 1769 (2026). https://doi.org/10.1038/s41467-026-68474-5
الكلمات المفتاحية: الضمور العضلي الدوشيني, خلايا جذعية عضلية, هجرة الخلايا, انقسام الخلايا الجذعية, الطب التجديدي