Clear Sky Science · ar
أنظمة تحرير القواعد المقسمة المُدارة بتغاير اللُفائف الحلزونية تتيح تبديلات نوكليوتيدية مرنة وقوية
إصلاح الحمض النووي بآثار جانبية أقل
تنتج العديد من الأمراض عن أخطاء صغيرة في حمضنا النووي—أخطاء حرفية مفردة قد يكون لها عواقب مهددة للحياة. لدى العلماء أدوات قوية، تُدعى معدِّلات القواعد، يمكنها تصحيح هذه الأخطاء دون قطع الحمض النووي، لكن هذه الأدوات كبيرة وصعبة الإيصال بأمان داخل الجسم. تقدم هذه الورقة طريقة جديدة لتقسيم معدِّلات القواعد إلى أجزاء أصغر وأذكى تظل تعمل بنفس جودة النسخة الأصلية—أو حتى أفضل—مما يفتح مسارات جديدة لعلاج الأمراض الوراثية في الكبد والعضلات وما وراءها.
لماذا الحجم مشكلة لأدوات تصحيح الجينات
تجمع معدِّلات القواعد بين أجزاء من نظام كريسبر وإنزيمات يمكنها استبدال حرف من الحمض النووي بآخر، مثل تحويل A إلى G أو C إلى T. هذه الاستبدالات الدقيقة واعدة لعلاج حالات مثل ارتفاع الكوليسترول أو ضمور العضلات. ومع ذلك، فإن ناقل التوصيل الرائد للعلاج الجيني، الفيروس المرتبط بالأدينو (AAV)، يمكنه حمل نحو 4.7 آلاف حرف من الحمض النووي فقط، بينما تكون معدِّلات القواعد القياسية أكبر من ذلك. حاولت أعمال سابقة تقسيم هذه المعدِّلات باستخدام "مقصات" بروتينية خاصة تُدعى إنتينات، أو بتقليصها عبر إنزيمات مُصغّرة، لكن هذه الأساليب غالبًا ما خفضت الفعالية، أو أضافت تعقيدًا في التصميم، أو قلّلت المواقع الجينية التي يمكن للأدوات أن تعمل فيها.
استخدام لاصق جزيئي لإعادة بناء المعدِّل
لحل هذه المشكلة، صمّم الباحثون معدِّل قواعد "مقسّم" يُمسك معًا بواسطة لُفائف بروتينية صغيرة تُعرف بتغايرات اللُفائف الحلزونية—مثل قطعة من لاصق الفِيلكرو الجزيئي. قسموا معدِّل القواعد إلى جزأين: أحدهما يحمل كاس9 نيكيز المستهدف للحمض النووي والآخر يحمل إنزيم التحرير. تسعى ببتيدات لُفائف حلزونية قصيرة على كل نصف إلى بعضها وتلتصق عندما يصل النصفان إلى نفس موضع الحمض النووي. هذا يخلق معدِّلات قواعد لُفائف حلزونية (CC‑BEs)، بما في ذلك أنواع تعدِّل C (CC‑CBE)، وA (CC‑ABE)، ونُسخًا معقدة يمكنها إجراء تغييرات حرفية مختلفة. 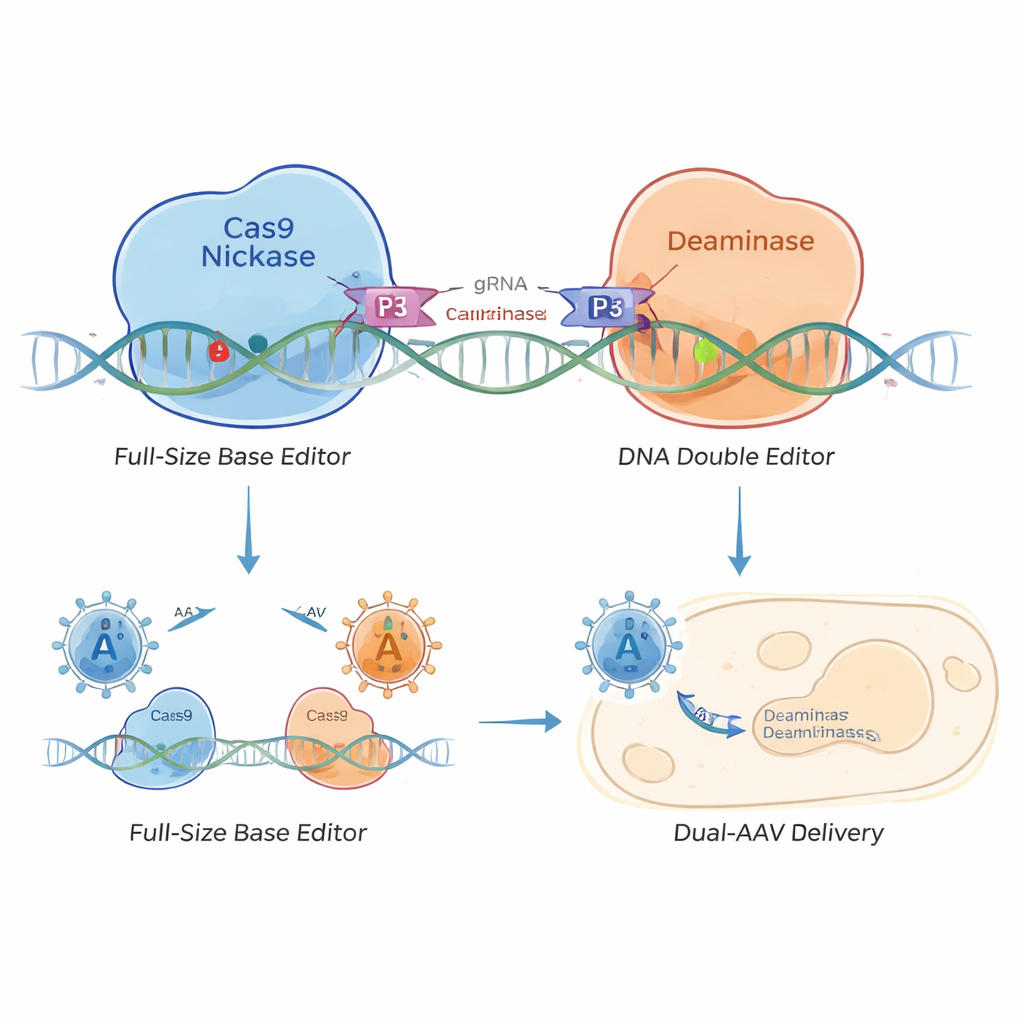
تحرير مرن، قوي ودقيق
اختبر الفريق CC‑BEs في عدة أنواع من الخلايا، بما في ذلك خلايا بشرية وخلايا خنزير أولية، ومع أشكال مختلفة من كاس9 التي تتعرف على نطاق أوسع من تسلسلات الحمض النووي. لم تعمل نسخ CC‑CBE بشكل موثوق عند العديد من المواقع فحسب، بل أظهرت أيضًا "نافذة تحرير" أوسع، بمعنى أنها يمكن أن تُغيّر الحروف المستهدفة عبر امتداد أكبر من الحمض النووي، مما يمنح العلماء مرونة أكبر في اختيار أدلة RNA. وصلت نسخ CC‑ABE إلى كفاءة مشابهة لأفضل معدِّلات الأدينين الموجودة وغالبًا ما أنتجت نواتج جانبية أقل. كما تكيف الباحثون مع استراتيجية اللُفائف الحلزونية لتصاميم معدِّلات أحدث—مثل TadCBE المدمجة والـ ABE9 الدقيقة—واكتشفوا أيضًا أن تقسيم الأدوات بأزواج لُفائف حلزونية حافظ على الأداء أو حسّنه.
من أطباق الخلايا إلى الفئران الحية
ومن الأهمية أن المؤلفين أظهروا أن هذه المعدِّلات المقسمة تعمل داخل حيوانات حية باستخدام توصيل مزدوج بواسطة AAV، حيث يحمل كل جسيم فيروسي نصف المعدِّل. في الفئران، حقق CC‑ABE مستهدفًا جين Pcsk9 في الكبد معدلات تحويل A إلى G تصل حتى نحو 70%، خافضًا بروتين Pcsk9 والكوليسترول الضار LDL في الدم بشكل حاد دون علامات تلف كبدي. 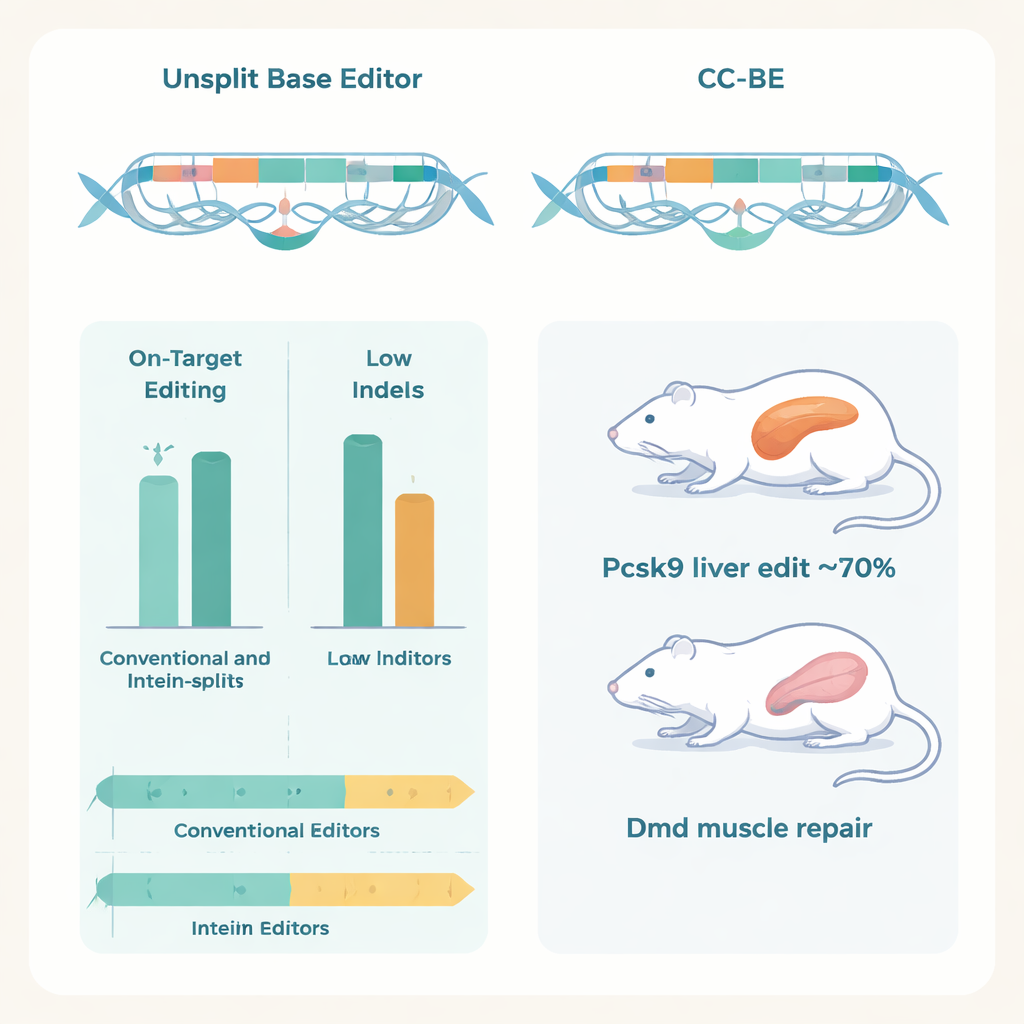
مسار جديد نحو إصلاح الحمض النووي العملي
باختصار، تقدم هذه الدراسة حيلة هندسية بسيطة لكنها قوية: استخدم خطاطيف لُفائف حلزونية صغيرة لتقسيم معدِّلات القواعد الكبيرة إلى وحدات بحجم يمكن لحزم AAV استيعابها تعود للالتقاء فقط عند الحاجة. للمختصين بغير المجال، الخلاصة هي أن العلماء يستطيعون الآن تعبئة أدوات إصلاح الحمض النووي عالية القدرة داخل ناقلات فيروسية مثبتة سريريًا دون التضحية بالدقة أو القوة. قد يجعل نهج اللُفائف الحلزونية هذا من الأسهل تصميم علاجات لمدى واسع من الأمراض الوراثية ذات الحرف المفرد في أعضاء مثل الكبد والقلب والعضلات، مقرّبًا تصحيح الجينات الدقيق خطوة أقرب إلى التطبيقات الواقعية.
الاستشهاد: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
الكلمات المفتاحية: تحرير القواعد, العلاج الجيني, كريسبر, توصيل AAV, المرض الوراثي