Clear Sky Science · ar
التحيُّز المعتمد على H3K27me3 والتنظيم النسخي في الأجنّة المبكرة للفأر يتطلب تقييد نشاط PRC2 بوساطة EZHIP
لماذا تحتاج الأجنّة الصغيرة إلى توقيت جيني دقيق
يبدأ كل حيوان ثديي حياته كخلية واحدة تحمل مجموعة كروموسومات من الأم ومجموعة من الأب. على الرغم من أن هاتين الحزمتين الوراثيتين تحتويان على حروف DNA متقاربة جدًا، إلا أنهما تأتيان مغطاة بعلامات كيميائية مختلفة تساعد على تحديد أي الجينات تُشغّل وأيها تُثبّط. تستكشف هذه الدراسة كيفية الحفاظ على توازن أحد أنظمة الوسم هذه خلال الأيام الأولى بعد الإخصاب في الفئران، ولماذا يؤدي اضطراب هذا التوازن إلى إخلال التطور الطبيعي.
والدان، جينومات مغلفة بشكل مختلف
في الثدييات، تتصرف بعض الجينات بشكل مختلف اعتمادًا على ما إذا كانت واردة من الأم أم الأب، وهي ظاهرة تُسمى الطباعة الجينومية. الطباعة التقليدية تعتمد على علامات كيميائية على DNA نفسه، لكن في السنوات الأخيرة اكتشف العلماء نوعًا ثانويًا، أقصر عمرًا، يعتمد على تعديل في بروتينات الهيستون يُدعى H3K27me3. تعمل هذه الهيستونات كبكرات يلتف حولها الـDNA، ويميل H3K27me3 إلى إسكات الجينات المجاورة. في الأجنّة الطبيعية للفأر، يحمل الجينوم الأمومي قدرًا أكبر من هذه العلامة مقارنة بالجسم الأبوي فورًا بعد الإخصاب، مما يساعد على قمع نسخ جينية أمومية محددة بينما يسمح لنسخ أبوية بالعمل.
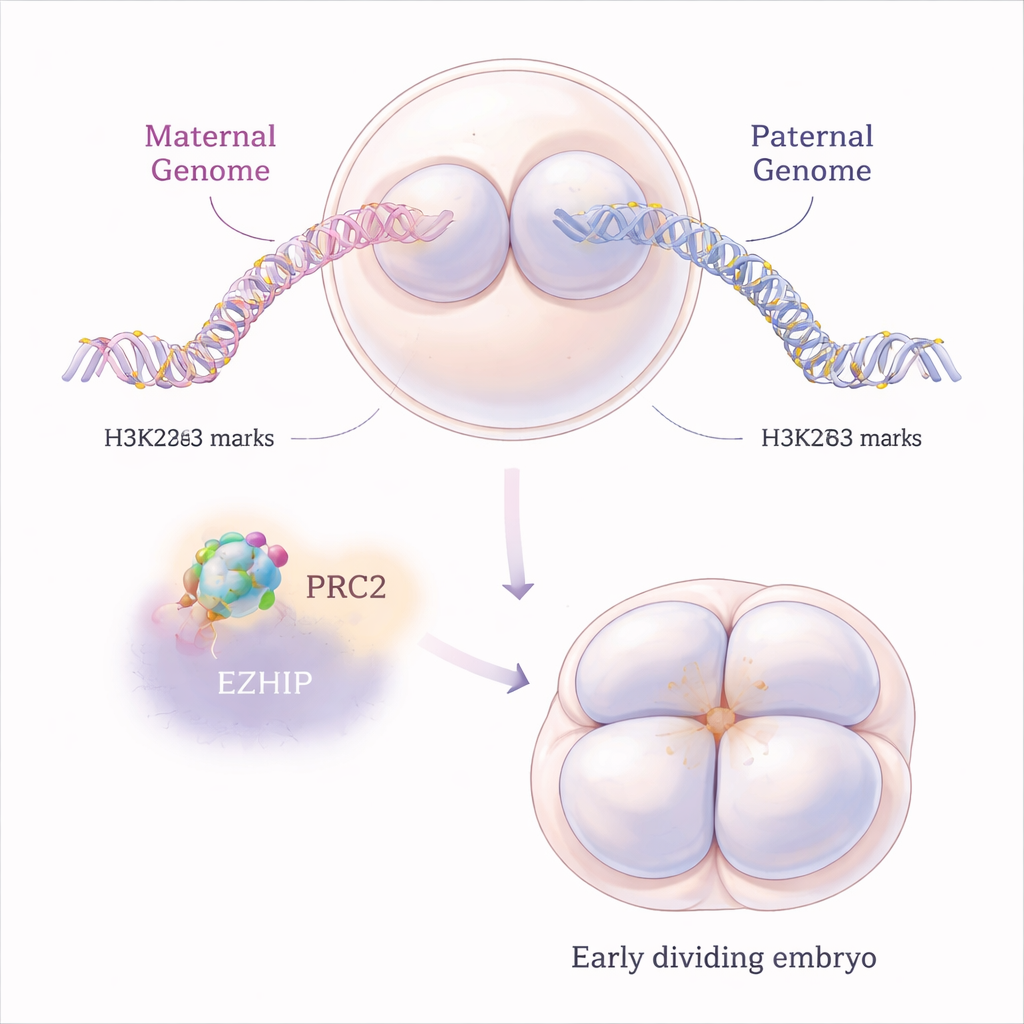
مكبح جزيئي لكابح قوي
يُوضع H3K27me3 على الكروماتين بواسطة آلة بروتينية كبيرة تُسمى PRC2. ركز المؤلفون على EZHIP، بروتين أقل شهرة يرتبط بـPRC2 ويبطئه. تنتج بويضات الفأر الكثير من رنا Ezhip، ويستمر بروتين EZHIP الناتج في الأجنّة خلال انقسامات الخلايا القليلة الأولى. بدراسة فئران أمهاتها تفتقر إلى Ezhip، سأل الباحثون ماذا يحدث عندما يُزال هذا المكبح الطبيعي. وجدوا أنه، دون EZHIP، اكتسبت البويضات والأجنّة المبكرة علامات H3K27me3 إضافية، لكن بطريقة «مُسطّحة» بشكل مفاجئ: بدلاً من مجالات حادة ومحددة جيدًا، انتشرت العلامة القمعية بصورة أوسع وطمرت الأنماط الطبيعية، مؤثرة على كروموسوماتٍ أمومية وأبوية على حد سواء.
عندما يكسر الإفراط في القمع الطباعة
باستخدام طرق حساسة لرسم خريطة الجينوم، أظهر الفريق أن التمايز المعتاد بين مشاهد H3K27me3 الأمومية والأبوية قد فُقد إلى حد كبير في الأجنّة التي تتطور من بويضات ناقصة Ezhip. اكتسبت مناطق عديدة كانت عادة تحافظ على H3K27me3 على نسخة واحدة فقط من الوالدتين هذه العلامة على كلتيهما، أو تلاشت أنماطها. وكان لهذا التغير عواقب هامة على الجينات المطبوعة التي تُسيطر عليها عادة H3K27me3 بدلًا من مثيلة الـDNA. في الأجنّة الضابطة، تميل هذه الجينات إلى التعبير أساسًا من الأليل الأبوي. أما في الأجنّة التي تفتقر إلى EZHIP الأمومي، فعادة ما كانت تُشغّل نفس الجينات من النسختين الأبوية والأمومية، وارتفعت مستويات الرنا الإجمالية للعديد منها بدلًا من أن تُسكّت مضاعفة.
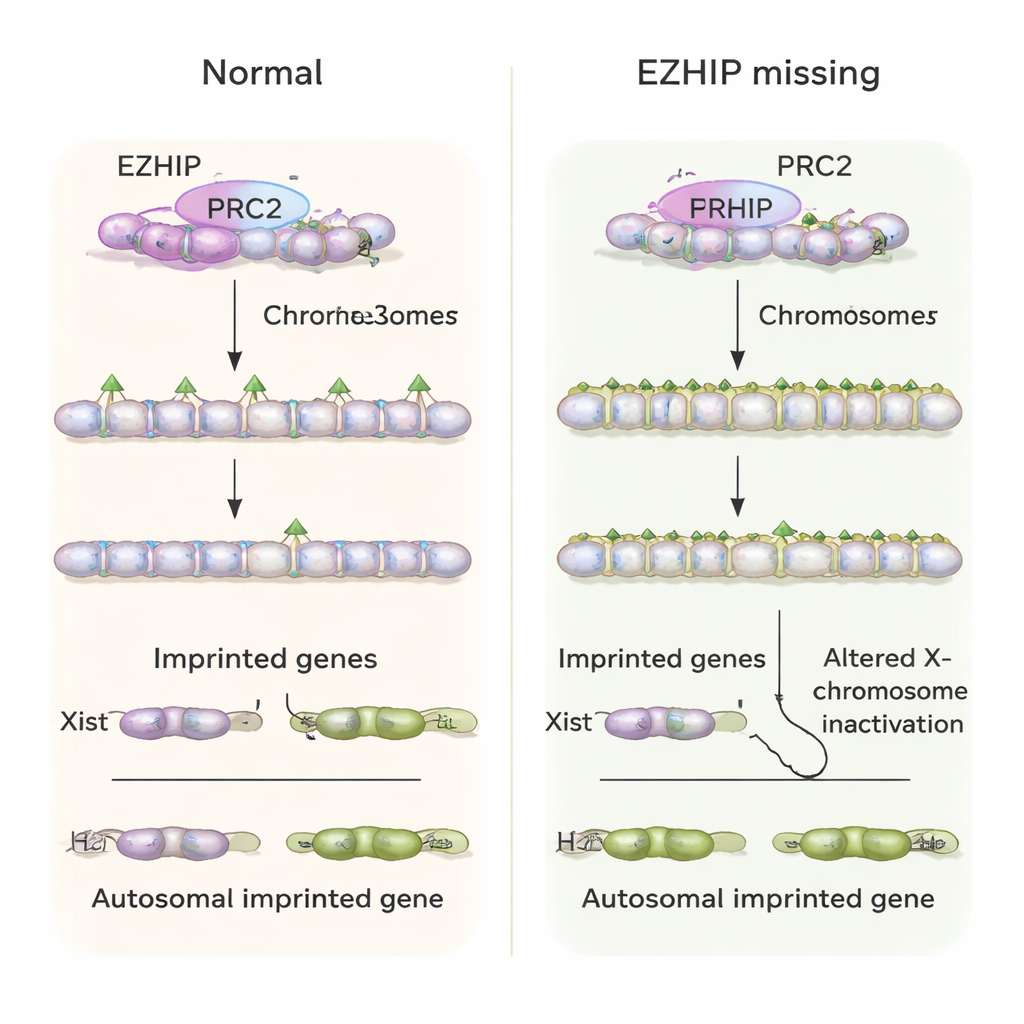
تعطيل ضبط كروموسوم X وصحة الجنين
أحد الجينات المطبوعة المعتمدة على H3K27me3 هو Xist، رنا طويل يغطي ويُعطّل أحد كروموسومات X في الخلايا الأنثوية لموازنة جرعة الجينات مع الذكور. عادةً تعبر الأجنّة المبكرة للفأر عن Xist من X الأبوي فقط في الإناث، ولا تُعبر عنه في الذكور على الإطلاق. في غياب EZHIP الأمومي، لاحظ المؤلفون أن الأجنّة الأنثوية غالبًا ما عبّرت عن Xist من كلا كروموسومي X، بينما بدت الأجنّة الذكرية قد شغّلت Xist من كروموسوم X الوحيد لديها «بشكل غير مناسب». أدى ذلك إلى أنماط تعطيل غير طبيعية للجينات المرتبطة بـX. وعلى مستوى الحيوان الكامل، كان عدد الفئران المولودة لأمهات ناقصات Ezhip أقل، وأظهرت الأجنّة نموًا متغيرًا ومشكلات في الأنسجة ما قبل الجنينية التي تدعم المشيمة، متسقة مع إجهاد تطوري طويل الأمد ناجم عن فشل الطباعة المبكرة.
الكثير من الشيء الجيد قد يكون ضارًا
قد يبدو للبسيط أن المزيد من علامة تثبيط مثل H3K27me3 سيكتفي بإسكات المزيد من الجينات. بدلًا من ذلك، تُظهر هذه الدراسة أن تحميل الجينوم بهذه العلامات بنمط خاطئ يمكن أن يقوض بالفعل قدرتها على العمل كمفاتيح دقيقة. بإزالة EZHIP، أطلق الباحثون PRC2، مما تسبب في انتشار H3K27me3 على نطاق واسع بصورة شوهت إشارات الطباعة وسيطرت على منظمات حاسمة مثل Xist بشكل خاطئ. تبرز الدراسة أن الأجنّة المبكرة لا تعتمد فقط على وجود الجزيئات الصحيحة، بل على ضبط نشاطاتها بدقة حتى تقرأ الجينومات الأمومية والأبوية بالتوازن الصحيح.
الاستشهاد: Diop, S., Richart, L., Petitalot, A. et al. H3K27me3-dependent imprinting and transcriptional regulation in early mouse embryos requires EZHIP-mediated restriction of PRC2 activity. Nat Commun 17, 1758 (2026). https://doi.org/10.1038/s41467-026-68467-4
الكلمات المفتاحية: علم التوريث فوق الجيني, الطباعة الجينومية, تطور الجنين المبكر, تعطيل الكروموسوم X, بوليكوم PRC2