Clear Sky Science · ar
المسوحات CRISPR الحية تكشف أعضاء مركب SAGA كمُنظِّمين رئيسيين لتكوّن الدم
لماذا يهم الحفاظ على توازن إنتاج الدم
يُنتج جسدك يومياً بهدوء مئات المليارات من خلايا الدم الجديدة التي تنقل الأكسجين، وتقاتل العدوى، وتوقف النزف. يعتمد هذا الإنتاج المتواصل على خلايا «أم» نادرة في نخاع العظم تسمى خلايا جذعية مكوّنة للدم. عندما يختل الآلية التي تتحكم بهذه الخلايا، قد يصاب الناس بفقر الدم، أو ضعف المناعة، أو سرطانات مثل اللوكيميا. تسأل هذه الدراسة سؤالاً بسيطاً لكنه قويًا: من بين الآلاف من الجينات في جينومنا، أيّ منها ضروري فعلاً للحفاظ على إنتاج خلايا الدم بشكل صحي ومتوازن؟
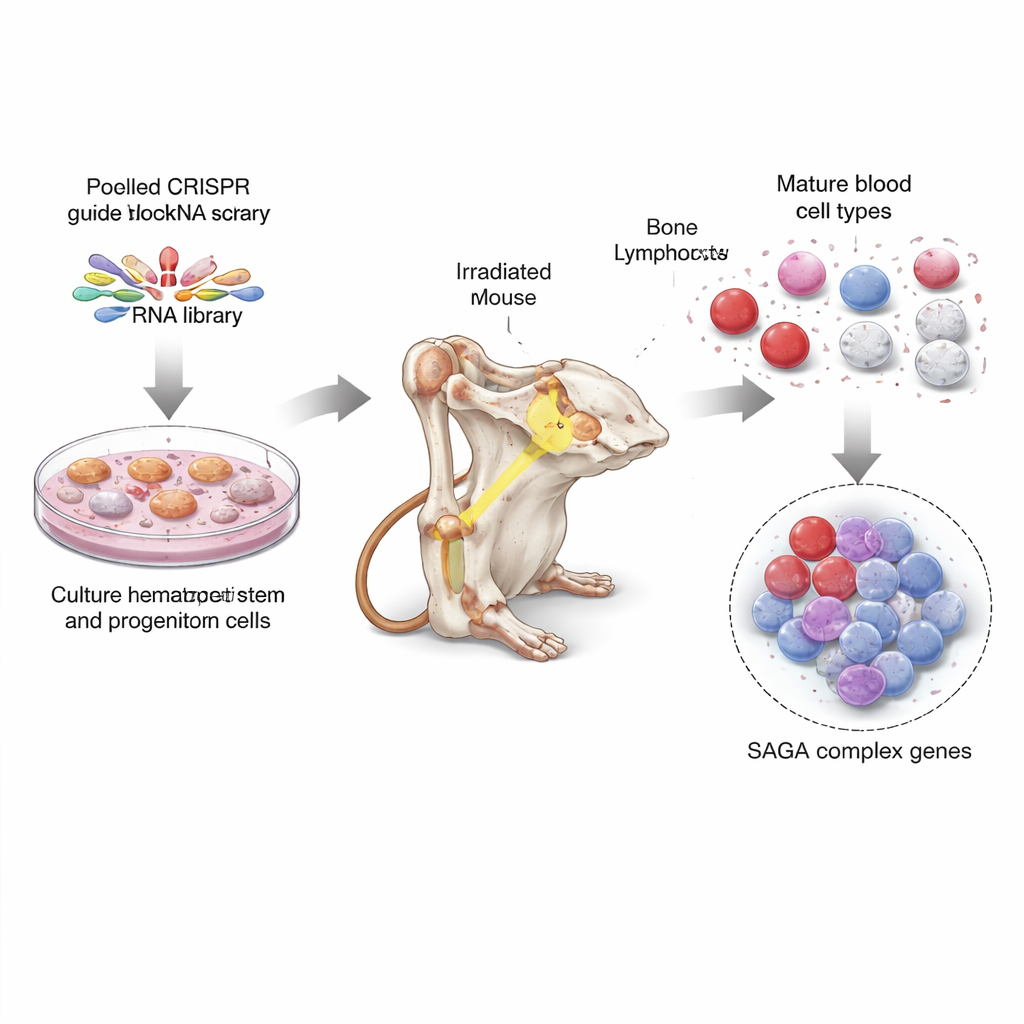
رحلة كنز جينومية شاملة في خلايا جذعية فأرية
لمعالجة هذا، استخدم الباحثون تقنية CRISPR، أداة تحرير الجينات التي يُشبهها البعض بمقصّ جزيئي، لإيقاف تشغيل تقريباً كل جين في جينوم الفأر، بعشر دلائل توجيهية لكل جين. نما الفريق أولاً أعداداً كبيرة من خلايا نخاع العظم الجذعية والسابقة في ظروف مزرعية خاصة، ثم أصابوا هذه الخلايا بمجمعة من دلائل CRISPR بحيث تحمل كل خلية تعطيلًا لجين مختلف. بعد ذلك، زرعوا هذه الخلايا المعدلة المختلطة في عشرات الفئران المشعة، مما أتاح للخلايا المُعدّلة إعادة بناء أنظمة الدم لدى الحيوانات. بعد شهور، نقّوا أنواعاً مختلفة من خلايا الدم الناضجة والخلايا الشبيهة بالجذع من نخاع العظم وقرأوا أي دلائل CRISPR كانت متمثلة أكثر أو أقل. كشف هذا أي خسائر جينية تُفضّل الخلايا غير الناضجة، وأيها يدعم إنتاج خلايا دم مكتملة التكوين.
يبرز محور تحكّم مخفي يُدعى SAGA
بين العديد من المنظمات المعروفة لتكوّن الدم، ظهرت نتيجة مفاجِئة: مجموعة من المكوّنات البنيوية لتجمع بروتيني كبير يُدعى مركب SAGA، بما في ذلك جينات مسماة Tada2b وTaf5l وTada1. لا يصنع SAGA خلايا الدم مباشرة؛ بل يساعد على تشغيل أو إيقاف جينات أخرى عن طريق وضع علامات كيميائية على بروتينات تغليف الحمض النووي المسماة هستونات. عندما عطّل الفريق هذه المكوّنات من SAGA بشكل منفرد وزرع الخلايا المعدّلة في فئران، لاحظوا نمطاً متسقاً. تراكمت الخلايا غير الناضجة في نخاع العظم، لكن قدرتها على النضوج إلى خلايا بيضاء متداولة وخلايا حمراء وبعض خلايا المناعة تقلّصت بشدة. باختصار، تعطلت خلايا الجذع والسابقة في عنق زجاجة، غير قادرة على إكمال المسار إلى خلايا دم وظيفية كاملة.
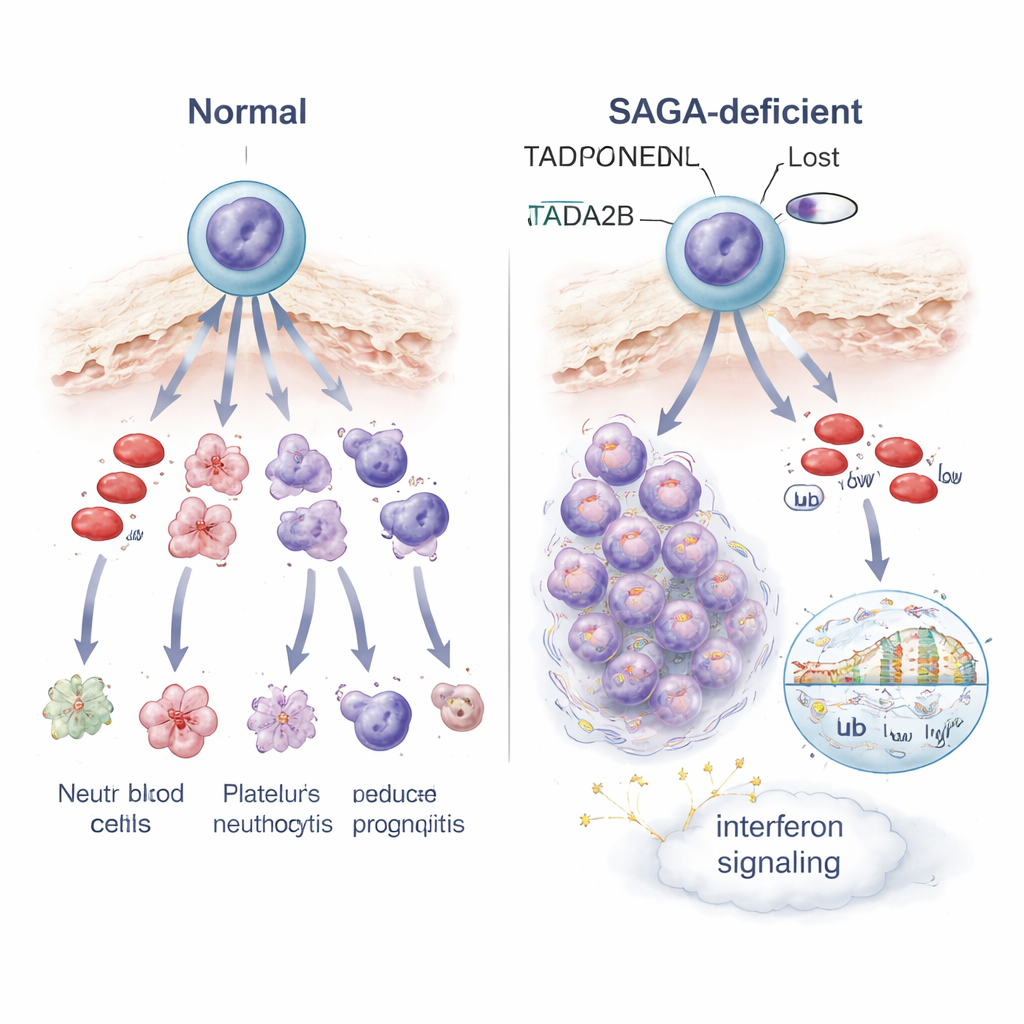
كيف يغيّر تعطل التحكم الجيني مصير الخلايا وإشارات الإجهاد
لفهم ما يحدث داخل هذه الخلايا المحجوزة، قيم العلماء نشاط الجينات خليةً خليةً وبالتحليل الكلي. أعاد فقدان Tada2b أو Taf5l برمجة نشاط العديد من الجينات في الخلايا الجذعية، مع سمتين بارزتين. أولاً، جُمعت الجينات المشاركة في إشارة الإنترفيرون — التي تُمثّل عادة جزءاً من دفاع الجسم ضد الفيروسات — فأصبحت مفعّلة، مما يشير إلى حالة إنذار داخلي أو إجهاد. ثانياً، أصبحت الميتوكوندريا، محطات الطاقة الصغيرة في الخلايا، أقل نشاطاً، وأبدت الخلايا المتغيرة حساسية أكبر لمركب دوائي يستهدف إنتاج الطاقة الميتوكوندرية. وعلى مستوى تغليف الحمض النووي، أظهرت الخلايا التي تفتقر إلى Tada2b انخفاضاً في علامة هستون مرتبطة بالكروما النشط المفتوح، وتغيّرات في علامة أخرى مرتبطة بكيفية قراءة الجينات. هذه التحولات في كيمياء الكروما على الأرجح تفسّر لماذا تُسجّل العديد من الجينات، بما في ذلك الجينات الموجّهة للنضج السليم للدم، تنظيمًا خاطئًا.
من الآليات الأساسية إلى نماذج المرض
سأل الفريق بعد ذلك ما إذا كان تعديل نشاط SAGA صعوداً أو نزولاً يمكن أن يعكس هذه التأثيرات. إجبار الخلايا على إنتاج Tada2b إضافية خفّض نشاط الجينات المرتبطة بالإنترفيرون وقلّل نسبة الخلايا الشبيهة بالجذع، وهي صورة معكوسة لمسألة التعطيل. معالجة الخلايا الجذعية الطبيعية بمركب دوائي يثبط الوحدات الإنزيمية الرئيسية في SAGA أعادت إنتاج جزء كبير من توقيع فقدان Tada2b، مما يعزز فكرة أن نشاط SAGA في تعديل الكروما مركزي لدوره. أخيراً، توجه الباحثون إلى نموذج خلوي بشري لمتلازمة خلل التنسج النخاعي، اضطراب قبل لِوكيميا يعجز فيه إنتاج الدم وغالباً ما ترتفع مسارات الإنترفيرون. عندما عطّلوا مكونات SAGA في هذه الخلايا البشرية وزرعوها في فئران ناقصة المناعة، اكتسبت الخلايا المعدلة ميزة نمو وأضاءت مجدداً برامج الإنترفيرون والميالويد، مما يوحي بأن هذا المركز التنظيمي يشكل أيضاً سلوك المرض.
ماذا يعني هذا لصحة الدم والعلاجات المستقبلية
للقارئ العام، الرسالة الأساسية هي أن هذه الدراسة تكشف عن مركز تحكّم قوي — مركب SAGA — يساعد خلايا الدم الجذعية على أن تقرر متى تبقى غير ناضجة، ومتى تنضج، وكيف تتفادى استجابات الإجهاد الضارة. عندما تختفي أجزاء رئيسية من SAGA، تتراكم الخلايا الجذعية لكنها تفشل في إنتاج ما يكفي من خلايا الدم العاملة، بينما ترتفع إشارات الإجهاد الشبيهة بالمضادة للفيروسات وتضعف الميتوكوندريا. لا تعمق هذه الاكتشافات فهمنا لكيفية الحفاظ على إنتاج الدم الصحي مدى الحياة فحسب، بل تشير أيضاً إلى أن تغيّرات دقيقة في نشاط SAGA قد تسهم في مشكلات الدم المرتبطة بالتقدم في العمر واضطرابات مثل متلازمة خلل التنسج النخاعي. على المدى البعيد، يمكن أن يساعد رسم هذه الدائرة التنظيمية العلماء على تصميم علاجات تُرجع الخلايا الجذعية المختلة نحو إنتاج دم متوازن ومتين.
الاستشهاد: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
الكلمات المفتاحية: الخلايا الجذعية المكوّنة للدم, مسح CRISPR, مركب SAGA, إشارة الإنترفيرون, متلازمة خلل التنسج النخاعي