Clear Sky Science · ar
DKK1 وNEDD4 المشتقان من خلايا العرف العصبي يعدّلان إشارة Wnt في الحقل القلبي الثاني لتنظيم تطور مجرى الخروج
لماذا يهم صانعو القلب الصغار
يبدأ قلب الجنين المبكر كأنبوب بسيط، لكنه ينبغي أن يعيد تشكيل نفسه سريعًا إلى عضو معقد يضخ الدم إلى الجسم والرئتين على حد سواء. خطوات بسيطة خاطئة في هذه العملية البنائية قد تؤدي إلى عيوب خلقية خطيرة، بما في ذلك حالات تتطلب جراحة بعد الولادة مباشرة. تكشف هذه الدراسة كيف تتواصل مجموعتان من الخلايا أثناء تشكيل ممر الخروج الرئيسي للقلب، وتحدد خطأ جزيئيًا يمكن أن يساهم في أمراض القلب الخلقية لدى الفئران والبشر.
فريقان يبنيان منحدر خروج القلب
الجزء من القلب الذي يحمل الدم خارج البطينين — مجرى الخروج — يتكوّن من منطقة تُدعى الحقل القلبي الثاني. يجب أن تظل الخلايا هنا «سلفية» مرنة بما يكفي لتُضاف إلى مجرى الخروج النامي، ثم تتحول إلى عضلة ناضجة في الوقت المناسب. إلى جانبها تتحرك خلايا العرف العصبي، وهي مجموعة متنقلة تساهم في بناء الشرايين الكبرى والصمامات. أشارت أعمال سابقة إلى أن خلايا العرف العصبي تؤثر بطريقة ما على الحقل القلبي الثاني، لكن كان مَبهمًا كيف تتم هذه المحادثة الخلوية. 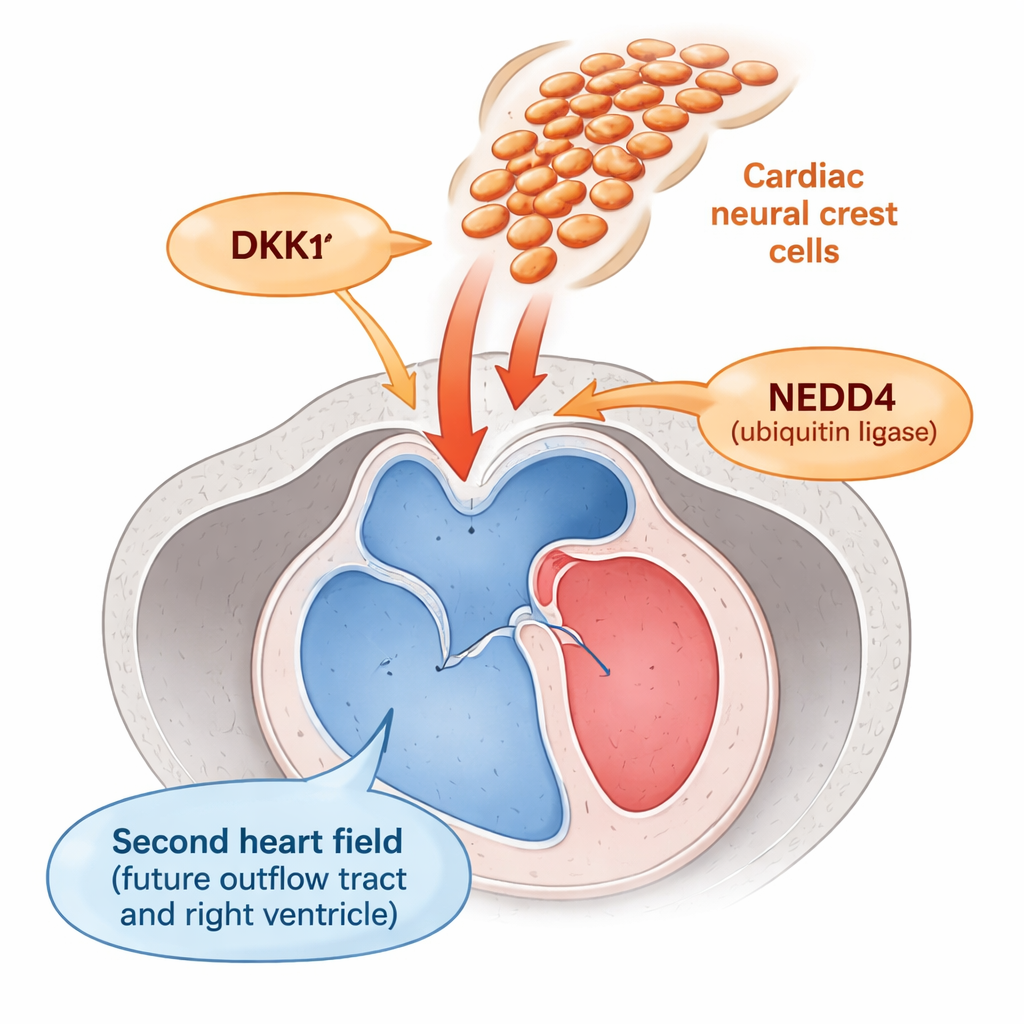
مفتاح تعتيم جزيئي لإشارات النمو
اكتشف الباحثون أن خلايا العرف العصبي تعمل كمفتاح تعتيم لإشارة نمو رئيسية تُدعى Wnt، التي تحافظ على انقسام الخلايا السلفية وتؤخر نضوجها. وجدوا أن خلايا العرف العصبي مصدر رئيسي لبروتين صغير مُفرز هو DKK1، الذي يثبط إشارة Wnt في الخلايا المجاورة. ويخضع DKK1 عادة للتحكم بواسطة NEDD4، بروتين يوسم DKK1 للتخلص منه. في أجنة الفئران التي تفتقر إلى Nedd4 بشكل محدد في خلايا العرف العصبي، تراكم DKK1 إلى مستويات غير طبيعية. هذا الارتفاع في DKK1 خفّض نشاط Wnt في الحقل القلبي الثاني المجاور، كما دل على ذلك انخفاض بيتا‑كاتينين النووي — وهو مؤشر نموذجي على إشارة Wnt — وانخفاض مستويات عدة جينات مستجيبة لـWnt.
عندما يخطئ التوقيت، تفشل هندسة القلب
كان لوجود DKK1 بكثرة وانخفاض Wnt نتيجة واضحة: بدأت خلايا الحقل القلبي الثاني تتحول إلى نسيج عضلي قلبي مبكرًا جدًا. ظهرت مؤشرات العضلة الناضجة مبكرًا في هذه المنطقة السلفية، وبقي عدد أقل من الخلايا غير المتمايزة لتمديد مجرى الخروج. من خلال تتبع الخلايا المنقسمة مع مرور الوقت، أظهر الفريق أن عدد خلايا الحقل القلبي الثاني المضافة إلى مجرى الخروج كان أقل في الطفرات. ونتيجة لذلك، كان مجرى الخروج أقصر ودار بشكل غير صحيح، مما أدى إلى سوء محاذاة بين الشرايين الكبرى والبطينين. تشابهت هذه الأخطاء الهيكلية مع عيوب كونوتروكال لدى البشر مثل بطين ذو مخرجين والعيوب المرافقة التي لوحظت في فئران ناقصة Nedd4 تمامًا.
إثبات دور الإشارة وصلة بمرض بشري
لتأكيد أن تغيّر إشارة Wnt هو السبب الفعلي لهذه المشكلات، عبث الباحثون بالطريق الإشاري باستخدام أدوية في فئران حاملات. حجب Wnt في أجنة صحية دفعها نحو نفس التمايز المبكر وعيوب الدوران التي شوهدت عند فقدان Nedd4، بينما أدى تقليل جرعة جين Dkk1 في خلفية ناقصة Nedd4 إلى إنقاذ جزئي في حجم ودوران مجرى الخروج. أخيرًا، عرّف الفريق طفلًا مصابًا برباعية فالوت وكان يحمل تغييرًا وراثيًا نادرًا موروثًا في NEDD4 أضعف قدرته على وسم DKK1 للتحلل. الفئران المصممة لتحمل نفس متغير Nedd4 طورت عيوبًا في جدار القلب والحاجز على الجهة اليمنى، مما يدعم الفكرة أن خلل التحكم بـNEDD4–DKK1 يمكن أن يساهم في أمراض القلب الخلقية لدى البشر. 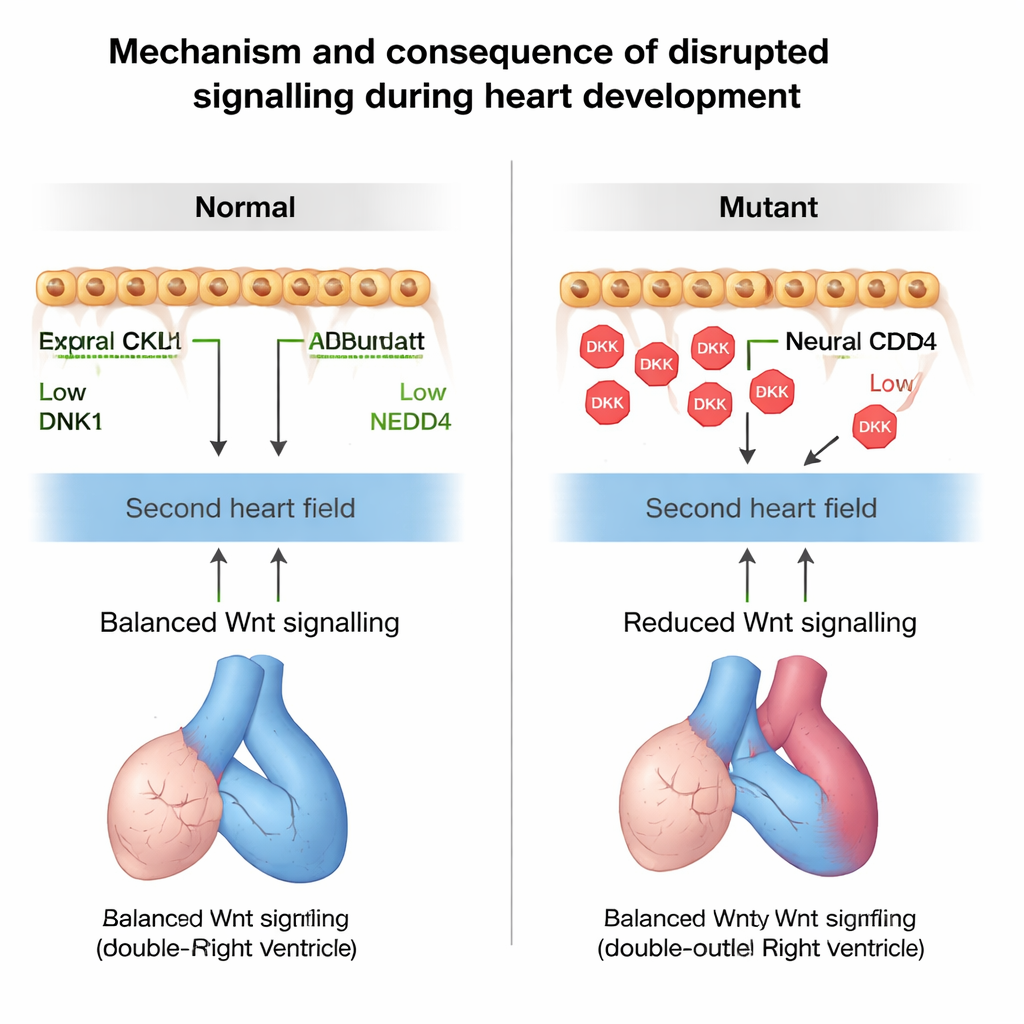
ماذا يعني هذا لفهم عيوب القلب
لغير المتخصصين، الرسالة الأساسية أن «منحدر الخروج» في القلب يعتمد على توقيت دقيق لانتهاء تضاعف اللبنات البنائية وبدء تحولها إلى عضلة. هذا التوقيت لا يتحكم به نسيج القلب وحده، بل أيضًا خلايا العرف العصبي المجاورة التي تضبط إشارة النمو عبر زوج NEDD4–DKK1. عندما يكون مفتاح التعتيم الجزيئي مضبوطًا منخفضًا جدًا، يصبح مجرى الخروج ناقص البناء وغير محاذٍ، مما يؤدي إلى عيوب خلقية خطيرة. من خلال رسم هذا المسار وربطه بمتغير جيني بشري، تقدم الدراسة دلائل جديدة حول كيفية نشوء بعض عيوب القلب الخلقية وتسلط الضوء على أهداف جزيئية محتملة للتشخيص أو التدخل في المستقبل.
الاستشهاد: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
الكلمات المفتاحية: أمراض القلب الخلقية, تطور القلب, خلايا العرف العصبي, إشارة Wnt, مجرى خروج القلب