Clear Sky Science · ar
حذف شائع في الـ DNA يغيّر المنطقة غير المُترجمة 3'UTR في جين mdr1 مرتبط بتناقص الحساسية لمفلوكين لدى طفيليات P. vivax من مرضى كامبوديا
لماذا تهم هذه الدراسة عن الملاريا
بالنسبة للأشخاص الذين يعيشون في مناطق تستوطِنها الملاريا أو الذين يسافرون إليها، تُعد الأدوية الفعالة شريان حياة. لكن طفيليات الملاريا تتطور باستمرار لتتجنب العلاج. تركز هذه الدراسة على Plasmodium vivax، المسبب الرئيسي للملاريا خارج أفريقيا، وتكشف عن تغيير جيني طفيف قد يساعد الطفيلي بالفعل في تحمل دواء مهم واحد هو المفلوكين. فهم هذا التحول الآن قد يساعد المسؤولين الصحيين على التقدم بخطوة أمام ظهور مقاومة للأدوية.
طفيلي عنيد وخيارات علاج تتقلص
تسبب عدة طفيليات مرتبطة الملاريا في البشر، لكن P. vivax يصعب التخلص منه بشكل خاص. يمكنه الاختباء في الكبد لشهور قبل أن يظهر مجددًا في الدم، وغالبًا ما يدور بمستويات منخفضة جدًا بحيث لا تلتقطه الاختبارات القياسية. لعقود، كان مركب الكلوروكوين فعّالًا ضد P. vivax، لكن علامات المقاومة انتشرت. نتيجة لذلك، توصي منظمة الصحة العالمية الآن باستخدام علاجات مركبة تعتمد على الأرتميسينين (ACTs)، التي تجمع بين دواء سريع المفعول وشريك أطول مفعولًا مثل المفلوكين. وبما أن استنبات P. vivax في المختبر يمثل تحديًا، يعتمد العلماء بشكل كبير على عينات المرضى والدلائل الجينية لتتبع كيفية استجابة الطفيلي لهذه الأدوية.
جزء صغير مفقود من الـ DNA في جين رئيسي لمقاومة الدواء
سلسَل الباحثون جينومات 206 عينات من P. vivax مأخوذة من مرضى ملاريا في كمبوديا بين 2021 و2023. بحثوا عن مقاطع DNA محذوفة أو مكررة. من بين العديد من إعادة الترتيبات، برزت واحدة: أكثر من 80% من الطفيليات حملت حذفًا صغيرًا في الـ DNA يقع مباشرة بعد نهاية منطقة الترميز في جين يُدعى mdr1 (مقاومة متعددة الأدوية 1). يشفر هذا الجين بروتين ناقل يمكنه ضخ مركبات متنوعة، بما فيها الأدوية، عبر غشاء داخل الطفيلي. وعلى عكس الطفرات المبلغ عنها سابقًا، لم يغيّر هذا الحذف المكون من 837 زوجًا من قواعد النيوكليوتيد تسلسل البروتين نفسه. بل كان موجودًا في ما يُسمى بالمنطقة غير المترجمة 3'UTR، وهي قطعة من الجين لا تُترجم إلى بروتين لكنها يمكن أن تؤثر بقوة على كمية البروتين التي تُنتَج في النهاية.
حذوفات مستقلة ورسائل معدّلة من نفس الجين
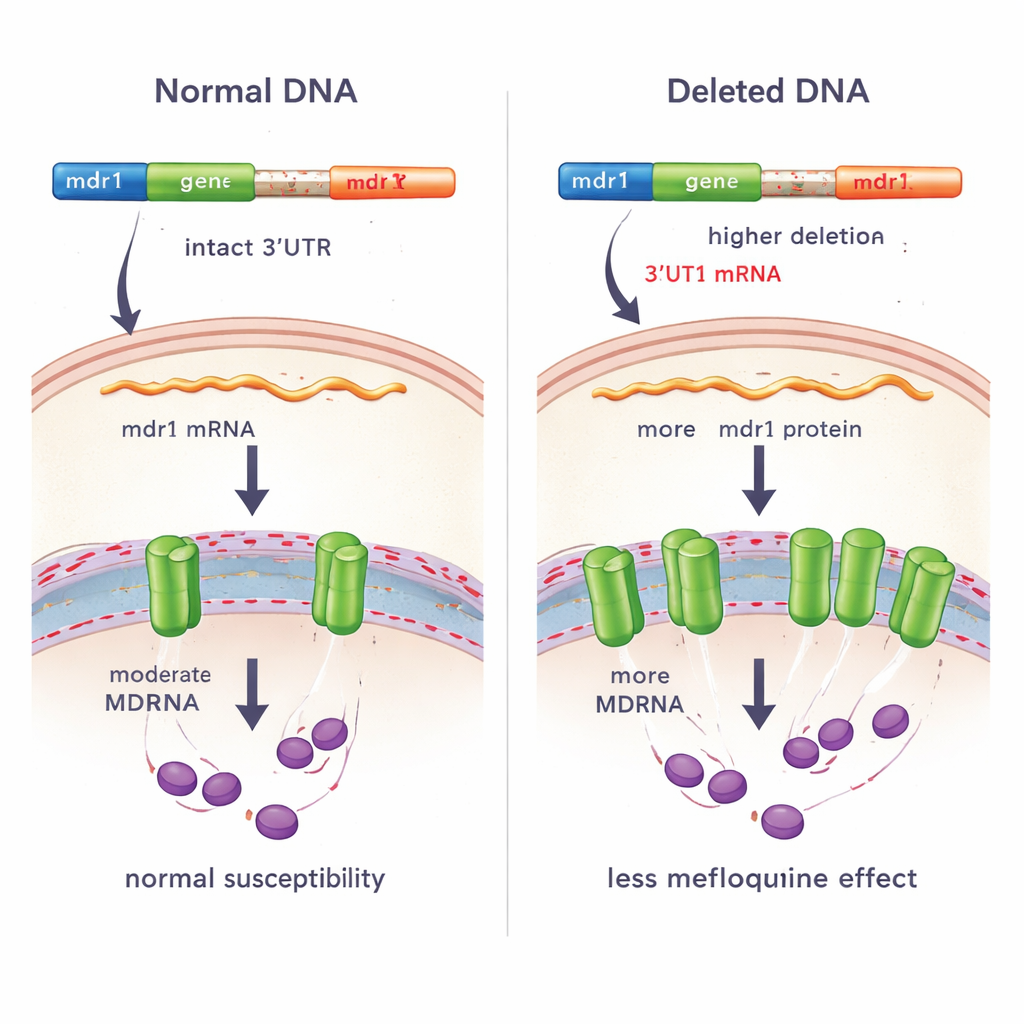
لفحص ما إذا كانت تغييرات مشابهة تظهر في أماكن أخرى، أعاد الفريق تحليل ما يقرب من 830 جينومًا لـ P. vivax من 25 دولة. اكتشفوا حذفًا آخر، أقصر، يتداخل مع نفس المنطقة اللاحقة لـ mdr1 في طفيليات من أمريكا الجنوبية. أظهرت المقارنات التفصيلية واختبارات PCR التأكيدية أن الحذوفين في جنوب شرق آسيا وأمريكا الجنوبية مختلفان، مما يشير إلى أنهما نشآ بشكل مستقل—وهو مؤشر قد يدل على أن الانتخاب الطبيعي قد يفضّل التغيرات في هذه المنطقة التنظيمية. باستخدام تسلسل RNA على 95 عدوى من كمبوديا، أظهر الباحثون أن الطفيليات التي تحمل الحذف أفرزت نسخة بديلة من RNA الرسول لـ mdr1، بوجود 3'UTR مختلف. وبعد احتساب طول المرسوم، كانت كمية mRNA لـ mdr1 لدى الطفيليات الحاملة للحذف تقريبًا ضعف تلك لدى الطفيليات التي لا تحمله، مما يوحي بأن الـ DNA المفقود أو تسلسل 3'UTR الجديد يساعد في استقرار أو زيادة التعبير عن الجين.
ربط الحذف باستجابة الدواء في المرضى والاختبارات المختبرية
نظرًا لأن mdr1 له دور مذكور في مقاومة عدة أدوية ضد الملاريا، تحقق الفريق مما إذا كان الحذف مرتبطًا بكيفية استجابة الطفيليات للعلاج. قارنوا أولًا مدى سرعة إزالة الطفيليات من دم المرضى بعد علاجهم بالأرتيسونات. بين 167 عدوى، لم يكن هناك فرق ذو دلالة في معدلات الإزالة بين الطفيليات الحاملة للحذف وتلك التي لا تحمله، مما يشير إلى أن هذا التغيير الجيني لا يؤثر مباشرة على الحساسية للأرتيسونات بحد ذاتها. ومع ذلك، في مجموعة أصغر من 14 عدوى حيث قاس الباحثون نمو الطفيليات في وجود المفلوكين خارج الجسم، ميّلت الطفيليات الحاملة للحذف إلى قيم IC50 أعلى—أي كانت بحاجة إلى كمية أكبر من الدواء لكبح النمو—مقارنة بالطفيليات بدون الحذف. هذا النمط يتسق مع انخفاض الحساسية للمفلوكين، رغم أن حجم العينة كان محدودًا.
ارتفاع مقلق مع مرور الوقت وما قد يعنيه
لفهم مدى انتشار الحذف، فحص المؤلفون 592 عينة مؤرشفة من P. vivax جُمعت عبر كمبوديا من 2014 إلى 2024. قبل إدخال المفلوكين كجزء من العلاجات المركبة لـ vivax حوالي 2016–2017، حمل نحو 30% من الطفيليات الحذف. بعد التحول، ارتفعت النسبة إلى أكثر من 60% ثم استقرت، وهو اتجاه كان قويًا إحصائيًا وبقي كذلك حتى عند التركيز على شرق كمبوديا وحدها. كان الحذف موجودًا بالفعل بمستويات منخفضة قبل أن يُستخدم المفلوكين على نطاق واسع ضد P. vivax، ربما نتيجة التعرض غير المباشر عندما استُخدم الدواء لعلاج P. falciparum أو لأن التغير يؤثر أيضًا على استجابة أدوية أخرى. إلى جانب تقارير حديثة عن تباطؤ طفيف في إزالة الطفيليات بعد علاج بالأرتميسينات، تثير النتائج القلق من أن P. vivax في كمبوديا قد تتجه نحو تراجع فعالية مركب الأرتيسونات–المفلوكين الحالي.
ماذا يعني هذا لجهود مكافحة الملاريا
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أنه حتى عندما يبدو جين مقاومة الدواء الرئيسي لدى الطفيلي سليمًا، فإن تغييرات صغيرة في "أسلاك التحكم" المجاورة للـ DNA يمكن أن تغيّر مدى نشاط الجين. في هذه الحالة، يبدو أن حذفًا شائعًا في منطقة غير مُشفَّرة من mdr1 يعزّز نشاط الجين ويرتبط بتأثير أضعف قليلًا للمفلوكين على P. vivax. ومع أنه لا توجد بعد أدلة واضحة على فشل العلاج في كمبوديا، فإن تزايد تواتر هذا الحذف يوحي بأن الضغط الدوائي قد يفضّل بصمت الطفيليات التي تحمل هذه السمة. إن التعرف على مثل هذه العلامات الجينية الدقيقة ومراقبتها مبكرًا يمكن أن يساعد السلطات الصحية على تعديل سياسات الأدوية، وتصميم أدوات مراقبة أفضل، وحماية مخزون الأدوية الفعّال المتناقص ضد الملاريا.
الاستشهاد: Ko, K., Tebben, K., Andrianinarivomanana, T. et al. A common DNA deletion altering the 3’UTR of mdr1 is associated with reduced mefloquine susceptibility in P. vivax parasites from Cambodian patients. Nat Commun 17, 1748 (2026). https://doi.org/10.1038/s41467-026-68456-7
الكلمات المفتاحية: Plasmodium vivax, مقاومة الأدوية ضد الملاريا, مفلوكين, جين mdr1, كمبوديا