Clear Sky Science · ar
منتجات طبيعية ببتيدية تستهدف ClpC1 تعطل بروتومات الميكوبكتيريوم السلِّي بطرق متفاوتة
لماذا يهم تعطيل طواقم التنظيف البكتيرية
لا يزال السل واحداً من أكثر الأمراض المعدية فتكاً في العالم، وسلالات ميكوبكتيريوم توبركولوسس المقاومة للأدوية تجعل علاجه أكثر صعوبة. تستهدف معظم المضادات الحيوية الحالية جدار الخلية أو قدرة البكتيريا على توليد الطاقة ونسخ مادتها الوراثية. تستكشف هذه الدراسة نقطة ضعف مختلفة تماماً: «فريق التنظيف» الداخلي للخلية الذي يحافظ على صحة البروتينات. من خلال فهم كيفية تعطيل جزيئات جديدة مبنية على منتجات طبيعية لهذا النظام، يأمل العلماء في تصميم أدوية مستقبلية يمكنها قتل بكتيريا السل بطرق جديدة وأكثر متانة.
مركز تنظيف البروتين في الخلية
مثل جميع الخلايا الحية، تبني بكتريا السل باستمرار البروتينات وتطويها وتصلحها وتعيد تدويرها. يلعب مركب كبير يدعى مركب ClpC1–ClpP1P2 دوراً مركزياً في شبكة صيانة البروتين هذه. يعمل جزء (ClpC1) كمرافق (chaperone) يتعرف على البروتينات التالفة أو غير المرغوب فيها ويجذبها، بينما يقوم الجزء الآخر (ClpP1P2) بقطعها إلى أجزاء لإعادة تدويرها. هذا النظام ضروري لبقاء البكتيريا، لا سيما تحت الضغوط مثل الحرارة أو هجوم المضادات الحيوية. مجموعة من الببتيدات الطبيعية — الإيكوميسين والإيلاميسينات (الروفوميسينات) والسيكلومارين — معروفة بقدرتها على الارتباط بـClpC1 وإظهار نشاط قوي ضد السل، ما يشير إلى أن هذا المركب قد يكون هدفاً دوائياً قوياً. 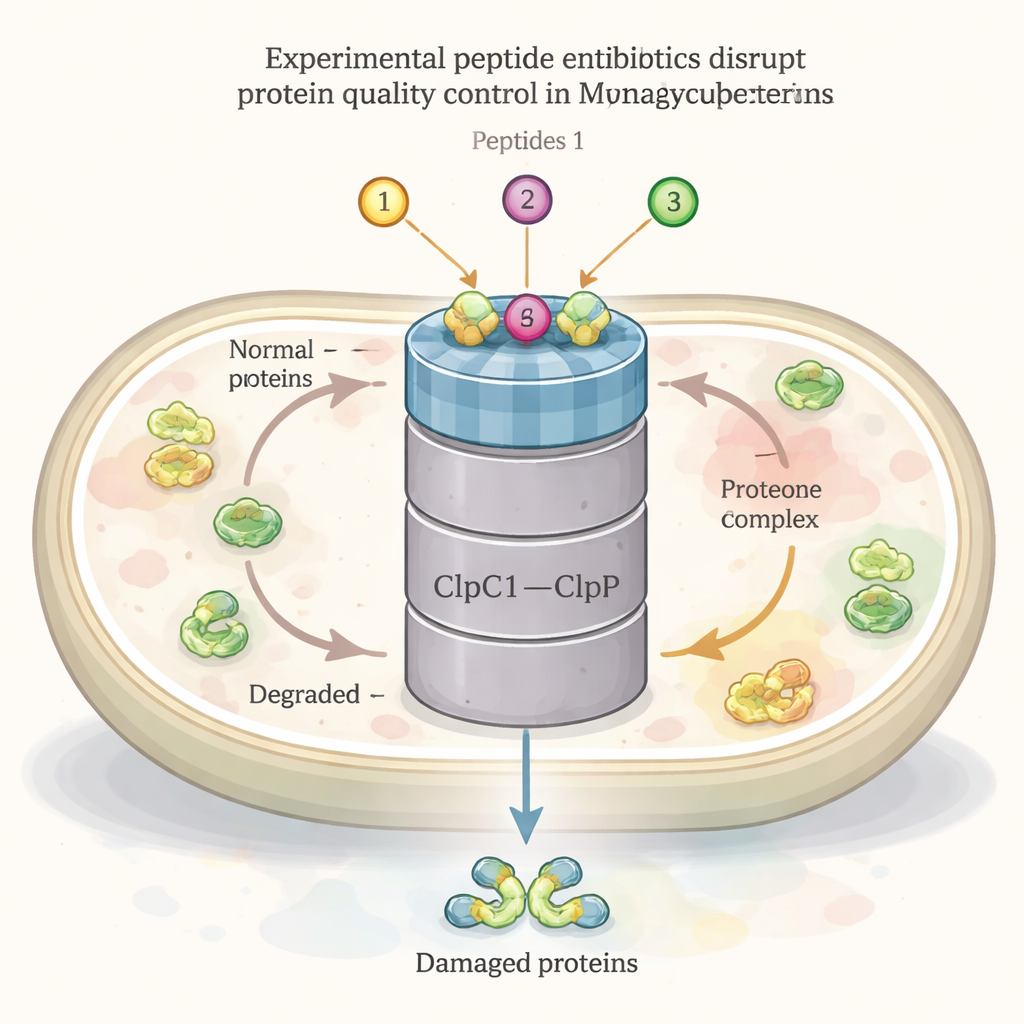
ثلاثة أدوية قريبة، ثلاث تأثيرات مختلفة
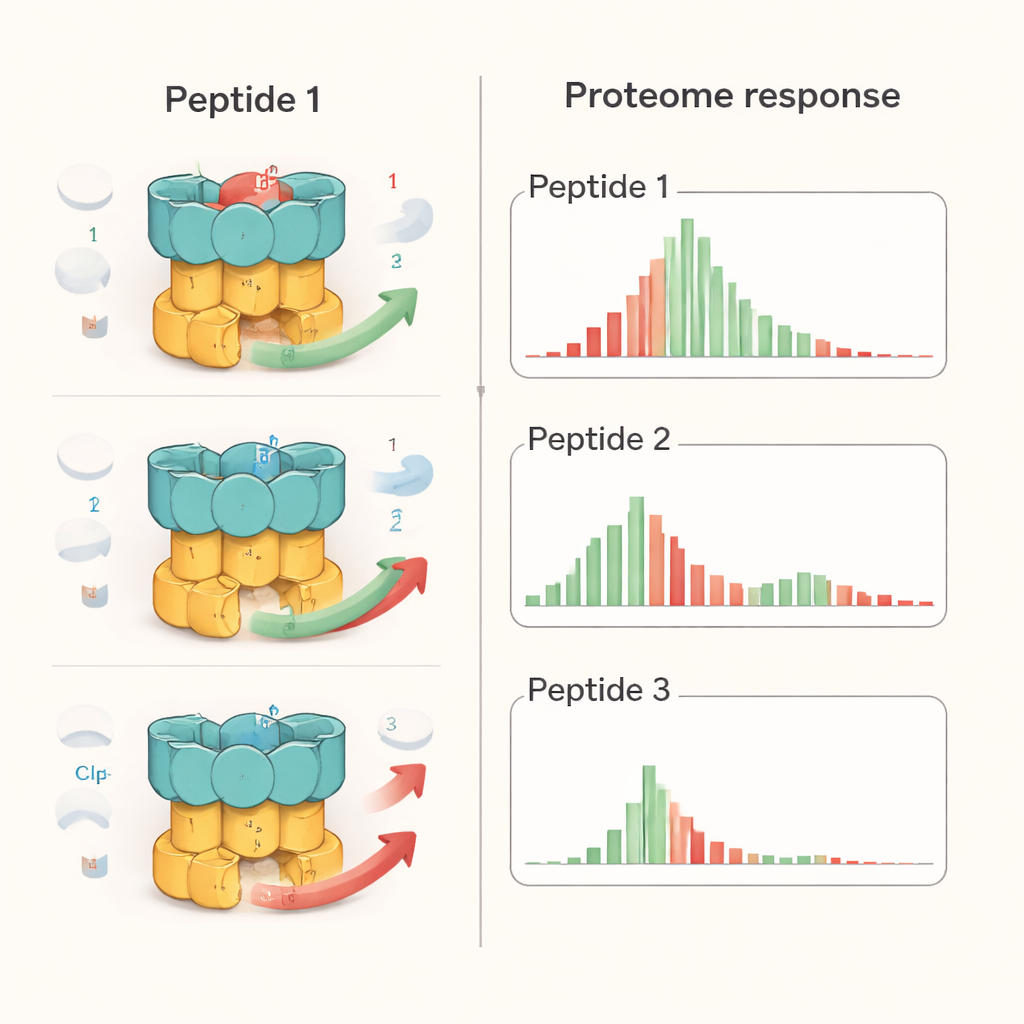
فحص الباحثون ممثلاً واحداً من كل عائلة ببتيدية: نظير للإيكوميسين (Ecu*), إيلاميسين E (IlaE) ومشتق من السيكلومارين (ديسوكسيسايكلومارين، dCym). على الرغم من أن الثلاثة ترتبط بمنطقة واحدة من ClpC1، إلا أنها لا تتصرف بالمثل داخل الخلية. باستخدام البروتيوميك الكمي — نهج يقيس آلاف البروتينات دفعة واحدة — وجدوا أن Ecu* أحدث أوسع اضطراب، مغيراً بشكلٍ كبير مستويات نحو 17% من جميع بروتينات البكتيريا. غيّرت IlaE حوالي 12%، وdCym نحو 7%. فقط 72 بروتيناً تأثروا باستمرار بجميع المركبات الثلاثة، وكان معظمهم منخفضي الوفرة. يوضح هذا أن كل جزيء يدفع ماكينة ClpC1 في اتجاه مختلف، معيداً تشكيل توازن البروتينات داخل الخلية بطرق مميزة بدلاً من «إيقاف الماكينة» ببساطة.
سد المفرمة مقابل قطع التيار
لوضع هذه التأثيرات في سياقها، قارن الفريق الببتيدات بدواء السرطان بورتزوميب الذي يثبط على نطاق واسع إنزيمات تحلل البروتينات. في بكتيريا السل، تسبب بورتزوميب تراكمًا عامًا للعديد من البروتينات، كما هو متوقع عند إيقاف المفرمات. بالمقابل، أنتجت الببتيدات أنماطاً أكثر انتقائية: تراكمت بعض أهداف ClpC1 المعروفة بينما نُقصت أخرى، ولم تُلاحظ مثبطة عامة لجميع تحطيم البروتين. أظهرت تجارب مختبرية مفصلة بمكونات مكررة أن كل ببتيد غيَّر طريقة معالجة ركائز محددة. فعلى سبيل المثال، تدخلت الثلاثة في تدمير بروتين تنظيمي واحد (PanD)، لكن فقط Ecu* أعاق تفكك نموذج لبروتين غير مرتب، وفقط dCym أعاق تحلل بروتين الحماية من الإجهاد Hsp20. تشير هذه الاختلافات إلى أن الشكل العام ومرونة كل بروتين مستهدف يؤثران في كيفية تأثره عندما تُعيَّر ClpC1 بواسطة مركب معيَّن.
مستجيبون للإجهاد وإنقاذ البكتيريا الذاتي
تمتلك بكتيريا السل أنظمة احتياطية للتعامل عندما يفوق تلف البروتين قدرة جهاز التنظيف الرئيسي. من هذه الأنظمة مرافق آخر، ClpC2، الذي يمكنه ربط جزيئات شبيهة بالسيكلومارين وتقليل تأثيرها على ClpC1. وجدت هذه الدراسة أنه بالرغم من أن الببتيدات الثلاثة يمكن أن ترتبط بـClpC2 في أنبوب الاختبار، إلا أن مشتق السيكلومارين (dCym) فقط هو الذي أثار في الواقع ارتفاع مستويات ClpC2 في البكتيريا الحية وأصبح أكثر فعالية عندما نُقص ClpC2 تجريبياً. بالمقابل، بقيت Ecu* وIlaE فعّالتين حتى عند خفض ClpC2، مشيرة إلى أنهما تتجاوزان إلى حد كبير هذا المسار الإنقاذي الذاتي. كما اكتشف الفريق ارتباطاً قوياً محدد المركب مع Hsp20، البروتين الصغير الذي يساعد في منع التكتلات الضارة: فقد سبب Ecu* (وإلى درجة أقل IlaE) زيادات دراماتيكية في مستويات Hsp20، وربط Ecu* مباشرةً بـHsp20، كاشفاً عن صلة جديدة بين هذه المرشحات الدوائية وشبكة استجابة الخلية للإجهاد.
تحويل الإجهاد إلى ميزة علاجية
بما أن نظام ClpC1 مهم بشكل خاص تحت ظروف قاسية، اختبر الباحثون الأدوية بينما كانت البكتيريا تتعرض لإجهاد حراري طفيف يزيد من حمولة البروتينات الملتوية. تحت هذه الظروف، أصبح كل من Ecu* وdCym أكثر فتكا بكثير، وبلغا سماحية سامة مشابهة لبورتزوميب، رغم أنهما يعملان بشكل أكثر انتقائية. يثبت هذا أن استهداف جهاز مراقبة جودة البروتين بعناية يمكن أن يكون فعالاً مثل إيقاف كل البروتيازات الرئيسية، لكن مع تحكم أكثر دقة محتملة. كما أظهرت الدراسة أن العديد من التغيرات التي أحدثها Ecu* في مستويات البروتين لم تعكس ببساطة تغيرات في نشاط الجينات، مما يبرز أن تعطيل ClpC1 يضطرب أساساً التنظيم بعد تصنيع البروتينات.
ماذا يعني هذا لعلاجات السل المستقبلية
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن بكتيريا السل تعتمد على نظام داخلي دقيق للتنظيف والاستجابة للإجهاد للبقاء. تنجذب الببتيدات الثلاثة المستمدة من المنتجات الطبيعية إلى نفس الماكينة المركزية لكنها تدفعها إلى أوضاع مختلفة، مما يؤدي إلى تشوهات متنوعة ومحددة للغاية في تركيبة البروتينات لدى البكتيريا. من المهم أن مركبات شبيهة بالإيكوميسين والإيلاميسين تتجنب آلية إنقاذ بكتيرية مدمجة قد تقلل من تأثير السيكلومارين، ومع ذلك تضعف الممرض تحت الإجهاد. تجعل هذه الخصائص منها هياكل واعدة لأدوية السل المستقبلية، بما في ذلك جزيئات مصممة قد تجبر خلايا السل على تدمير بروتيناتها الحيوية بشكل انتقائي أو تُبنى في «شيميرات مستهدفة للبروتين» لتوجيه الهضم الذاتي البكتيري بدقة.
الاستشهاد: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
الكلمات المفتاحية: السل, مراقبة جودة البروتين, ClpC1, مقاومة المضادات الحيوية, مضادات حيوية من المنتجات الطبيعية