Clear Sky Science · ar
بروتينات لَيڭاز E3 يوبيكويتين الحارسة تُستهدف نازعات أمين APOBEC3 المرتبطة بالسرطان للتَّحَلُّل لتعزيز سلامة الجينوم البشري
حماية حمضنا النووي من «النيران الصديقة»
تستخدم خلايانا إنزيمات قوية لإتلاف الحمض النووي الفيروسي، مما يساعدنا على صد العدوى. لكن بعض هذه الإنزيمات نفسها، إذا تُركت دون ضابطة، قد تترك ندوباً على جينومنا وتساهم في السرطان. تكشف هذه الدراسة كيف تراقب الخلايا البشرية هذه الإنزيمات الخطرة، آخذةً الضوء على نظام «مراقبة جودة» داخلي يعلِّم النسخُ المُعيبة لتتحلل قبل أن تعيد كتابة حمضنا النووي.
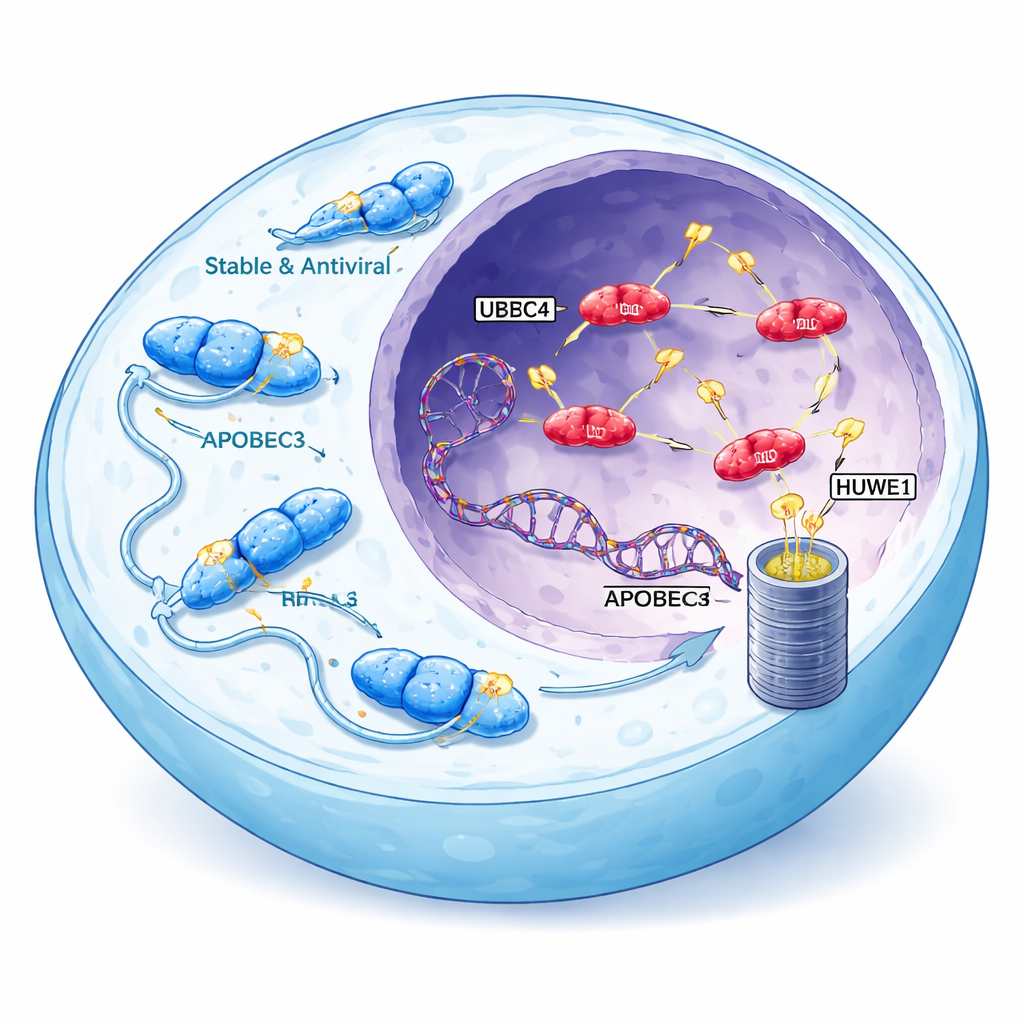
مقاتلو الفيروسات الذين قد ينقلبون علينا
عائلة إنزيمات APOBEC3 تساعد عادةً في الدفاع ضد فيروسات مثل فيروس العوز المناعي البشري (HIV) عن طريق تعديل الحمض النووي الفيروسي كيميائياً، محدثة أخطاء قاتلة للفيروس. يحمل البشر سبعة متغيرات من APOBEC3، وثلاثة منها — A3A وA3B وشكل من A3H يُدعى النمط الوراثي I (A3H-I) — مرتبطة بقوة بنماذج الطفرات المرصودة في العديد من السرطانات. يمكن لهذه الإنزيمات المحددة الانتقال إلى نواة الخلية، حيث توجد كروموسوماتنا، وإحداث مجموعات مميزة من الطفرات في الجينوم. تظهر بصمات الطفرات المرتبطة بـAPOBEC في أكثر من نصف السرطانات البشرية، لا سيما في سرطانات الثدي والرئة والمثانة، حيث تزيد من مجموعة التغيرات الجينية التي قد تستفيد منها الأورام للتكيّف ومقاومة العلاج.
لماذا الأشكال الأكثر خطورة غير مستقرة بشكل غريب
ومن المثير للفضول أن إنزيمات APOBEC3 الأكثر ارتباطاً بالسرطان هي أيضاً الأقل استقراراً. بخلاف نظائرها السيتوبلازمية التي تتراكم بمستويات عالية وتعيق الفيروسات بكفاءة، فإن A3A وA3B وA3H-I تتحلّل بسرعة وعادة ما تتواجد بتركيزات منخفضة في النواة. افترض الباحثون أن هذه اللااستقرار قد يكون مقصوداً: إذا كانت الخلايا تقيد فعلياً مستويات بروتينات APOBEC3 النوية، فإن أي خلل في هذا الضبط قد يطلق موجات من الطفرات. باستخدام A3H-I كنموذج، أظهروا أن نازعات APOBEC3 المرتبطة بالسرطان تُدمر في المقام الأول عبر البروتيازوم، مهراس البروتين الخلوي، بعد تمييزها بعلامات جزيئية صغيرة تُدعى يوبيكويتين على مواقع أمينية متعددة.
اكتشاف الحراس الخلويين
لتحديد الآلية المسؤولة عن تعليم A3H-I وA3B، دمج الفريق فحص كريسبر مع رسم خريطة قرب البروتينات. مهَّدوا خلايا تتوهج بشكل مختلف اعتماداً على مدى استقرار A3H-I ونمطه غير الضار A3H-II، ثم عطلوا منهجياً جينات متورطة في تحلل البروتين. برزت ثلاث ليغازات يوبيكويتين — UBR4 وUBR5 وHUWE1. أدى تعطيل أيٍّ من هذه الليغازات إلى رفع مستوى A3H-I النوي غير المستقر بشكل انتقائي من دون أن يؤثر على A3H-II السيتوبلازمي المستقر. كما أن نفس الليغازات زادت مستويات A3B الذاتية في خطوط خلايا القولون والخلايا المناعية، وحذف الثلاثة معاً أعطى ازدياداً تراكمياً في وفرة A3B. وأظهرت تجارب بيوكيميائية أن UBR5 وHUWE1 يرتبطان فعلياً بـA3B وA3H-I ويُلحقان سلاسل يوبيكويتين مباشرة، بينما يبدو أن UBR4 يتخصص في إطالة هذه السلاسل لجعل البروتينات أكثر قابلية للتخلص منها بكفاءة.
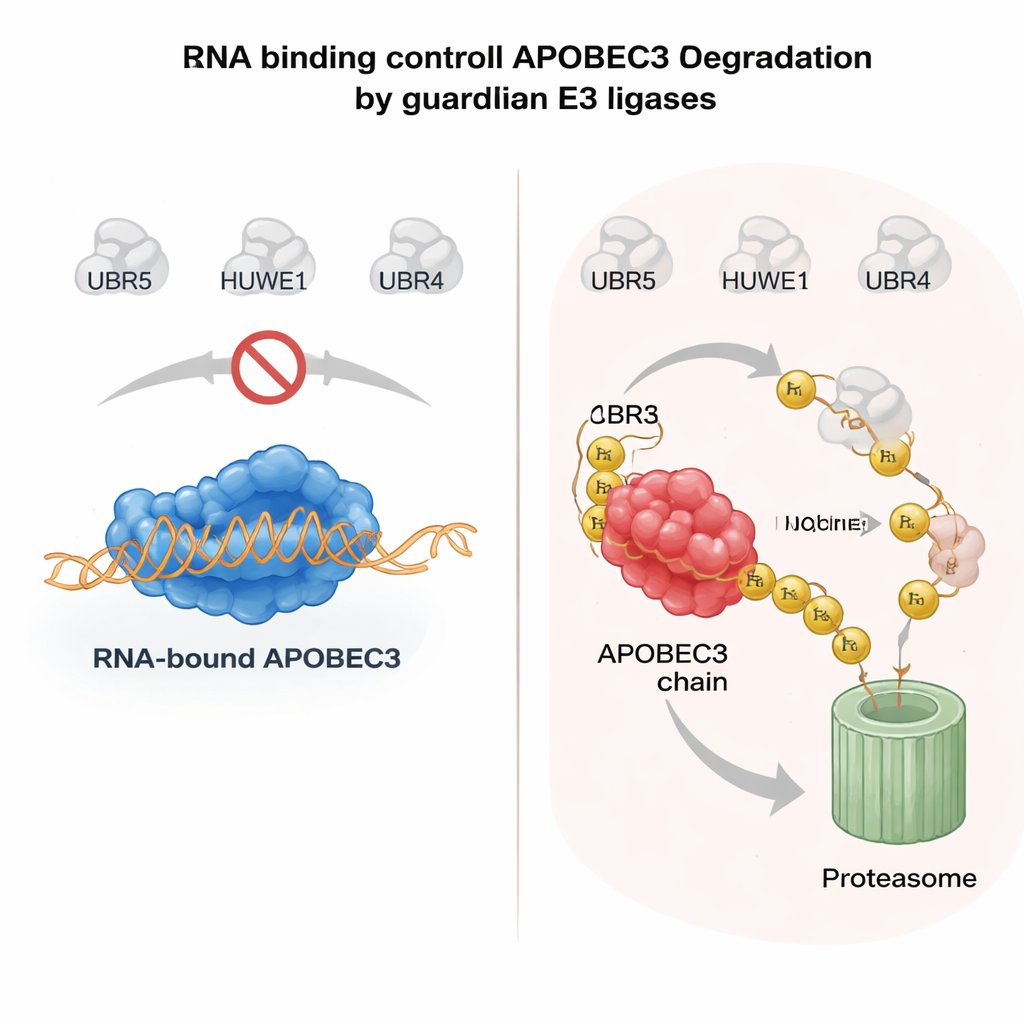
الحمض النووي الريبي كحزام أمان للإنزيمات الخطرة
ما الذي يحدد ما إذا كان إنزيم APOBEC3 يُعفى أم يُدمر؟ جاءت إشارة مفصلية من طريقة ارتباط بروتينات APOBEC3 بجزيئات الحمض النووي الريبي في السيتوبلازما. عندما يرتبط A3H أو عضو آخر من العائلة، A3G، بالحمض النووي الريبي، يميل إلى البقاء في مجمعات كبيرة في السيتوسول ويكون مستقراً نسبياً. الطفرات التي تُضعف ارتباط الحمض النووي الريبي تدفع هذه الإنزيمات إلى الانجراف إلى النواة، فقدان شركائها الواقين، وتصبح شديدة اللااستقرار. أظهر المؤلفون أنه عندما لا تكون بروتينات APOBEC3 مرتبطة بالحمض النووي الريبي، تتعرف UBR5 وHUWE1 على السطوح المكشوفة في الإنزيم، وتزينها باليوبيكويتين، وتستهدفها للتحلل النوي. في أنظمة منظفة، عززت إضافة RNase لإزالة الحمض النووي الريبي قدرة هذه الليغازات على الارتباط وتهيئة يوبيكويتين لبروتينات APOBEC3، مؤكدة أن ارتباط الحمض النووي الريبي يعمل كدرع جزيئي. تتيح هذه الآلية للخلايا إبقاء APOBEC3 المضادة للفيروسات نشطة في السيتوبلازم مع تطهير سريع لأي مجموعة غير مرتبطة مهددة للجينوم في النواة.
عندما يفشل الحراس: روابط مع طفرات السرطان
إذا كانت UBR4 وUBR5 وHUWE1 تعمل كحراس، فينبغي أن يؤدي فقدانها إلى زيادة مستويات الطفرات. اختبر الباحثون ذلك عن طريق تعطيل كل ليغاز في خلايا سرطان القولون وتتبع التغيرات في الحمض النووي مع مرور الوقت باستخدام طريقة تسلسل حساسة تقرأ «بصمات» الطفرات. أدى إزالة هذه الليغازات، لا سيما في الخلايا التي تعبر عن A3H-I، إلى تضخيم أنماط الطفرات المحددة لـAPOBEC — بالضبط النوع الموجود في الأورام البشرية. وبتوسيع التحليل إلى بيانات المرضى، حللوا آلاف جينومات السرطان ووجدوا أن الأورام التي تحمل طفرات في UBR5 أو HUWE1 لديها جزء أكبر بكثير من بصمات الطفرات المرتبطة بـAPOBEC مقارنةً بالأورام ذات الليغازات السليمة، حتى بعد احتساب الحمل الطفري الإجمالي. يشير هذا إلى أن عيوباً في ليغازات الحراسة لدى المرضى قد تسمح لإنزيمات APOBEC3 المرتبطة بالسرطان بالانتشار وإعادة تشكيل جينوم الورم.
ما معنى ذلك لعلاج السرطان في المستقبل
بالنسبة لغير المتخصص، الخلاصة أن خلايانا تمتلك نظام مراقبة متطوراً يمنع الإنزيمات المضادة للفيروسات المفيدة من تخريب حمضنا النووي عن طريق الخطأ. تعمل UBR4 وUBR5 وHUWE1 كحراس يشعرون عندما تتوقف بروتينات APOBEC3 عن الارتباط الآمن بالحمض النووي الريبي، وخاصة في النواة، ويُرسلونها إلى المهراس الخلوي. عندما يضعف هذا النظام — بسبب طفرات في الليغازات أو أدوية تمنع تحلل البروتين — يمكن لنشاط APOBEC3 أن يغذي الفوضى الجينية التي تدفع تطور السرطان ومقاومتَه للعلاج. يفتح فهم شبكة الحراس هذه أبواباً لعلامات تشخيصية جديدة، مثل طفرات الليغازات أو مستويات بروتينات APOBEC، ويشير إلى أن ضبط هذا المسار بعناية قد يساعد يوماً في الحد من موجات الطفرات الضارة في الأورام من دون المساس بدفاعنا المضاد للفيروسات.
الاستشهاد: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
الكلمات المفتاحية: APOBEC3, ثبات الجينوم, ليغاز يوبيكويتين, طفرات السرطان, تحلل البروتين