Clear Sky Science · ar
تبديل فالنين واحد إلى ليوسين يعطل ارتباط AP2-G من Plasmodium falciparum بـ DNA ويكشف دور GDV1 في تنشيط ap2-g
كيف تتخذ طفيليات الملاريا قراراً حرجاً بين الحياة والموت
تواجه طفيليات الملاريا التي تعيش في دمنا باستمرار قراراً يغير مصيرها: مواصلة التكاثر داخل مضيف واحد، أم التحول إلى شكل يمكنه الانتقال إلى مضيف جديد عبر لدغة بعوضة. تكشف هذه الدراسة كيف يستطيع تغيير صغير جداً في بروتين واحد للطفيلي أن يقضي تماماً على تلك المرحلة المعدية الجاهزة للبعوض، مما يفتح زوايا جديدة لعرقلة انتقال الملاريا.
المفترق الذي تواجهه الطفيليات
في مجرى الدم، تركز طفيليات Plasmodium falciparum في الغالب على النمو السريع، مما يسبب المرض. لكن أقلية صغيرة تتحول إلى أشكال جنسية تسمى الأمشاج (gametocytes)، وهي المراحل الوحيدة التي يمكن للبعوض نقلها واستدامتها. كان سر كيفية تحول بعض الطفيليات فقط ضمن التجمع إلى هذا الشكل لغزاً طويلاً. أظهرت أعمال سابقة أن بروتينين طفيليين، GDV1 وبروتين رابط للحمض النووي يُدعى AP2-G، يقعان في قلب هذا القرار. يساعد GDV1 على إيقاظ جين ap2-g الذي يكون عادة خاملاً، ويقوم AP2-G بدوره بتشغيل مجموعة من الجينات التي تدفع التطور الجنسي. كانت الدراسة الحالية تهدف إلى استكشاف بروتين آخر، كيناز يُدعى STK2، لكنها عثرت بدلاً من ذلك على نتيجة أكثر دراماتيكية في AP2-G نفسه.
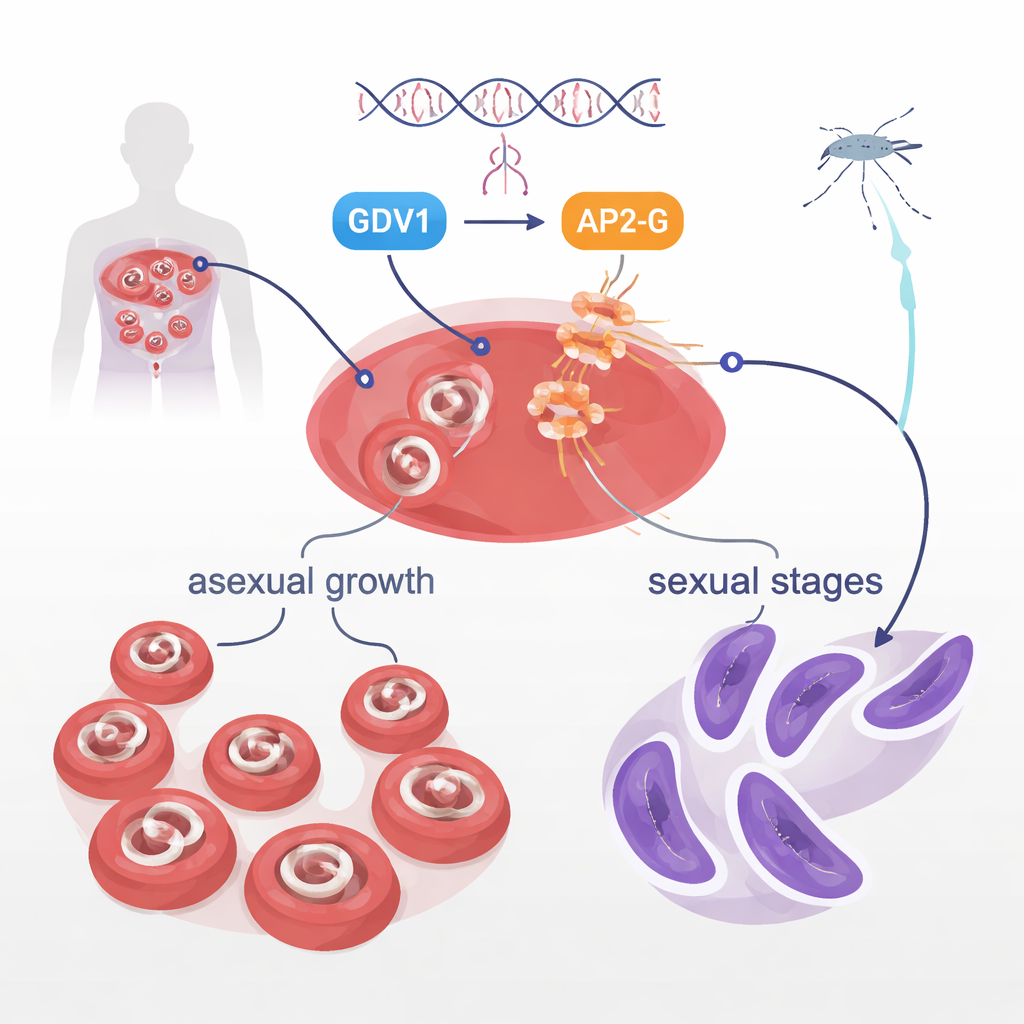
حمض أميني واحد يوقف الانتقال
أثناء حذف جين stk2 في سلالة مخبرية واحدة من الطفيلي، لاحظ الباحثون أن هذه الطفيليات فقدت تماماً قدرتها على إنتاج الأمشاج، مع استمرار نموها اللاجنسي بشكل طبيعي. بشكل مفاجئ، عندما كرروا تَلاعبات مشابهة في سلالة أخرى، تشكلت الأمشاج بشكل طبيعي. كشفت تسلسل الجينوم الكامل عن المذنب المخفي: تغيير «حرف» واحد في جين ap2-g، حيث استبدل حمض أميني واحد، الفالين، بآخر مشابه جداً، الليوسين، عند الموضع 2163. يقع هذا الموضع في بداية منطقة ربط DNA في AP2-G، الجزء الذي يمسك فعلياً بأنماط DNA محددة لتشغيل الجينات. كان هذا التبديل الصغير من فالين إلى ليوسين كافياً بمفرده لإلغاء تكوين الأمشاج. عندما هندس العلماء هذه الطفرة في طفيليات طبيعية بخلاف ذلك، اختفت الأمشاج؛ وعندما أعادوا التبديل إلى الفالين، عاد التطور الجنسي بالكامل.
كيف يكسر هذا التبديل القفل الجزيئي
لفهم سبب كون هذا التغيير الطفيف مدمرًا للغاية، جمع الفريق بين النمذجة الحاسوبية والتجارب المخبرية. أشارت توقعات البنية إلى أن استبدال الفالين بالليوسين يحرف ويزعزع الشكل الدقيق لمجال ربط DNA في AP2. في تجارب أنبوب الاختبار باستخدام بروتينات مُنقاة، ارتبط AP2-G الطبيعي بقوة بتسلسل DNA المفضل لديه، وهو رمز قصير يحتوي على النمط «GnGTAC». في المقابل، فشل AP2-G الطافر بالليوسين عند الموضع 2163 في الارتباط بهذا التسلسل تماماً. دون ارتباط مستقر بالـ DNA، لم يعد بإمكان AP2-G تنشيط جينه الخاص (حلقة تغذية إيجابية معروفة بالتحكم الذاتي) أو تنشيط عشرات الجينات اللاحقة اللازمة لدفع الطفيليات نحو المسار الجنسي. وظيفياً، أصبحت الطفيليات الطافرة «عقيمة»: لم تستطع تكوين الأشكال التي تصيب البعوض، رغم أنها استمرت في الازدهار داخل خلايا الدم الحمراء.
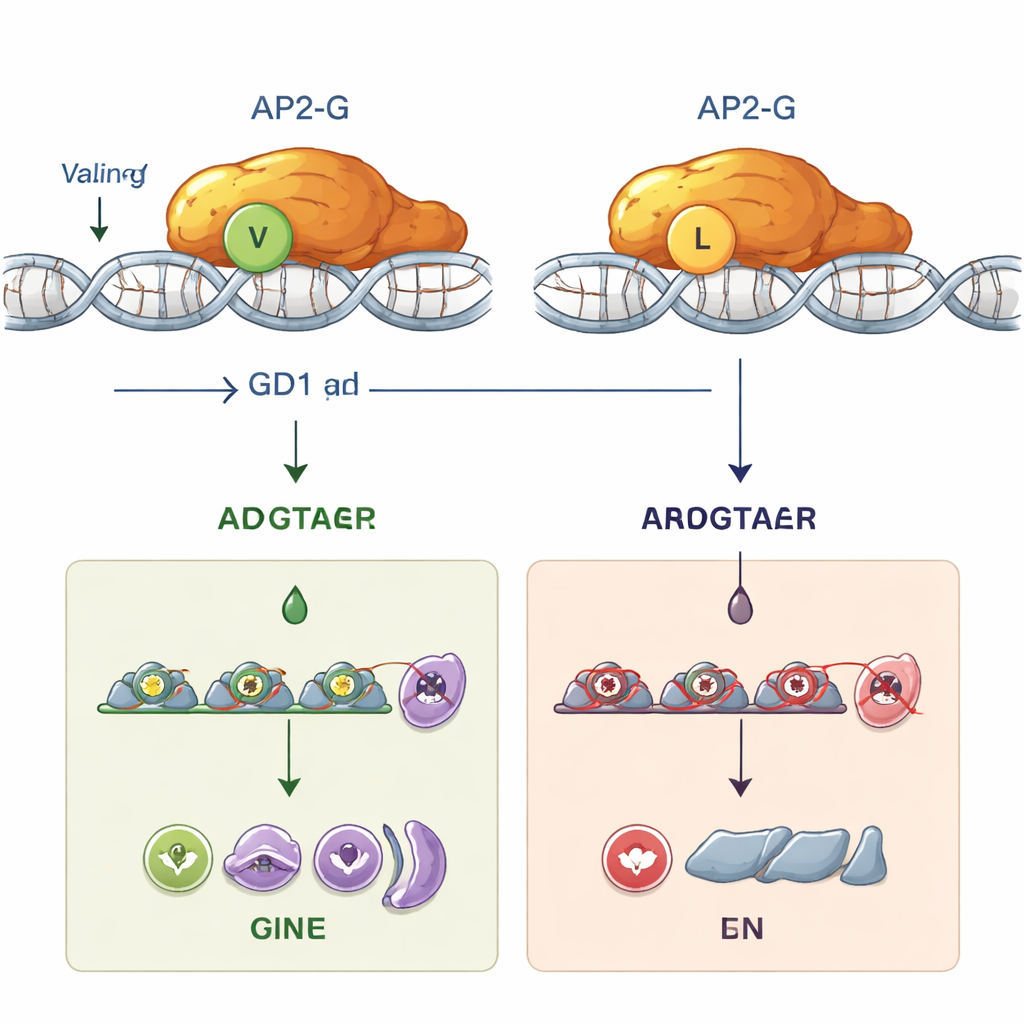
الدور الخفي لـ GDV1 قبل أن يتولى AP2-G المسؤولية
قدمت الطفرة أيضاً أداة فريدة للباحثين: طفيليات يمكن فيها تشغيل جين ap2-g، لكن AP2-G لا يستطيع الارتباط بـ DNA. باستخدام مرافقات متوهجة ومانحات ضوئية، تتبّعوا توقيت عمل العناصر المختلفة خلال دورة الطفيلي التي تستغرق 48 ساعة في خلايا الدم الحمراء. وجدوا أن بروتين GDV1 يظهر أولاً، مبكراً في مرحلة تسمى الانشطار النووي (schizogony)، وهو ضروري لبدء تعبير ap2-g من حالته الصامتة. حدث هذا التنشيط المبكر سواء كان ap2-g يشفر AP2-G الطبيعي أو النسخة الطافرة. في وقت لاحق فقط، وبمجرد تراكم كمية كافية من AP2-G الطبيعي، ظهرت الحلقة التعزيزية الذاتية القوية وتنشيط جينات «جنسية» أخرى. علامة رئيسية، بروتين يُدعى MSRP1، أضاءت فقط في الطفيليات التي تمتلك AP2-G وظيفياً، مما وفر وسيلة عملية لتمييز الطفيليات الملتزمة جنسياً مبكراً ومتأخراً. في السلالات الطافرة ذات تبديل الليوسين، كان بإمكان GDV1 إيقاظ ap2-g، لكن بروتين AP2-G المكسور لم يستطع استكمال العملية، فتعثر التطور الجنسي.
دلالات لإيقاف انتشار الملاريا
بالنسبة للقارئ العام، الخلاصة بسيطة: تعتمد طفيليات الملاريا على قفل جزيئي شديد الحساسية لاتخاذ قرار ما إذا كانت ستكون قابلة للانتقال. تُظهر هذه الدراسة أن تغيير «سنانة» واحدة في ذلك القفل — فالين واحد في منطقة مسك DNA لـ AP2-G — يمنع الطفيلي من صنع المراحل المعدية للبعوض تماماً. وفي الوقت نفسه، تُوضح أن بروتيناً آخر، GDV1، يعمل مبكراً كمفتاح لفتح جين ap2-g الصامت، قبل أن يعزز AP2-G إنتاجه ويشغّل برنامجاً جنسياً أوسع. من خلال رسم تسلسل هذه الأحداث وإنشاء سلالات طفيلية مرجعية تتوهج عند حدوث كل خطوة، يوفر العمل أدوات قوية لفحص الأدوية أو العوامل البشرية التي تتداخل مع الالتزام الجنسي. على المدى الطويل، قد يؤدي استهداف منطقة ربط DNA في AP2-G أو خطوة التنشيط التي يقودها GDV1 إلى استراتيجيات جديدة لا تكتفي بعلاج الملاريا في مريض واحد، بل تقطع سلسلة الانتقال بأكملها.
الاستشهاد: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
الكلمات المفتاحية: انتقال الملاريا, Plasmodium falciparum, تطور الخلايا التناسلية, AP2-G, GDV1