Clear Sky Science · ar
آليات هرمية تتحكم في إزالة إنزيم RNA بوليمراز II المتوقف بواسطة إصابات الحمض النووي
عندما تصطدم آلات نسخ الجينات بحاجز
كل ثانية، تسافر ملايين الآلات الجزيئية الصغيرة المسماة إنزيمات RNA بوليمراز II على طول حمضنا النووي، ناسخة الجينات إلى RNA. لكن عندما يتعرض الحمض النووي للضرر — على سبيل المثال بفعل ضوء الأشعة فوق البنفسجية من الشمس — قد تتعطل هذه الآلات. إذا تراكمت النسخ المتوقفة، قد تتوقف الخلايا عن قراءة جيناتها بشكل صحيح، وهو أمر خطير بشكل خاص للخلايا العصبية وقد يؤدي إلى اضطرابات نادرة مثل متلازمة كوكساني. تكشف هذه الدراسة، بتفصيل، كيف تستشعر خلايانا هذه الآلات المحجوبة وتعيد تشغيلها أو تزيلها قبل أن تسبب ضرراً دائماً.
طريقة جديدة لمراقبة ازدحام المرور الخلوي
لفهم كيف تزيل الخلايا البوليمرازات المحجوبة، بنى الباحثون "كاميرا مرورية" زمانية للنسخ. استخدموا دواءً يسمح لجزيئات RNA بوليمراز II الموجودة بالاستمرار في الحركة لكن يمنع الجزيئات الجديدة من بدء الرحلة، ثم أحدثوا رقعة صغيرة من تلف الأشعة فوق البنفسجية داخل كل نواة خلية. بمتابعة وسم كيميائي محدد على الشكل النشط من البوليمراز، تمكنوا من مراقبة مدى سرعته في الاختفاء من منطقة التلف مقارنة بباقي الجينوم. بالتوازي، طوّروا اختباراً مرافقاً نظر إلى كمية البوليمراز النشط في مستخلصات الخلايا، مما أظهر ليس فقط متى غادرت البوليمرازات الحمض النووي، بل متى تم تفكيكها بواسطة نظام التخلص في الخلية.
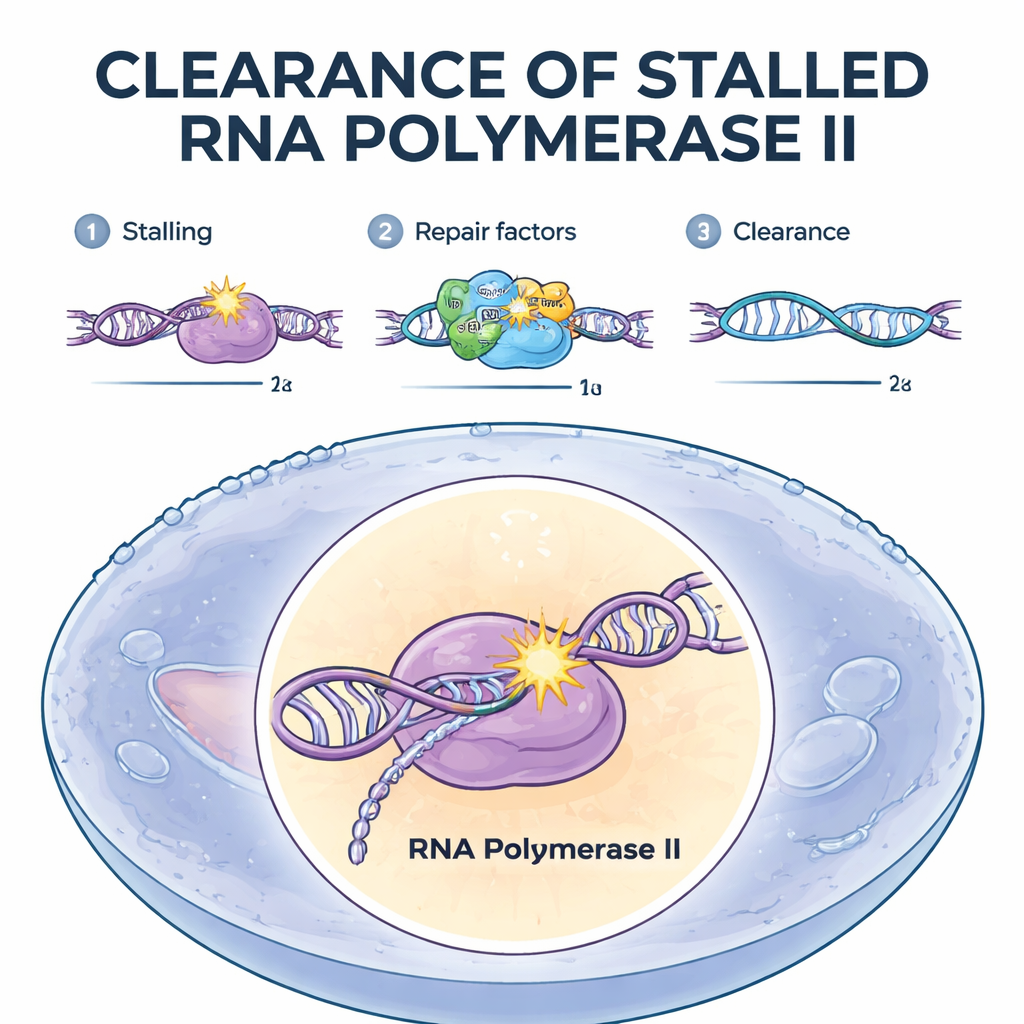
وسم الآلات المتوقفة للتمكن من إزالتها
ركز الفريق على الإصلاح المرتبط بالنسخ، وهو نظام إصلاح متخصص يصلح الآفات على الجينات المقروءة بنشاط. استخدموا مجموعة متطابقة من خطوط خلايا بشرية، كل منها تفتقر إلى عامل إصلاح مختلف. برزا بروتينان، CSB وCSA، كحراس حاسمين. عندما غاب أي منهما، تراكم بوليمراز II وبقي بعناد في مواقع التلف، وفشلت الخلية في تكسيره. كيميائياً حيوية، فشلت هذه الخلايا أيضاً في إرفاق وسم صغير من اليوبكويتين بموقع رئيسي على البوليمراز. بالمقابل، الخلايا التي تفتقر إلى بروتينات إصلاح لاحقة — تلك التي تقص وتستبدل الحمض النووي التالف — ظلت تزيل البوليمراز بشكل طبيعي. أظهر ذلك أن الوسم الأولي باليوبكويتين للبوليمراز المتوقف هو الزناد الحاسم لتقرير مصيره.
فريقان للتنظيف: واحد سريع وآخر احتياطي
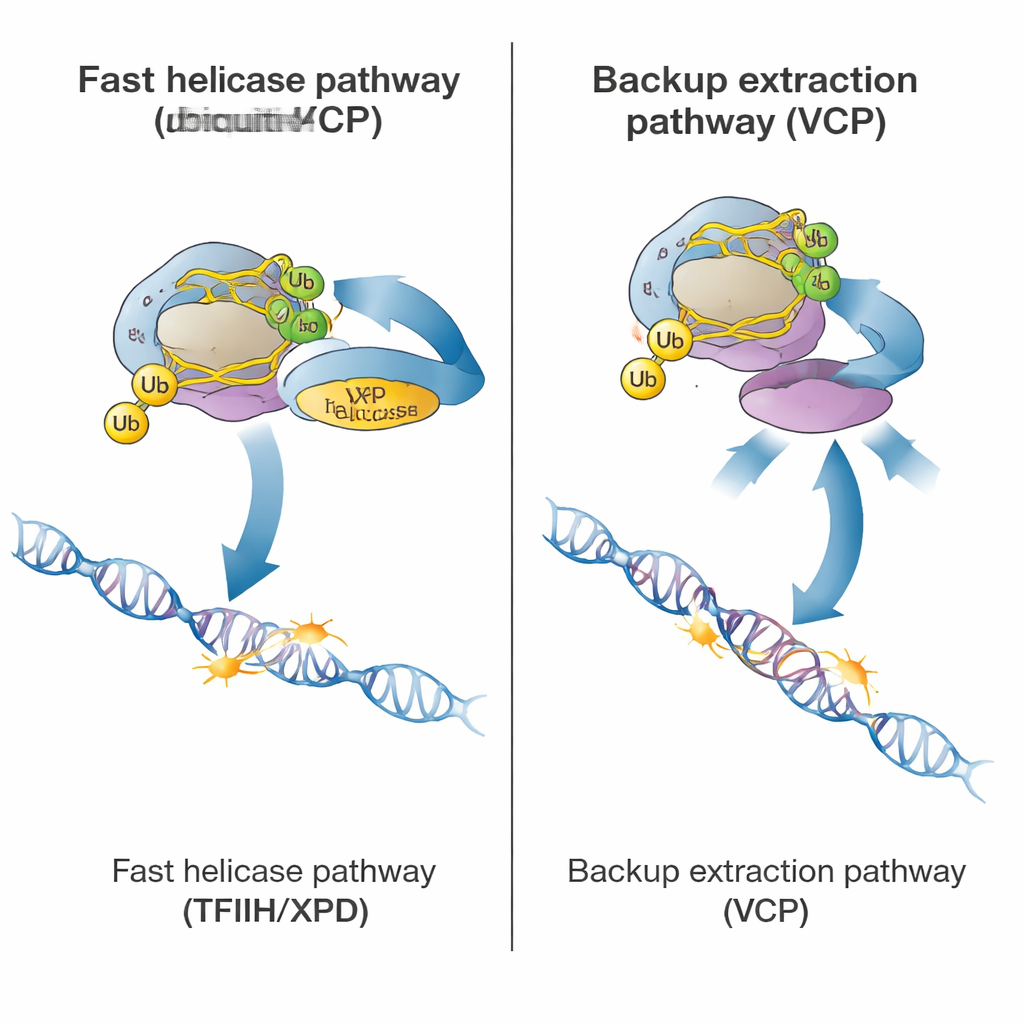
بمجرد وسم البوليمراز، تستطيع الخلية الاختيار بين طريقتين لإزالته. الطريق الأساسية والسريعة تعتمد على مركب إصلاح كبير يُسمى TFIIH، وبالأخص وحدة الهليكاز XPD فيه، التي تستخدم الطاقة لفك التفاف الحمض النووي. بروتينات مساعدة، بما في ذلك ELOF1 وUVSSA وSTK19، تجلب TFIIH إلى البوليمراز المتوقف وتضع XPD على الحمض النووي أمامه مباشرة. باستخدام اختبارات جديدة في خلايا مرضى تحمل طفرة تُعطل نشاط الهليكاز في XPD، أظهر المؤلفون أنه حين لا يستطيع XPD فك التفاف الحمض النووي، يبطئ إخلاء البوليمراز بشكل كبير، على الرغم من وجود بقية آلية الإصلاح. هذا يشير إلى أن الفعل الميكانيكي لسحب XPD هو ما عادةً "يهز" البوليمراز ليُفكك عن الآفة حتى تتمكن إنزيمات الإصلاح من الوصول إلى المكان التالف.
خطة ب بطيئة لكن أساسية
كشفت الدراسة أيضاً عن مسار طوارئ أبطأ لإزالة البوليمراز المتوقف. تعتمد هذه المسار على VCP (المعروف أيضاً باسم p97)، وهو بروتين يتعرف على علامات اليوبكويتين ويمكنه اقتلاع البروتينات قسراً من الكروماتين. في الخلايا السليمة التي يعمل فيها TFIIH بالكامل، كان حجب VCP له تأثير طفيف فقط. لكن في الخلايا التي كان فيها TFIIH مفقوداً أو موضوعة بشكل خاطئ أو ذات XPD معطل، أصبح إخلاء البوليمراز يعتمد إلى حد كبير على VCP. في هذه الحالات، كان بإمكان VCP سحب البوليمراز المسمى بعيداً عن الحمض النووي، حتى عندما لم يتمكن الإصلاح الطبيعي من التقدم. والأهم أن هذا الطريق الاحتياطي ظل يعتمد على بعض وسم اليوبكويتين، مما يفسر سبب فشل الخلايا التي تفتقر إلى CSB أو CSA — وبالتالي تفتقر إلى علامات اليوبكويتين — في كل من المسار الرئيسي والمسار الاحتياطي.
لماذا هذا مهم للصحة والمرض
عند تجميع النتائج، ترسم هذه الدراسة برنامج أمان هرمي تستخدمه الخلايا كلما اصطدم إنزيم RNA بوليمراز II بتلف في الحمض النووي. أولاً، يحدد CSB وCSA الآلة المتوقفة بعلامة اليوبكويتين. إذا كان كل شيء يعمل بشكل صحيح، يقوم TFIIH وهليكازه XPD بعد ذلك بإخراج البوليمراز بسرعة حتى تُقتطع الآفة ويُصلح الحمض النووي. إذا لم يستطع TFIIH أداء عمله، يتدخل VCP لاستخراج البوليمراز وإرساله للتفكيك، مانعاً تراكمه المعيق للتعبير الجيني حتى وإن ظل تلف الحمض النووي قائماً. يساعد هذا الإطار في تفسير سبب تسبب العيوب الوراثية في CSB أو CSA بمشاكل عصبية شديدة بشكل خاص: بدون وسم اليوبكويتين، تفقد الخلايا كل من المسار الرئيسي المدفوع بالإصلاح والمسار الاحتياطي للاقتلاع، تاركة البوليمراز المتوقفة عالقة على الجينات التالفة ويظل النسخ محظوراً باستمرار.
الاستشهاد: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
الكلمات المفتاحية: إصلاح الحمض النووي المرتبط بالنسخ, إنزيم RNA بوليمراز II, الضرر الناتج عن الأشعة فوق البنفسجية, يوبيكويتين البروتين, متلازمة كوكساني