Clear Sky Science · ar
نمذجة الأيض الخاص بالأنسجة في ذبابة الفاكهة تكشف عن اضطراب أيضي في العضلات ناتج عن نظام غذائي عالي السكر على مستوى التفاعلات والمسارات
لماذا تهم هذه الدراسة على ذبابة الفاكهة صحة الإنسان
الإفراط في استهلاك السكر يمكن أن يجهد قدرة الجسم على إدارة الوقود، مما يساهم في النهاية في الإصابة بمرض السكري من النمط الثاني. تستخدم هذه الدراسة ذبابة الفاكهة لكشف، بتفصيل ملحوظ، كيف تتعامل الأنسجة المختلفة مع الأيض وكيف يعرقل النظام الغذائي عالي السكر وظيفة العضلات. وبما أن الذباب يتشارك مع البشر عدداً كبيراً من الجينات والأعضاء الأيضية، فإن هذه النتائج تساعد على تفسير ما قد يخطئ في عضلاتنا عند التعرض الطويل للوفرة السكرية.
رسم خريطة الأيض نسيجاً نسيجاً
أجسامنا، مثل أجسام ذبابة الفاكهة، تتألف من أنسجة تؤدي أدواراً أيضية مختلفة تماماً: تحرق العضلات الوقود، يخزن النسيج الشحمي الوقود، يعالج القناة الهضمية الطعام، وهكذا. بدلاً من قياس كل إنزيم مباشرة، بنى الباحثون «خرائط» أيضية واسعة النطاق — تُسمى نماذج أيضية على مستوى الجينوم — لـ 32 نسيجاً متميزاً في الذبابة. جمعوا شبكة تفاعلات كيميائية منقَّحة مع بيانات التعبير الجيني على مستوى الخلية الواحدة، التي تشير إلى أي الجينات الأيضية مفعلة في كل نسيج. أتاح لهم ذلك مقارنة عدد التفاعلات والوسائط والجينات النشطة في كل شبكة خاصة بالنسيج ولرؤية أي المسارات تُبرز في العضلات، والنسيج الشحمي، والقناة الهضمية، وأنواع الخلايا العصبية المختلفة.
وظائف وقود مميزة للأعضاء المختلفة
أظهر المقارنة «شخصيات» أيضية واضحة عبر الأنسجة. احتوى النسيج الشحمي والخلايا الدهنية الخاصة بالذبابة — المعادلات البشرية للدهون والكبد — على أغنى مجموعة من التفاعلات، خصوصاً تلك التي تحرق الدهون عبر بيتا-أكسدة. في المقابل، لم تمتلك العضلات أكبر شبكة، لكنها امتلكت أعلى نسبة من التفاعلات التي تنقل المواد داخل وخارج الخلايا، مما يشير إلى أن العضلات تمثل محوراً رئيسياً لتبادل الوقود واللبنات البنائية مع بقية الجسم. كما تحقق العلماء فيما إذا كانت المسارات المتوقعة تتطابق مع أنماط الوسائط الحقيقية المقاسة في مناطق جسمية مختلفة. باستخدام قياسات موجهة للأيض، حللوا مئات الجزيئات الصغيرة من رؤوس الذباب والصدر والقناة الهضمية والبطن، ثم فحصوا ما إذا كانت المسارات الغنية في البيانات تتداخل مع تلك المتوقعة بواسطة النماذج. في العضلات والنسيج الشحمي، كان التطابق قوياً، مما يعطي ثقة بأن النماذج الخاصة بالأنسجة التقطت بيولوجيا حقيقية أفضل من الاعتماد على التعبير الجيني وحده.
ما الذي يفعله النظام الغذائي عالي السكر بتدفُّق الوقود في العضلات
بوجود نموذج عضلي تم التحقق منه، حاكى الفريق ما يحدث عندما تُطعَم الذباب نظاماً غذائياً عالي السكر طويل الأمد، نموذج راسخ لمرض السكري من النمط الثاني. قيدوا النموذج باستخدام خواص معروفة للعضلات السكرية، مثل انخفاض امتصاص الغلوكوز وضعف نشاط دورة الطاقة المركزية في الميتوكوندريا. أظهرت تحليلات «التدفق» الحسابية — حسابات السرعات الممكنة للتفاعلات — انخفاضات واسعة في التفاعلات التي تعتمد على زوج الاختزال–الأكسدة NAD وNADH، الجزيئات التي تنقل الإلكترونات والضرورية لإنتاج الطاقة. على وجه الخصوص، تباطأت تفاعلات مسار حرق السكر المركزي، التحلل السكرِي (glycolysis)، بما في ذلك التفاعلات التي يحفزها الإنزيم GAPDH. تنبأ النموذج أيضاً بانخفاض بنحو ربع قدرة العضلة على إنتاج NADH إجمالاً، ما يوحي بانخفاض في توازن الاختزال–الأكسدة. أكدت القياسات المباشرة في عضلات صدر الذباب أن نسبة NAD إلى NADH فعلاً انخفضت تحت النظام الغذائي عالي السكر.
تتبُّع السكر المعلم والبروتينات المؤكسدة
للتحقق مما إذا كانت اختناقات المرور المتوقعة تحدث فعلاً في الحيوانات الحية، أطعم الباحثون الذباب نظاماً غذائياً عالي السكر يحتوي على غلوكوز معلم كلياً بكربون-13 ثم تتبعوا مكان ذهاب الكربون المعلم. وجدوا أن الوسطيات المبكرة في التحلل السكري الموجودة قبل GAPDH تراكمت، بينما انخفضت النواتج اللاحقة وأجزاءها المعلمة، ما يشير إلى تباطؤ حقيقي عند هذه النقطة وما بعدها. وبالمثل، انخفضت مساهمات كربون الغلوكوز في دورة الطاقة المركزية. في الوقت نفسه، أظهر بروتيوميات الاختزال–الأكسدة — طريقة تكشف التغييرات التأكسدية على أحماض أمينية محددة في البروتينات — زيادة في تأكسد العديد من إنزيمات التحلل السكري، بما في ذلك مواقع متعددة على GAPDH. عبر التحلل السكري، كانت الإنزيمات التي حملت تعديلات أكسدية أكثر تميل إلى إظهار انخفاضات أكبر في التدفق المتوقع، على الرغم من أن مستوياتها البروتينية الإجمالية ظلت في الغالب دون تغيير. يشير ذلك إلى أن التلف الكيميائي الناتج عن الإجهاد التأكسدي، بدلاً من فقدان كمية الإنزيم، هو محرك رئيسي لضعف معالجة السكر في العضلة.
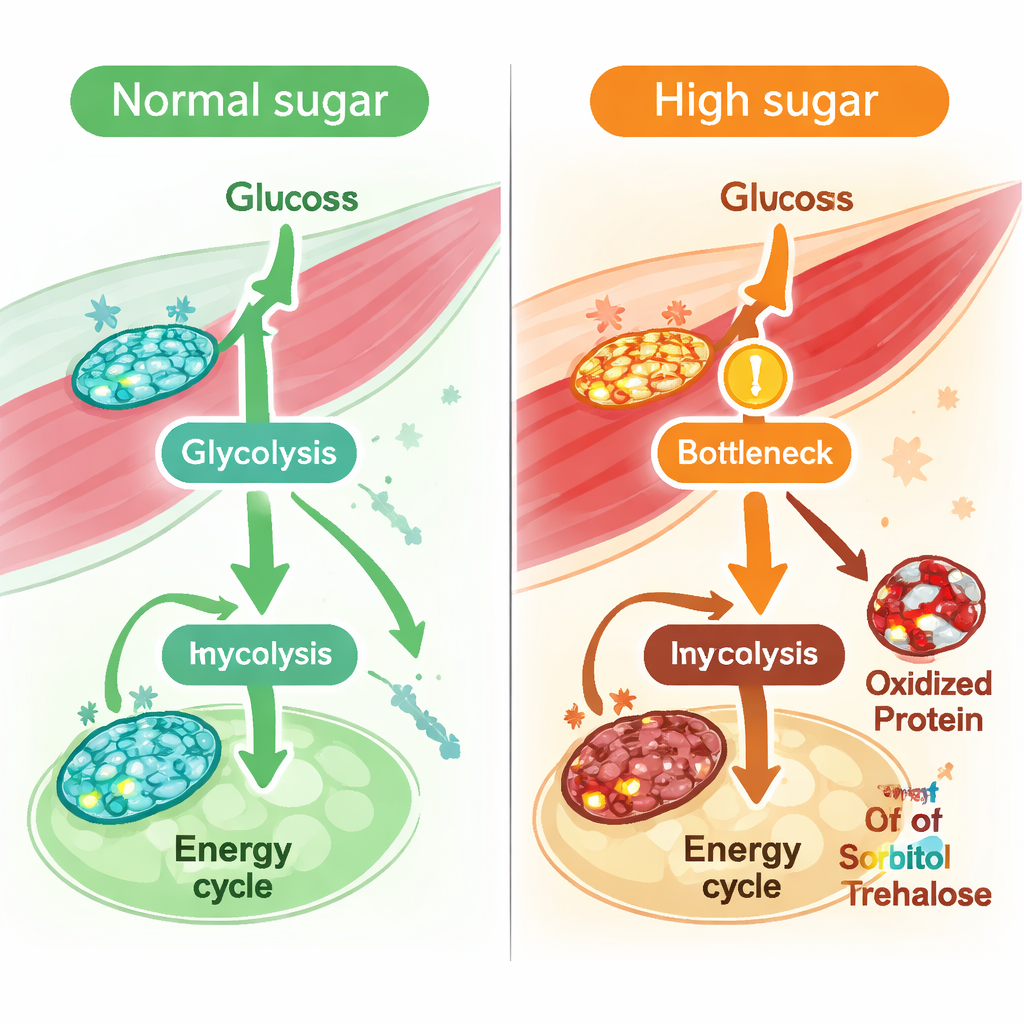
مشاكل خفية في تعامل الفركتوز والسكروز
عند النظر أبعد من التفاعلات الفردية، وسّط الفريق التدفقات عبر المسارات الكاملة ليرى أيها الأكثر اضطراباً بفعل السكر العالي. أظهر التحلل السكري، ودورة الطاقة، والفوسفوريلات المؤكسدة جميعها تراجعات، لكن أحد أقوى الانخفاضات المتوقعة كان في أيض الفركتوز. دعمت ملفات الوسائط في العضلات هذه الفكرة: ارتفعت مستويات السوربيتول والتريهالوز/السكروز، وأظهر إنزيم رئيسي يحول التريهالوز إلى غلوكوز، التريهالاز، نشاطاً متوقعاً مخفضاً وزيادة في التأكسد عند بقايا ميثيونين حساسة. معاً، تشير هذه النتائج إلى اضطراب أوسع في كيفية تعامل العضلات مع السكريات الغذائية — وخصوصاً الوقود المشابه للفركتوز والمشتق من السكروز — تحت التعرض المزمن للسكر.
ماذا يعني هذا لفهم مرض السكري
بعبارات بسيطة، تُظهر هذه الدراسة أن الإفراط في السكر لا يكتفي بتحميل الدم بالسكر؛ بل يعيد بهدوء تشكيل كيفية توجيه وحرق خلايا العضلات للوقود. من خلال بناء خرائط أيضية مفصلة خاصة بالأنسجة لذبابة الفاكهة ومطابقتها مع ميتابولوميات، وتتبع النظائر، وبروتيوميات الاختزال–الأكسدة، يكشف الباحثون أن السكر العالي يدفع الإجهاد التأكسدي، ويؤكسد إنزيمات تحلل السكر الرئيسية مثل GAPDH، ويبطئ تفكيك السكر، ويعطل المسارات المرتبطة بالفركتوز. توفر هذه الرؤى، التي نُشرت في كائن نموذجي سهل التعامل معه، إطار عمل قوي لتحديد التفاعلات والمسارات التي قد تكون الأهم لحمايتها أو استعادتها في عضلة الإنسان للوقاية أو العلاج من مرض السكري من النمط الثاني.
الاستشهاد: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
الكلمات المفتاحية: أيض ذبابة الفاكهة, نماذج أيضية خاصة بالأنسجة, نظام غذائي عالي السكر, تحلل السكر في العضلات, تنظيم الاختزال–الأكسدة