Clear Sky Science · ar
تجديد ميكانيكي للخلايا الجذعية المسنة والعظام المتقدمة في العمر عبر إعادة تشكيل الكروماتين
لماذا الحفاظ على عظام شابة مهم
مع تقدمنا في العمر، تفقد عظامنا تدريجيًا قوتها، فتصبح أنحف وأكثر هشاشة. هذا يزيد من خطر الكسور وفقدان الاستقلالية والألم المزمن. تركز معظم العلاجات الحالية على أدوية تبطئ تحلل العظام أو تضيف معادن، لكنها لا تصلح مباشرة شيخوخة الخلايا الجذعية المسؤولة عن بناء العظام. يستكشف هذا البحث زاوية مختلفة: استخدام قوى فيزيائية محكمة الضبط — بدلاً من الأدوية — لـ "تجديد" الخلايا الجذعية البانية للعظام وتحسين صحة العظام واللياقة العامة لدى الفئران المسنة.
عندما يتقدم بناؤو العظام في السن
في أعماق عظامنا تعيش خلايا جذعية نخاعية مزنخية، وهي البنّائون الرئيسيون القادرون على التحول إلى خلايا مكونة للعظم. مع التقدم في العمر، تقل قدرة هذه الخلايا على الانقسام وتكوّن العظم، وتظهر عليها علامات شيخوخة خلوية نموذجية مثل تلف الحمض النووي وإشارات التهابية. قارن الباحثون خلايا من متبرعين شباب وكبار في السن ووجدوا أن الخلايا المسنة لم تكن مختلفة كيميائيًا فحسب — بل كانت أضعف ميكانيكيًا. كانت تولد قوة سحب داخلية أقل، وكانت هياكلها الداخلية أكثر رخاوة، وأظهرت مشاكل في نقل الإشارات الميكانيكية إلى نواة الخلية. في أنسجة العظام من فئران مسنة ظهر تدهور مماثل: تقلصت شبكة العظم الإسفنجي، وانخفضت بروتينات الإشارة الميكانيكية الأساسية، وارتفعت مؤشرات الشيخوخة.
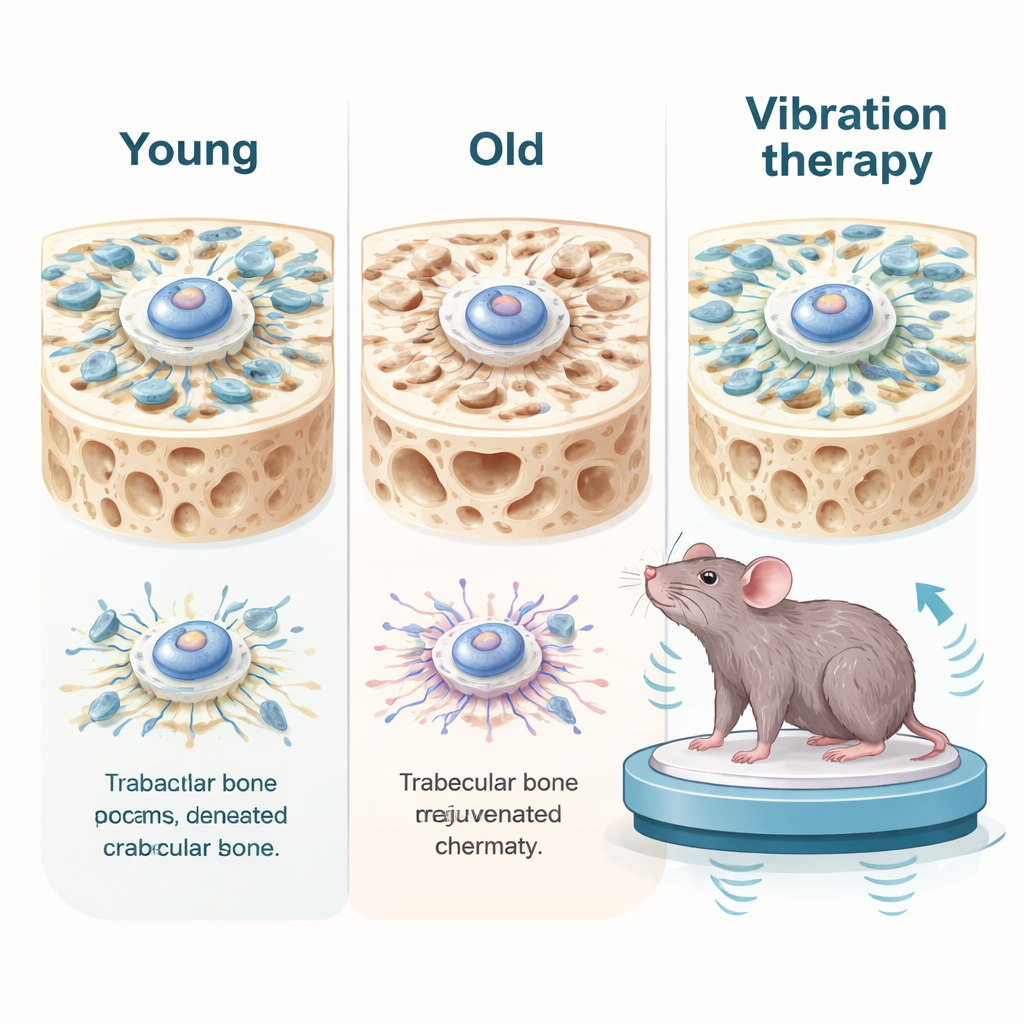
سحب الخلايا برفق نحو الشباب
بعد ذلك تساءل الفريق عما إذا كان استعادة القوة الميكانيكية يمكن أن يعكس هذه السمات المرتبطة بالشيخوخة. في الأطباق، طبقوا تمددًا طفيفًا على الخلايا الجذعية المسنة أو استخدموا دواءً يعزز نشاط المحركات الجزيئية. عززت هذه المعالجات قوى السحب الخلوية وحسّنت تنظيم الهيكل الداخلي. بشكل لافت، بدأت الخلايا المسنة تبدو وتتصرف بشكل أكثر شبابًا: انخفضت علامات الشيخوخة، تراجع تلف الحمض النووي، وتكاثرت الخلايا بسهولة أكبر. وناظرًا لذلك، عندما لينو البيئة تحت خلايا شابة أو أضعفوا كيميائيًا آلية التقلص لديها، انزلقت الخلايا إلى حالة شبيهة بالشيخوخة، تباطأت وفعّلت علامات الشيخوخة حتى في مادة هلامية ثلاثية الأبعاد تحاكي العظم.
كيف تتواصل القوة مع الجينات
لفهم كيف يمكن للقوى الفيزيائية أن تغيّر سلوك الخلية بعمق، توجه الباحثون إلى الكروماتين — الصيغة المعبأة للحمض النووي داخل النواة. في الخلايا الجذعية المسنة كان الكروماتين أكثر تكثفًا وأقل وصولًا، مما يصعّب تشغيل الجينات المفيدة. أدى استعادة القوة الميكانيكية إلى استرخاء الكروماتين موضعيًا، وزيادة العلامات الكيميائية المرتبطة بالحمض النووي المفتوح والنشط. باستخدام اختبار واسع النطاق لوصولية الكروماتين في الجينوم، وجد الفريق أن التحفيز الميكانيكي اللطيف فتح مناطق قريبة من جينات مشاركة في السيطرة على الشيخوخة. برزت جينة واحدة، تسمى FOXO1، كحساسة بشكل خاص للقوة. عندما زادت القوة، أصبحت منطقة FOXO1 أكثر انفتاحًا، ارتفع نشاطها، وقلّت الشيخوخة في الخلايا. إلغاء عمل FOXO1 أزال فوائد التحفيز الميكانيكي، ما كشف عنها كمفتاح يربط الإجهاد الفيزيائي ببرامج وراثية للمرونة والإصلاح.
البحث عن نقطة التوازن للعلاج الميكانيكي
اختبر الباحثون بعد ذلك التحفيز الميكانيكي في فئران حية. وُضعت الحيوانات المسنة على منصة اهتزاز منخفض الشدة لجلسات يومية قصيرة على مدار شهر، بينما عومل آخرون بإزالة تحميل أرجلهم الخلفية عبر تعليق الذيل، محاكاةً لقصور نشاط متطرف. في الفئران المسنة عزز الاهتزاز اللطيف إشارات ميكانيكية في العظام، خفض علامات الشيخوخة والالتهاب، وأعاد جزئيًا بناء شبكة العظم الإسفنجي. كما حسّن قوة المصّ، وتحمل التمارين، ومهام مرتبطة بالذاكرة، وخفّض الالتهاب في الدم والكبد والكليتين. مع ذلك، عندما طُبق الاهتزاز بشكل مستمر بدون أيام راحة، اختفت الفوائد وعاودت النتائج الانعكاس: ساءت بنية العظم، ازداد تلف الحمض النووي، وارتفع الالتهاب. في دراسات الخلايا، تسبب التمدد الشديد أو المتكرر بتكسر الحمض النووي ودفع الخلايا مرة أخرى نحو الشيخوخة، مما يبين أن القوة الميكانيكية قد تشفي أو تضر اعتمادًا على الجرعة.
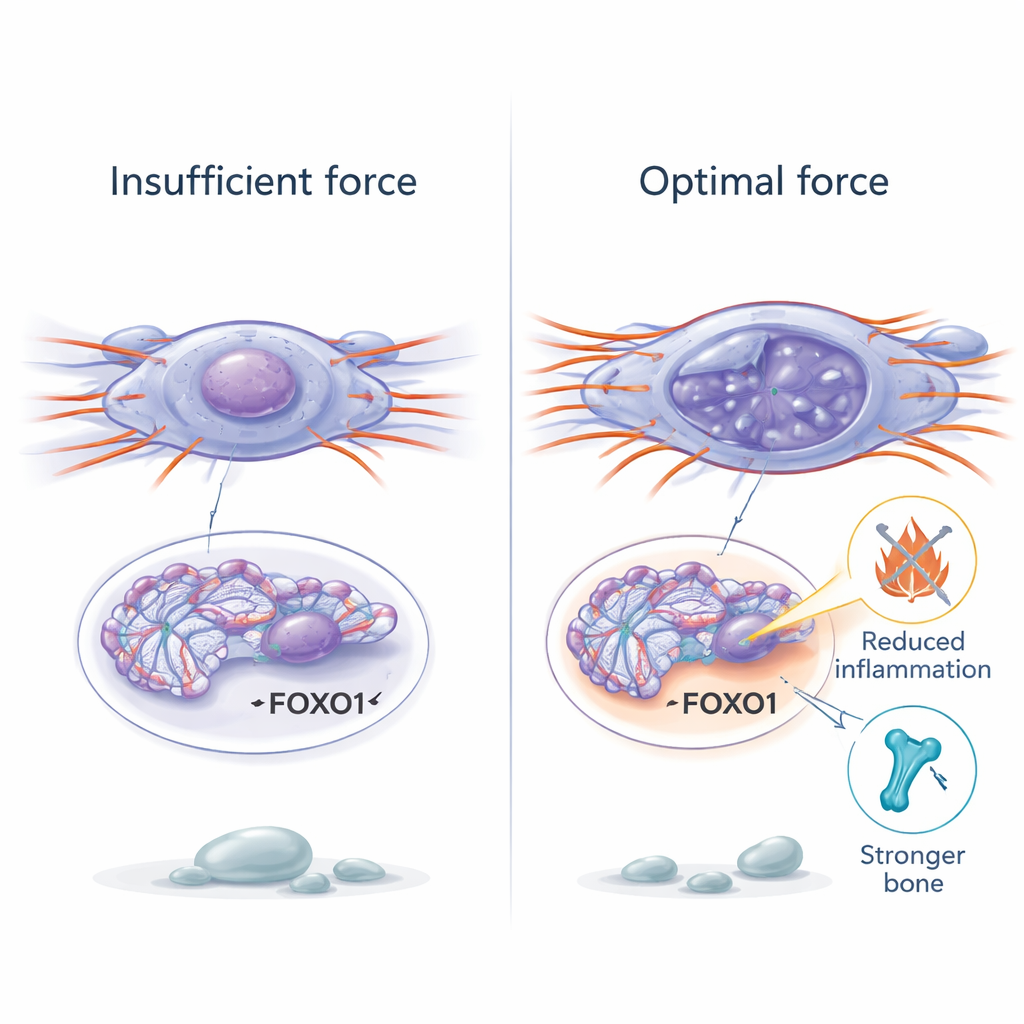
من محاكيات التمرين إلى علاجات مستقبلية
لغير المتخصص، الرسالة المركزية هي أن خلايانا لا تستجيب للهرمونات والمواد الكيميائية فقط — بل "تستمع" أيضًا عن كثب إلى القوى الفيزيائية. في هذا العمل يظهر المؤلفون أن التحفيز الميكانيكي المعتدل والمضبوط جيدًا يمكن أن يوقظ خلايا العظام المسنة، ويفتح برامج جينية واقية مثل FOXO1، ويعيد بناء العظام الضعيفة، ويهدئ الالتهاب المزمن في الفئران المسنة. في المقابل، يؤدي القليل جدًا أو الكثير جدًا من القوة إلى تسريع تدهور الخلايا. تلمّح هذه النتائج إلى أن علاجات ميكانيكية مصممة بعناية — ربما نظم تمرين محددة أو أجهزة اهتزاز آمنة — قد تكمل يومًا ما الأدوية في الحفاظ على صحة العظام، وربما أنسجة أخرى، لفترة أطول.
الاستشهاد: Liu, X., Ye, Y., Li, Z. et al. Mechanical rejuvenation of senescent stem cells and aged bone via chromatin remodeling. Nat Commun 17, 1684 (2026). https://doi.org/10.1038/s41467-026-68387-3
الكلمات المفتاحية: شيخوخة العظام, التحفيز الميكانيكي, تجديد الخلايا الجذعية, إعادة تشكيل الكروماتين, FOXO1