Clear Sky Science · ar
القص الدقيق لتكرارات GGC الموسعة في NOTCH2NLC عبر CRISPR/Cas9 لعلاج داء الشمول النووي العصبي
تحرير الحمض النووي لمواجهة اضطراب دماغي غامض
داء الشمول النووي العصبي (NIID) هو اضطراب دماغي نادر لكنه مدمر قد يسبب الخرف ومشكلات حركية، وقد يؤدي أحياناً إلى الوفاة المبكرة. لا وجود لعلاج شافٍ حتى الآن. تستقصي هذه الدراسة ما إذا كان بإمكان أداة تحرير الجينات القوية CRISPR أن تقص قطعة صغيرة لكنها سامة من الحمض النووي تقف خلف NIID، مما يقدم لمحة عن كيفية إمكانية إعادة كتابة جينومنا مستقبلاً لمواجهة أمراض الدماغ. 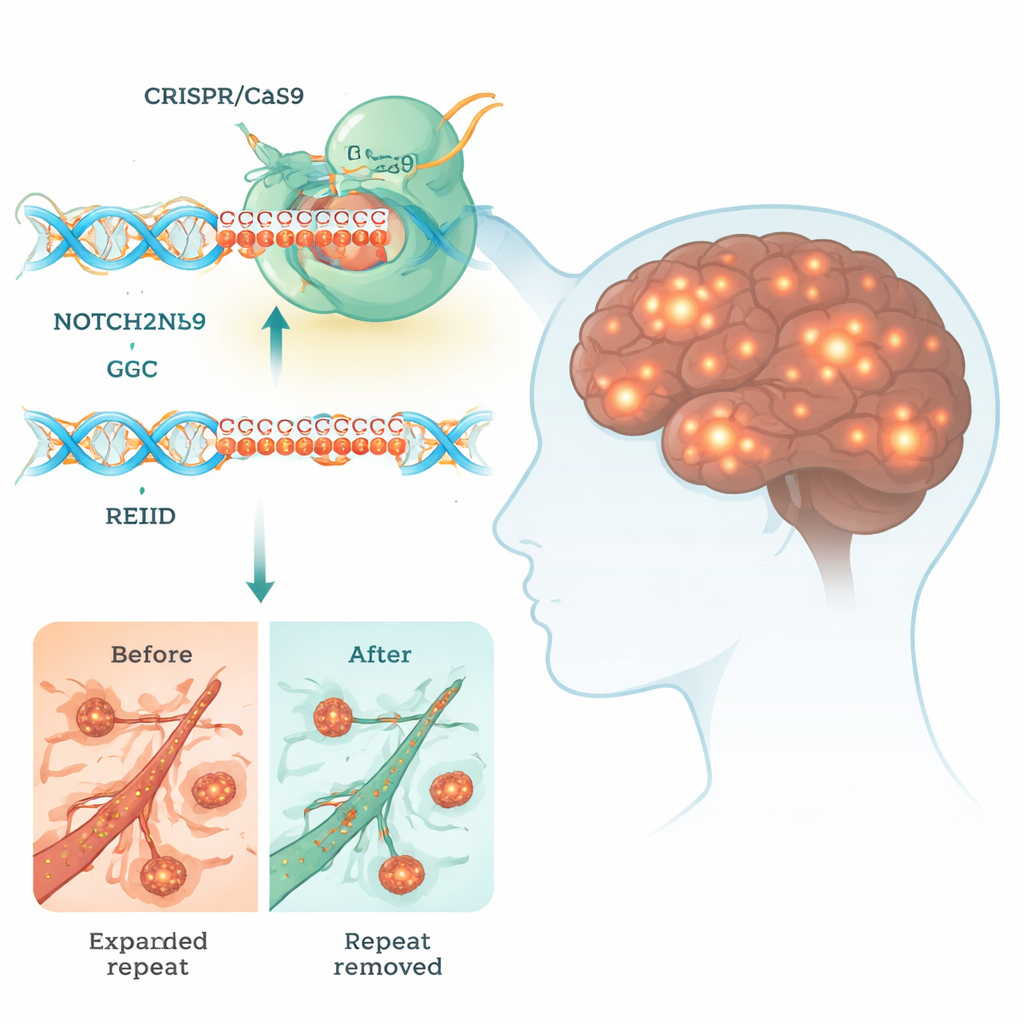
مذنب جيني مخفي
العديد من اضطرابات الدماغ الوراثية ناجمة عن مقاطع قصيرة من الحمض النووي التي تكبرت إلى ما وراء طولها الطبيعي. في NIID، المشكلة هي امتداد مفرط لوحدات ثلاثية الحروف، "GGC"، في جين يسمى NOTCH2NLC. رغم أن هذا الامتداد يقع في منطقة لا تُشفّر مباشرة لبروتين تقليدي، فإن آليات الخلية قد تقرأه وتنتج سلاسل جليسين متعددة غير طبيعية (polyG). تتجمع هذه السلاسل اللاصقة على شكل عقيدات داخل نواة الخلايا العصبية وأنسجة أخرى، معطلة عمليات حيوية مثل إنتاج الطاقة ومعالجة الحمض النووي الريبوزي وحركة الجزيئات بين النواة والسيتوبلازم.
تحدي الجراحة الجزيئية الدقيقة
تصميم علاج بتحرير الجينات لـ NIID صعب على نحو غير معتاد لأن NOTCH2NLC له عدة جينات شقيقة متقاربة ضرورية لتطور الدماغ البشري. إذا قطع CRISPR الجين الخاطئ فقد يسبب ضرراً أكبر من النفع. فحص الباحثون بعناية الحمض النووي المحيط بتكرار GGC ووجدوا اختلافات طفيفة في التسلسل تميّز NOTCH2NLC عن أقاربه. صمموا بعد ذلك أزواجاً من حمضيات الإرشاد الدليلي (guide RNAs) لوجيهزوا إنزيم Cas9 "المقص الجزيئي" لقطع موقعين قبل وبعد التكرار الموسع. تتيح هذه الاستراتيجية ذات القطعين لجهاز إصلاح الخلية إزالة الجزء السام مع ترك بقية عائلة الجينات سليمة.
من خلايا في طبق إلى خلايا عصبية مشتقة من مريض
اختبر الفريق أولاً تصميم CRISPR في خلايا بشرية قياسية وفي خلايا مُهندَسة لتحمل تكرار NOTCH2NLC كبير. في هذه النماذج، أزال المحرر التكرار بكفاءة وانخفضت مستويات تجمعات polyG بنحو النصف أو أكثر. ثم انتقلوا إلى خلايا جذعية متعددة القدرات المهندسة من ضروب (iPSCs) مأخوذة من مريض بـ NIID وحوّلوا هذه الخلايا إلى خلايا سلف عصبية، وهي مرحلة مبكرة من خلايا الدماغ. باستخدام CRISPR، حذفوا إما التكرار الموسع أو استبدلوه بنسخة بطول طبيعي. أظهرت تحليلات الحمض النووي والتسلسل الجينومي الكامل أن التحرير كان دقيقاً جداً مع أدلة قليلة على قصوص غير مرغوبة، وأن الخلايا المعدلة استمرت في الانقسام والنضج بشكل طبيعي. 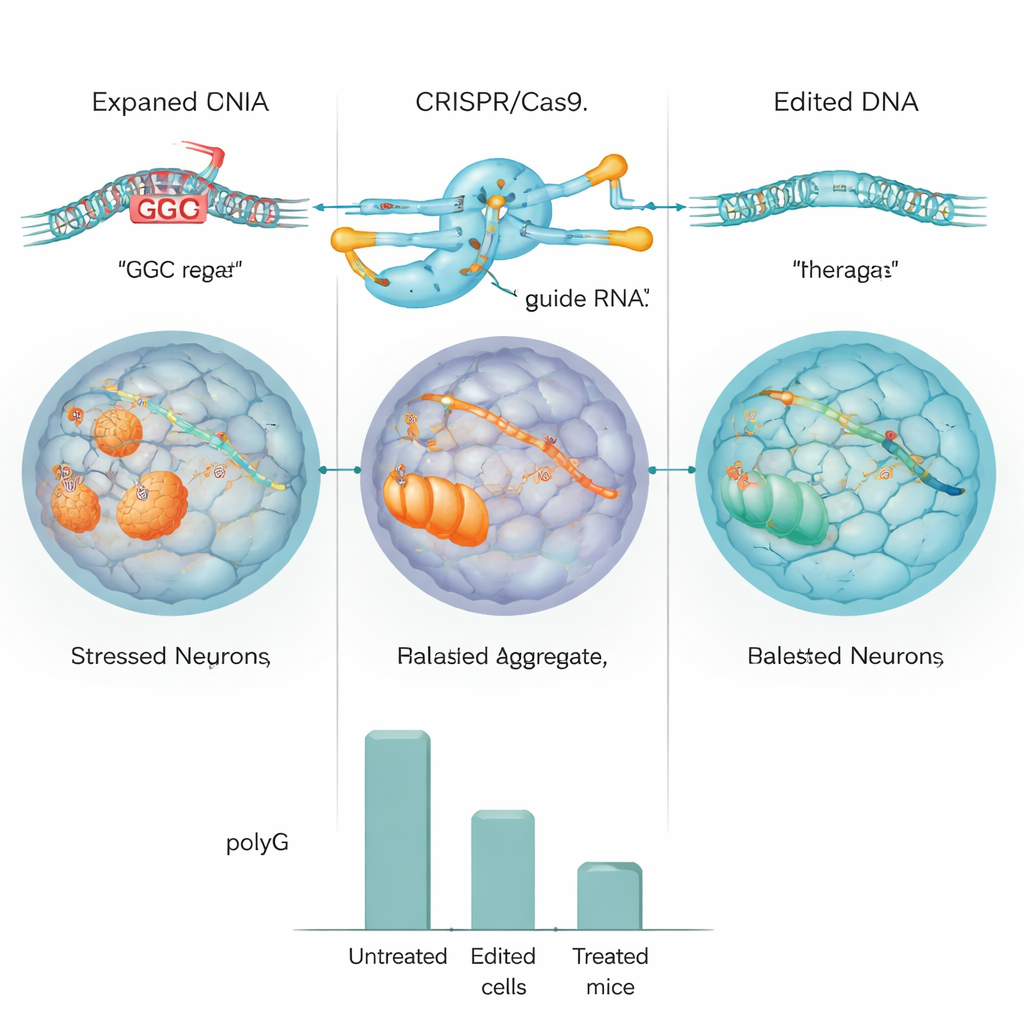
إنقاذ الدماغ والجسم في نموذج فأري
للاختبار ما إذا كان هذا النهج يستطيع فعلاً تحسين المرض، لجأ الباحثون إلى فئران مُهندَسة لتحمل تكرار NOTCH2NLC البشري وتطوّر سمات شبيهة بـ NIID، بما في ذلك الشمول النووي والمشكلات الحركية وقصر العمر. حزموا نظام CRISPR في فيروس معدل يمكنه الانتشار في جميع أنحاء الدماغ بعد حقنة بسيطة في مجرى الدم للفئران حديثة الولادة. في الحيوانات المعالجة أزيل التكرار الموسع بنجاح في أنسجة الدماغ. نتيجة لذلك، هبطت مستويات polyG السامة بشكل حاد، تحسنت مؤشرات صحة الخلايا العصبية، وتراجع التنشيط غير الطبيعي للخلايا الداعمة في الدماغ. أظهرت اختبارات السلوك أن الفئران المعالجة تحركت أكثر، حافظت على توازن أفضل، وعاشت مدة أطول من أشقائها غير المعالجين. لوحظت فوائد مماثلة في القلب، الذي يتراكم فيه polyG أيضاً في هذا النموذج.
ماذا يعني هذا للعلاجات المستقبلية
بالنسبة للقارئ العام، الرسالة الأساسية هي أن NIID يبدو مدفوعاً إلى حد كبير بتكرار DNA واحد محدد وممتد، وأن إزالة ذلك التكرار بدقة يمكن أن تعكس العديد من علامات المرض في الخلايا وفي الفئران. هذه العملة لا تتحول حالياً إلى علاج جاهز للاستخدام البشري: لا يزال على الباحثين تحسين السلامة على المدى الطويل، وتحسين طرق التوصيل، والاختبار في حيوانات أكبر وأكثر شبهاً بالإنسان. لكن الدراسة تقدم دليلاً قويّاً على المفهوم بأن تحرير الجين المستهدف بعناية يمكنه كبت تكرار سام مع إبقاء الجينات القريبة سالمة. قد تُكيّف هذه الاستراتيجية ذات يوم ليس فقط لـ NIID، بل أيضاً لاضطرابات دماغية وعضلية أخرى ناجمة عن توسعات تكرارية مماثلة.
الاستشهاد: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
الكلمات المفتاحية: تحرير الجينات CRISPR, داء الشمول النووي العصبي, اضطرابات توسع التكرارات, NOTCH2NLC, اعتلال عصبي تنكسي