Clear Sky Science · ar
تنظّم Tmem110 شكل TRPML1 للحفاظ على التوازن داخل الإندو-لايسوزومي ومنع تسرب حمض الميتوكوندريا النووي ومعالجة الحمض النووي الذاتي المرضية
لماذا يهم تسرب الحمض النووي بعد الإصابة
عندما نتعرض لصدمات شديدة، مثل ضربة عنيفة في الرأس، لا يقتصر الضرر على موقع الإصابة فحسب. كثير من المرضى يصابون برد فعل خطير يشمل الجسم بأكمله، حيث تبدأ الرئتان والكبد والكليتان وأعضاء أخرى في الفشل. تكشف هذه الدراسة كيف تتواصل بنى صغيرة داخل الخلايا — اللايسوزومات والميتوكوندريا وأجهزة استشعار المناعة — لتقرر ما إذا كان الجسم سينظف الحطام بهدوء أم سيدخل في هجوم مناعي موجه ضد نفسه. فهم هذا النظام الخفي للتنظيف قد يفتح طرقاً جديدة لمنع فشل الأعضاء بعد الصدمة وعلاج أمراض المناعة الذاتية والالتهابية.
من إصابة الرأس إلى أزمة تصيب الجسم كله
يمكن للإصابة الدماغية الرضّية (TBI) أن تثير عاصفة التهابية قوية تُعرف بمتلازمة اختلال أعضاء متعددة (MODS)، لكن كان غير واضح كيف ينتقل الضرر من الدماغ إلى الأعضاء البعيدة. ركز المؤلفون على الخلايا المناعية الأحادية والبلاعم، وهي خلايا تتجول في الدم والأنسجة وتعمل كجامعي نفايات محترفين. بعد TBI، تموت خلايا بطرق خارجة عن السيطرة وتطلق ميتوكوندريات كاملة — مصانع طاقة صغيرة تحمل حمضها النووي الخاص — إلى الدورة الدموية. يبدو الحمض النووي للميتوكوندريا (mtDNA) مريبًا للجهاز المناعي ويشبه حمض البكتيريا، ما قد يشغّل دفاعات قوية شبيهة بمقاومة الفيروسات إذا لم يُزال بسرعة. عادة، تبتلع الخلايا هذه الميتوكوندريات المتشردة داخل حويصلات حمضية تُدعى لايسوزومات، حيث تقصم الإنزيمات الحمض النووي قبل أن يتسرب إلى سائِل الخلية. 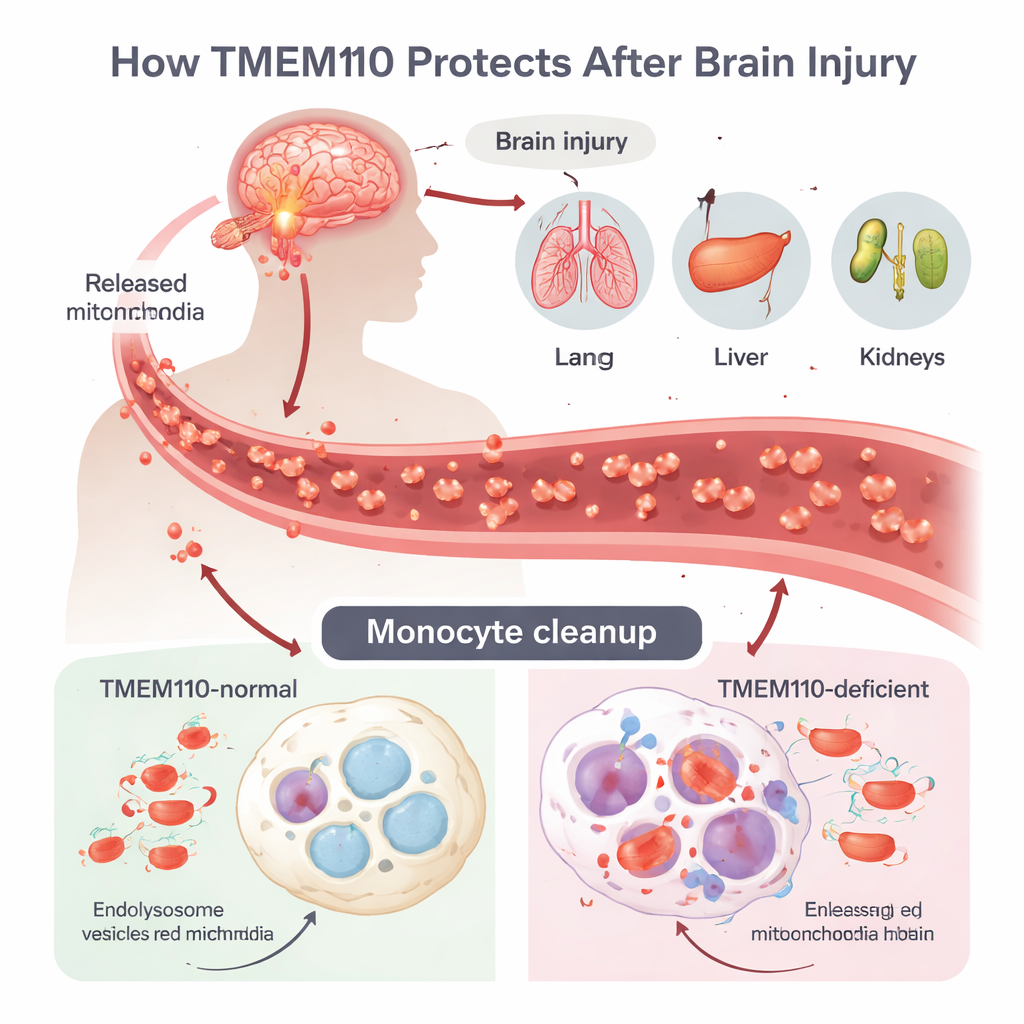
بروتين حارس يحافظ على ثبات اللايسوزومات
حددت المجموعة بروتين TMEM110، الذي يعبر غشاء الشبكة الإندوبلازمية (شبكة غشائية خلوية رئيسية)، باعتباره حارسًا مهمًا في هذه العملية. باستخدام فئران مُهندَسة وراثيًا نفت TMEM110 فقط في الخلايا الأحادية والبلاعم، أنشأوا نموذجًا محكمًا لإصابة الدماغ. بالمقارنة مع الفئران الطبيعية، طورت الحيوانات التي تفتقر إلى TMEM110 مستويات أعلى بكثير من إنترفيرونات النوع الأول — جزيئات إشارية مضادة للفيروسات قوية — في دمها والسائل الدماغي الشوكي. أظهرت رئتاها وكبدها وكليتاها والعقد اللمفاوية أضرارًا أشد، وكان البقاء طويل الأمد بعد TBI أسوأ بكثير. عندما أعاق الباحثون مستقبلات إنترفيرون النوع الأول، أو استبدلوا نقيع العظام الطافر بخلايا طبيعية، انخفضت معدلات إصابة الأعضاء والوفيات، مما أظهر أن إشارة إنترفيرون المفرطة من الخلايا الأحادية المحيطية هي محرك رئيسي لمتلازمة اختلال الأعضاء المتعددة في هذا السياق.
كيف يسمح سوء معالجة الأيونات للحمض النووي بالهروب
بالغوص داخل هذه الخلايا المناعية، وجد المؤلفون أن لايسوزومات الخلايا الناقصة TMEM110 كانت غير متوازنة كيميائيًا: كانت أقل حموضة ومشحونة بفرط بالكالسيوم. في هذه الظروف، فقد إنزيم DNase II — الذي يقصّ الحمض النووي عادة في اللايسوزومات — نشاطه، وأصبحت أغشية اللايسوزوم هشة، وهرب mtDNA إلى السيتوسول المحيط. أكدت تجارب مخبرية مع خلايا مناعية بشرية تبتلع ميتوكوندريات وُسمت أن غياب TMEM110 أدى إلى تسرب مزيد من mtDNA إلى سائِل الخلية وتحفيز اندفاع في جينات المحفزة بالإنترفيرون. تُظهر الدراسة أن TMEM110 يعمل من خلال التحكم في بروتين آخر، قناة أيونية لايسوزومية تُدعى TRPML1. عندما يكون TMEM110 حاضرًا، يتصل فعليًا بـTRPML1 ويغيّره إلى حالة «مفتوحة» تخلق بقعًا صغيرة لإطلاق الكالسيوم على سطح اللايسوزوم. تساعد هذه التدفقات المحكمة للكالسيوم في الحفاظ على الحموضة المناسبة، ودعم إصلاح الغشاء، وإبقاء mtDNA محاصرًا ومهضومًا بداخله. 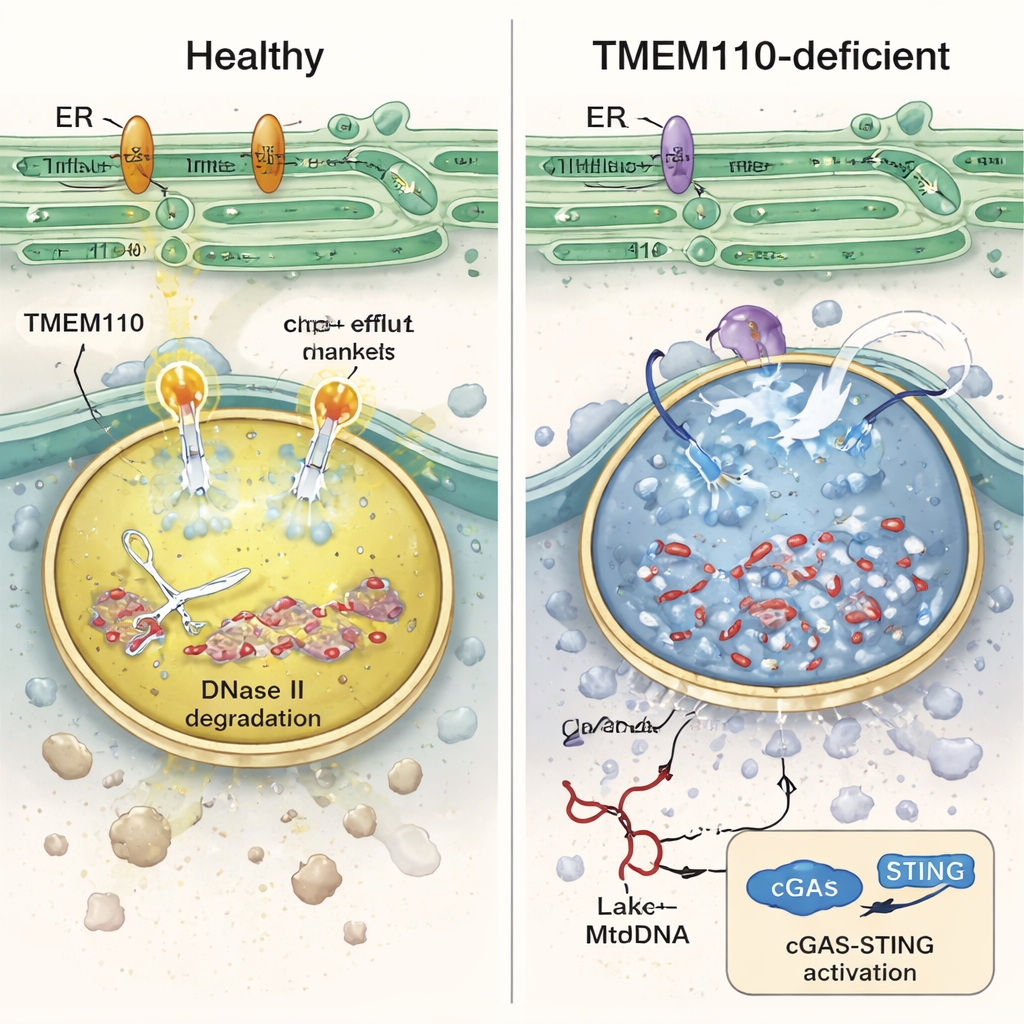
حلقة ارتجاعية مع نظام إنذار الحمض النووي في الخلية
بمجرد أن يتسرب mtDNA إلى السيتوسول، يتعرّفه مسار cGAS–STING، وهو نظام الإنذار الرئيسي للخلية ضد الحمض النووي المتشرد. ومن المثير أن TMEM110 يرتبط أيضًا بـSTING في حالة الراحة ويحتجزه في الشبكة الإندوبلازمية، مانعًا إطلاق إنذار غير ضروري. عندما يتراكم الحمض النووي السيتوسولي، يُفعّل STING ويخفف قبضته عن TMEM110. هذا بدوره يكشف منطقة مختلفة من TMEM110 تتفاعل مع TRPML1 وتعزز تدفق الكالسيوم من اللايسوزوم، فتنشأ حلقة ارتجاعية: استشعار الحمض النووي الذاتي ينشط آلية تعزز إزالة الحمض النووي. الطفرات المرتبطة بالأمراض في STING الموجودة في متلازمات التهابية ذاتية لدى البشر تعطل هذه الانتقالة، وتحجز TMEM110 في حالة مثبطة وتساهم في تنشيط مزمن للإنترفيرون. في الفئران الحاملة لمثل هذه الطفرة في STING، أدى TBI إلى تلف أعضاء أسوأ ومعدلات وفيات أعلى، لكن توصيل قطعة صغيرة من TMEM110 إلى اللايسوزومات باستخدام علاج جزيئي mRNA ضمن جسيمات دهنية نانوية استعاد جزئيًا السيطرة على mtDNA وحسّن البقاء.
دلائل من المرضى وسبل لعلاجات جديدة
ثم تحول المؤلفون إلى مجموعة سريرية مكوّنة من 143 شخصًا مصابًا بإصابة دماغية رضّية وMODS. كان المرضى الذين كانت خلاياهم الأحادية تُظهر مستويات أعلى من TMEM110 مبكرًا بعد الإصابة أكثر عرضة لاستعادة وظيفة الأعضاء والبقاء على قيد الحياة. أما أولئك الذين لديهم مستويات أقل من TMEM110 فقد أظهروا مزيدًا من mtDNA الدائري والميتوكوندريات المزالة الخلوية في الدم، واستجابات إنترفيرون أقوى، ونقاط فشل أعضاء أعلى، وأنماطًا أوسع من الأجسام المضادة الذاتية، بما في ذلك أضداد ضد الحمض النووي والبروتينات النووية. تواقت هذه الأنماط مع النتائج في الفئران، مؤيدةً الفكرة القائلة بأن ضبط TMEM110 لاستقرار اللايسوزومات والتخلص من mtDNA هو آلية مشتركة في المرض البشري.
ماذا يعني هذا لمرضى الصدمات الشديدة
بعبارات بسيطة، تشير هذه الدراسة إلى أن جهازنا المناعي يواجه بعد إصابة كبيرة خيارًا حساسًا: هل يهضم بصمت سيل الحمض النووي الذاتي المتحرر من الخلايا الميتة، أم يفسّره كغزو فيروسي ويشن هجومًا شاملًا قد يتلف أعضائنا؟ يساعد TMEM110، من خلال ضبط قناة أيونية لايسوزومية والتنسيق مع مستشعر الحمض النووي STING، الخلايا على اختيار المسار الأكثر أمانًا. عندما يفشل هذا النظام — لأن TMEM110 مفقود أو STING مُطعَّم بالطفرة أو اللايسوزومات مُثقلة — يهرب mtDNA، ويستمر جهاز الإنذار في الصراخ، ويتبع ذلك تلف متعدد الأعضاء. قد يوفر استهداف محور TMEM110–TRPML1–STING، على سبيل المثال بواسطة علاجات mRNA موجهة إلى اللايسوزوم، نهجًا جديدًا لمنع أو علاج فشل الأعضاء والمضاعفات الشبيهة بالمناعة الذاتية بعد الصدمات الشديدة.
الاستشهاد: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
الكلمات المفتاحية: إصابة دماغية رضّية, الحمض النووي الميتوكوندري, اللايسوزومات, إنترفيرون من النوع الأول, مسار cGAS-STING