Clear Sky Science · ar
الهيكل المجمد بالإلكترونيات لبنية مجمّع يوبكويتين ليغاز COP1-DET1 البشري
كيف تقرر الخلايا أي البروتينات تحطّم
داخل كل خلية، يجب بناء آلاف البروتينات وإعادة تشكيلها أو تدميرها في الوقت المناسب باستمرار. تبحث هذه الورقة في إحدى آليات "مراقبة الجودة" الرئيسية في الخلية، آلة جزيئية تبتّ إدها تقرر متى تزيل منظمات جينية قوية مرتبطة بالسرطان والتطور. من خلال كشف بنيتها ثلاثية الأبعاد بتفصيل قريب من الذرّي، يظهر المؤلفون كيف يمكن لهذه الآلة أن تتبدل بين حالة مكدسة خاملة وشكل نشط يعالج الركيزة — رؤى قد تساعد في نهاية المطاف على تصميم أدوية تضبط عملها أو توقفه.
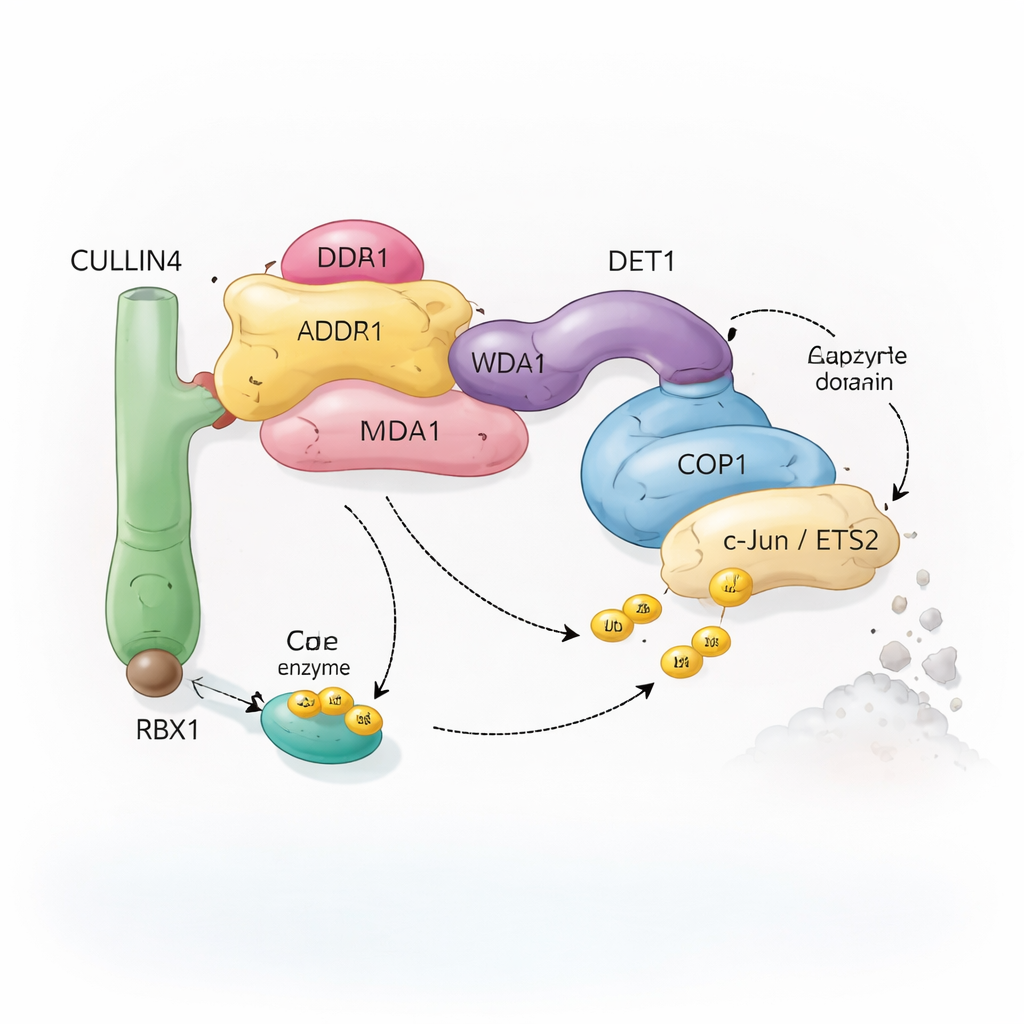
طقم جزيئي لإعادة التدوير يتألف من أجزاء عديدة
تعتمد الخلايا على نظام يُسمى اليوبيكويتيشن لوضع علامة على البروتينات لإعادة تدويرها. تعمل جزيئات صغيرة من اليوبيكويتين كأعلام قابلة للإزالة تشير إلى الخلية ما إذا كان ينبغي تعديل البروتين أو نقله أو تدميره. تقوم مركبات إنزيمية خاصة، تعرف بليغازات اليوبيكويتين، بإرفاق هذه الأعلام بالأهداف المختارة. يتركز المجمّع المدروس هنا حول COP1، بروتين يوجد في النباتات والبشر على حد سواء، ويساعد في وسم عوامل النسخ المهمة — وهي بروتينات تتحكم في تشغيل أو إيقاف الجينات. لا يعمل COP1 بمفرده: يمكنه أن ينضم إلى تجمّع أكبر مبني حول بروتين سقالة يدعى CULLIN4، بالإضافة إلى عدد من الحوامل المسماة DDB1 وDDA1 وDET1. تشكل هذه المكونات معاً "طقم إعادة التدوير" المرن الذي يتعرف على عوامل نسخ محددة مثل c‑Jun وETS2، والعديد منها يشارك في نمو الخلايا والسرطان.
التقاط المجمّع في ثلاثية الأبعاد
لفهم كيفية عمل هذا الطقم، استخدم الباحثون مجهر إلكترونيات كريو للجسيمات المفردة، تقنية تُصوّر البروتينات المجمّدة فجأة وتعيد بناء أشكالها بدقة عالية. أعادوا إنشاء نظام COP1–DET1 البشري في خلايا مزروعة، نَقّوا المجمعات، وصوّروا عدة حالات هيكلية مميزة. أولاً، حلّوا بنية وحدة DDB1–DDA1–DET1 التي تعمل كمحور مركزي. يتخذ DET1 شكلاً غير عادي جزئياً مرناً بدلاً من قرص صلب، مع "مخلب" بارز يمكنه الإمساك بالأنزيمات الشريكة. ثم، بإضافة COP1 وفئة من الأنزيمات المساعدة المعروفة باسم E2s، التقطوا تراكيب أكبر تُظهر كيفية تلاقي كل الأجزاء، كاشفةً عن تراكيب مضغوطة مكدسة وترتيبات ثنائية (تضم COP1 مزدوجًا) أكثر انفتاحًا.
كومة خاملة وثنائية نشطة
واحدة من أكثر النتائج إثارة هي بنية مكدسة تشبه الخيوط تتألف من طبقات متكررة من المجمّع. في كل طبقة، تتداخل ثمانية جزيئات COP1 عبر مقاطعها الملفوفة، مكوِّنة حلقة على شكل ماسة. مناطق تعرفها على الركائز، المسماة مجالات WD40، كلها تواجه في اتجاه واحد ومحميّة جزئياً بواسطة الطبقات المجاورة. من المرجح أن هذا الحزم الضيق يمثل حالة "إيقاف" حيث يكون الوصول إلى البروتينات المستهدفة محدودًا. بالمقابل، عندما فحص الفريق مجمّعات عبّرت مع ركيزات COP1 مثل c‑Jun أو ETS2، رأوا شكلاً ثنائيًا مختلفًا: جزيئتا COP1 مرتبتان جنبًا إلى جنب، مع مجالات WD40 تتجه للخارج ومتاحة لربط الدوافع القصيرة "VP" الموجودة في العديد من عوامل النسخ. أكدت تجارب بيوكيميائية أن هذه الحالة الثنائية فقط هي التي تدعم بكفاءة بناء سلاسل يوبكويتين طويلة على c‑Jun.
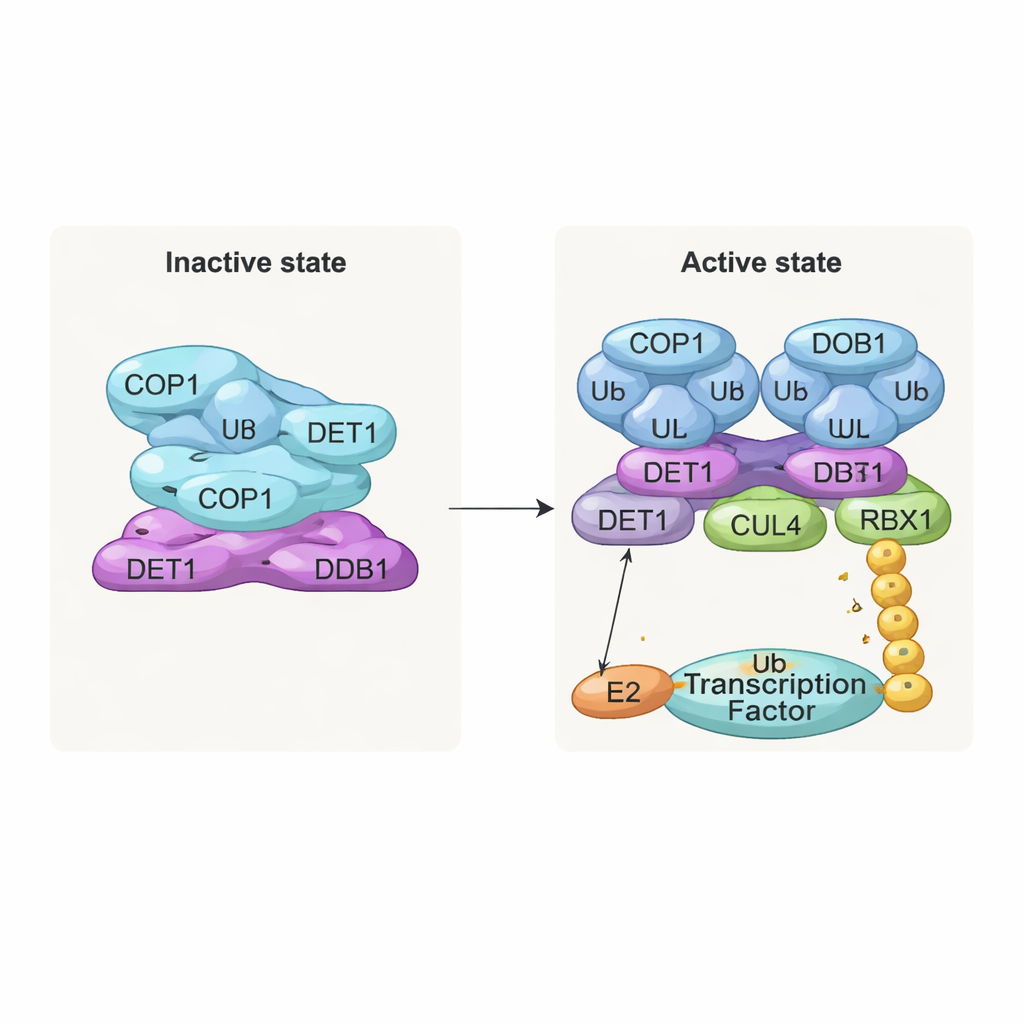
DET1 كجسر مرن وموجّه لحركة المرور
يبرز DET1 كمنظّم رئيسي يربط كل أجزاء الآلة. يستقر نطاقه الطرفي الأمامي داخل DDB1، مثبتًا المجمّع على السقالة CULLIN4، بينما يلتف جزء المخلب حول عائلة من أنزيمات E2 تسمى Ube2e. تُظهر تجارب طفيريّة مفصّلة أن DET1، وليس COP1، هو الذي يمسك مباشرة بهذه E2s، موضّعًا إياها بالقرب من منطقة RING التحفيزية في COP1. في هذا الترتيب، يبدو أن Ube2e يساعد في وضع أول علامات اليوبيكويتين على الركيزة. ثم يتم استقطاب أنزيم E2 ثاني، Ube2d3، عبر ذراع CULLIN4–RBX1 لتمديد هذه العلامات إلى سلاسل أطول تشير إلى التحلل الكامل. بعبارة أخرى، يعمل DET1 كجسر مرن يقدم E2 واحدًا إلى COP1، بينما تجلب السقالة الأكبر E2 ثانيًا لإكمال المهمة.
لماذا يهم هذا للصحة والمرض
من خلال رسم هذه الحالات البنائية وأنشطتها، تشرح الدراسة كيف يمكن لمجموعة البروتينات نفسها أن تتناوب بين شكل مكدس خامد وشكل ثنائي نشط يستهدف عوامل النسخ للتدمير. هذه النقلة مهمة بشكل خاص لعوامل مثل c‑Jun، التي تحفز انقسام الخلايا وترتبط ارتباطًا وثيقًا بالسرطان عند اختلال تنظيمها. إن فهم كيفية تعاون COP1 وDET1 — كيف يختار مخلب DET1 أنزيمات E2 محددة، كيف تتعرف سطحية WD40 في COP1 على الركائز المحتوية على VP، وكيف يتكوّن الثنائي النشط — يوفر مخططًا للعمل المستقبلي. على المدى الطويل، قد تمنح الأدوية التي تثبت الكومة الخاملة أو تفضّل الثنائي النشط الباحثين طرقًا جديدة لضبط مسارات التحكم الجيني في السرطان وغيره من الأمراض التي يختل فيها تحلل البروتين.
الاستشهاد: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
الكلمات المفتاحية: ليغاز اليوبيكويتين, COP1, تحلل البروتين, بنية كرايو-EM, c-Jun