Clear Sky Science · ar
البروتياز المعتمدة على يوبيكويتين K48 تقطع البروتينات بعد الشبكة الإندوبلازمية
كيف تقرر الخلايا أي البروتينات تدمر
تقوم خلايانا باستمرار بإزالة البروتينات البالية أو التالفة، وخصوصاً تلك المدمجة في الأغشية التي تعمل كبوابات ومستشعرات. تكشف هذه الورقة أن الخلايا تستخدم وسمًا صغيرًا يُدعى يوبيكويتين ليس فقط كعلامة «قمامة» عامة، بل كرمز يخبر كيف سيتم تفكيك بروتينات الغشاء بالضبط. فهم هذا الرمز يساعد في تفسير كيفية حفاظ الخلايا على صحتها وقد يوجّه علاجات مستقبلية تهدف إلى تدمير البروتينات المسببة للأمراض بشكل متعمد.
باركود خلوي للتخلص من البروتينات
تزيّن الخلايا البروتينات غير المرغوب فيها بسلاسل من بروتين صغير يسمى يوبيكويتين. يمكن ربط هذه السلاسل بطرق مختلفة، مثل خرز موصول عبر ثقوب متعددة، وكل نمط يمكن أن يرسل إشارة نتيجة مختلفة. ركَّز المؤلفون على بروتينات الغشاء التي غادرت بالفعل الشبكة الإندوبلازمية وتسافر عبر مقصورات مثل جهاز جولجي والإندوزومات. طرحوا سؤالًا عما إذا كان نوعا السلسلة الشائعان، المسميان المرتبطين عبر K48 وK63، قابلين للتبادل أم أن كلًا منهما يوجّه الحمولات إلى مسار تدمير مختلف.
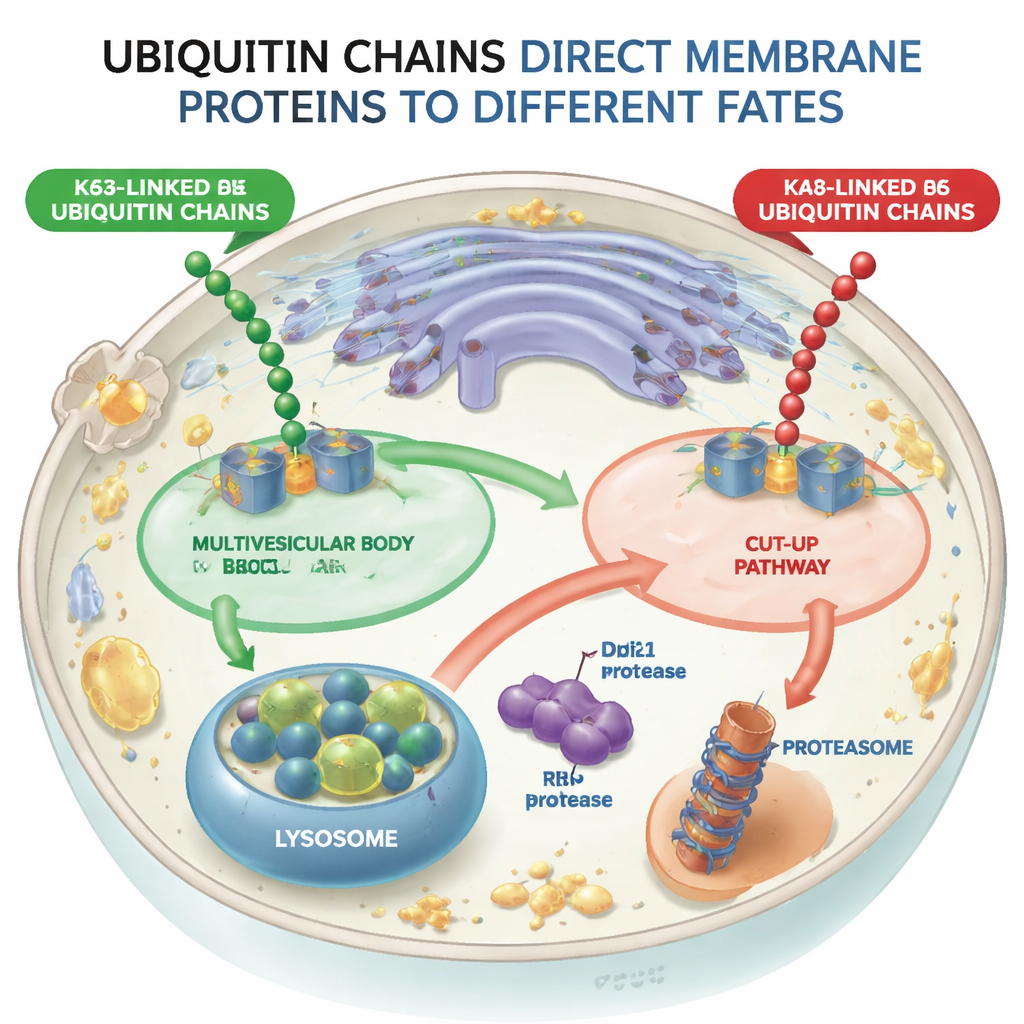
مساران متباعدان للبروتينات الموسومة
باستخدام خلايا الخميرة كنموذج، صمم الباحثون آلات جزيئية (ليجازات يوبيكويتين) قادرة على ربط سلاسل إما من نوع K48 أو K63 بنفس بروتين الغشاء الاختباري، مستقبل الفرز المسمى Vps10. عندما تلقى Vps10 سلاسل مرتبطة عبر K63، أُرسِل إلى الحويصلات الداخلية داخل الإندوزومات — وهي هياكل تُعرف بالأجسام متعددة الحويصلات — والتي تندمج في النهاية مع الليزوزومات، مقصورات الهضم الخلوية. بالمقابل، عندما حمل Vps10 سلاسل K48، لم يتبع هذا المسار متعدد الحويصلات. بدلاً من ذلك، تفتّت بآلية مختلفة تمامًا، ما يدل على أن الخلية تميّز بين هذين النوعين من السلاسل وأن مسار الأجسام متعددة الحويصلات يرفض فعليًا الحمولات الموسومة بـK48.
مسار «القطع» الذي يشطر البروتينات إلى قسمين
اكتشف الفريق أن السلاسل المرتبطة عبر K48 تفعّل مسار تقطيع البروتينات الذي أطلقوا عليه CUT-UP، اختصارًا لـ Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases. بدلًا من سحب البروتين بأكمله من الغشاء دفعة واحدة، يقوم CUT-UP بتقطيعه إلى أجزاء تُستكمل معالجتها بعد ذلك بواسطة أنظمة الإزالة الخلوية القائمة. أحد الإنزيمات الأساسية، Ddi1، يطفو في السيتوسول ويقطع الجزء من بروتين الغشاء المواجه للسيتوبلازم. يُهضم ذلك الجزء بعد ذلك بواسطة البروتيازوم، آلة تمزيق البروتين الرئيسية في الخلية. في الوقت ذاته، يجلس إنزيم آخر، Rbd2، داخل الغشاء نفسه ويقطع الجزء من البروتين المواجه لداخل الحُجرة، مطلقًا إياه إلى المساحة التي تتصل في النهاية بالليزوزوم. كان حظر Ddi1 وRbd2 والبروتيازوم وإنزيمات الليزوزوم معًا مطلوبًا لحماية Vps10 الموسوم بـK48 بالكامل من التحلل، مما يؤكد أن كل هذه المكونات تتعاون ضمن مسار CUT-UP.
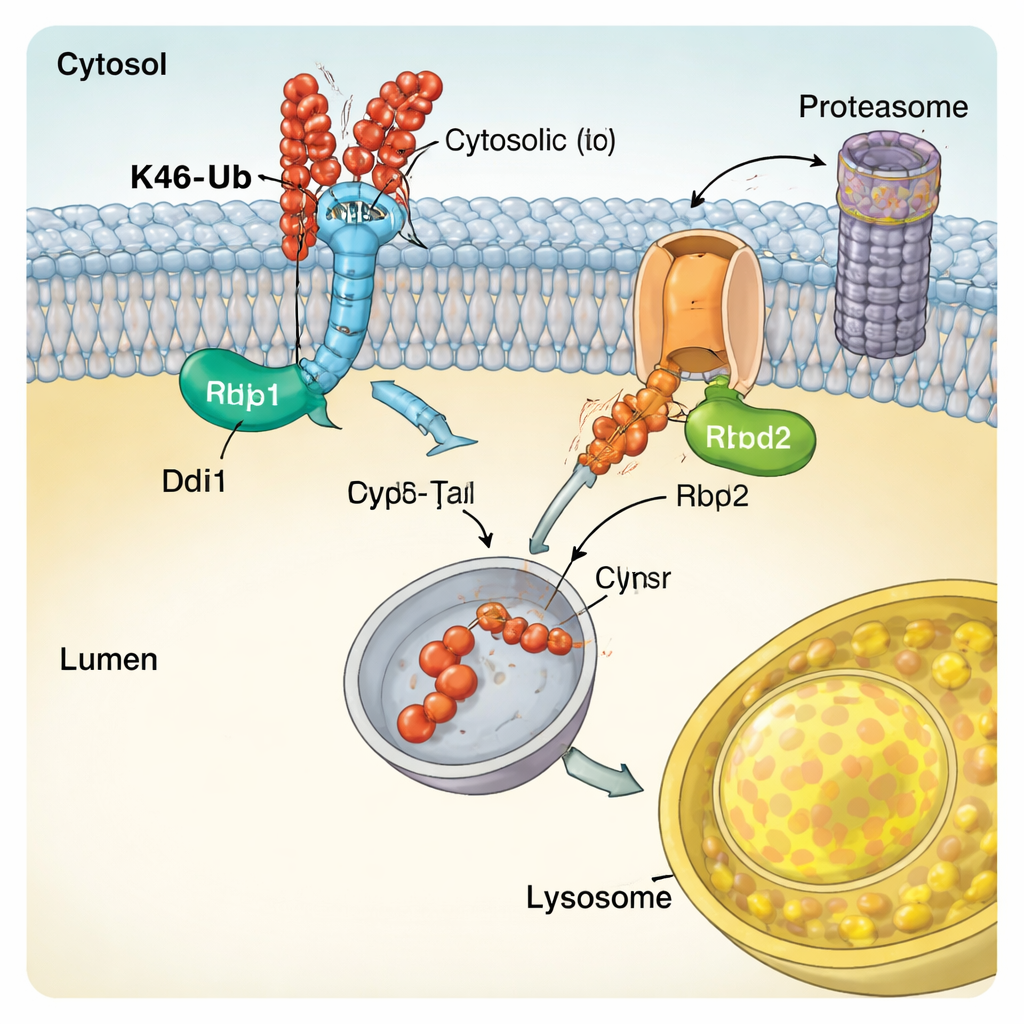
إنزيمات متخصصة تقرأ رمز اليوبيكويتين
لفهم كيف يتعرف CUT-UP على أهدافه، فحص المؤلفون الميزات الجزيئية لـDdi1. أظهروا أن النواة الحفزية المركزية لدى Ddi1 لا تقطع البروتينات فحسب، بل يمكنها أيضًا ربط اليوبيكويتين مباشرة، وأن نشاطها مضبوط بواسطة مناطق إضافية تتشبث بسلاسل اليوبيكويتين. أظهر Ddi1 اعتمادًا خاصًا على السلاسل المرتبطة عبر K48، مما يتوافق مع دوره في CUT-UP. أما Rbd2، فهو بروتيز rhomboid يعبر الغشاء. وجدت الدراسة أن الموقع الفعّال لـRbd2 ضروري لقص الأجزاء المواجهة للحواء من Vps10 وأن الإنزيم يمر عبر عدة مقصورات إفرازية، مما يسمح له بالعمل في مواقع خلوية متعددة. هناك إنزيمات مماثلة في الخلايا البشرية وقد ارتبطت بحالات تتراوح من التنكُّس العصبي إلى السرطان، مما يشير إلى أن آليات شبيهة بـCUT-UP قد تكون مهمة على نطاق واسع.
لماذا يهم هذا للصحة والعلاج
من خلال إظهار أن أنواعًا مختلفة من سلاسل اليوبيكويتين تُرسِل نفس بروتين الغشاء إلى مصائر متباينة بحدة — إما فرز داخل الأجسام متعددة الحويصلات أو تقطيع بواسطة CUT-UP — يوفر هذا العمل دليلًا قويًا على أن الخلايا تستخدم «رمز اليوبيكويتين» الحقيقي لتعديل التخلص من البروتينات بدقة. يوضّح اكتشاف CUT-UP كيف يمكن تفكيك البروتينات المقاومة قطعة بقطعة ويبرز Ddi1 وRbd2 كعناصر رئيسية تَقرَأ وتنفّذ هذا الرمز. للخارج عن التخصص، الخلاصة أن الخلايا لا تكتفي بوضع علامة «نفاية» على البروتينات؛ بل تحدد كيف سيتم إخراج هذه النفايات. بينما يصمم مطورو الأدوية أدوات وسم البروتينات الضارة باليوبيكويتين لإزالتها، سيكون فهم مسارات مثل CUT-UP ضروريًا للتنبؤ بما ستنتجه من شظايا وكيف قد يؤثر ذلك على سلوك الخلية.
الاستشهاد: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
الكلمات المفتاحية: رمز اليوبيكويتين, تحلل البروتين, بروتينات الغشاء, البروتيازوم, الليزوزوم