Clear Sky Science · ar
فقدان استشعار الكَثافة Fsr يعزز تكوّن الأغشية الحيوية ويُسوء النتائج في التهاب شغاف القلب العصوي
مخربون صامتون على صمامات القلب
التهاب شغاف القلب العدوائي عدوى مهددة للحياة تصيب صمامات القلب، وتزداد انتشارًا على مستوى العالم. تركز هذه الدراسة على فاعل رئيسي، البكتيريا المعوية Enterococcus faecalis، وتسأل لماذا تكون بعض الإصابات صعبة المعالجة بشكل خاص. من خلال كشف كيف تتواصل هذه البكتيريا مع بعضها وتبني أغشية حيوية واقية على الصمامات القلبية، يبيّن الباحثون لماذا تثير سلالات معينة مرضًا أشد ومقاومة للمضادات الحيوية، ولماذا يكون نظام الاتصال البكتيري المسمى Fsr مفاجئًا ككبح بدلًا من أن يكون مُسرّعًا للضرر.
كيف تبني البكتيريا حصونًا داخل القلب
عادةً تتحمل صمامات القلب بعضًا من أسرع تدفق دموي في الجسم، لكن إذا تضررت سطحية الصمام يمكن للصفائح الدموية وبروتينات التخثر أن تُكوّن خثرة صغيرة أو «نبتة». تصبح هذه الخثرة منصة تهبط عليها البكتيريا المتواجدة في مجرى الدم. بعد الالتصاق، تتكاثر البكتيريا وتنسج نفسها في غشاء حيوي — مجتمع لزج ومنظّم يحميها من خلايا الجهاز المناعي والأدوية. استخدم الفريق أجهزة ميكروفلويديك لمحاكاة تدفّق الدم في المختبر، ونموذجًا جرذانيًا لإعادة تكوين التهاب الشغاف في حيوانات حية، مما أتاح لهم مراقبة كيفية تكيّف E. faecalis مع تطور العدوى من بضع خلايا متناثرة إلى أغشية حيوية سميكة وناضجة. 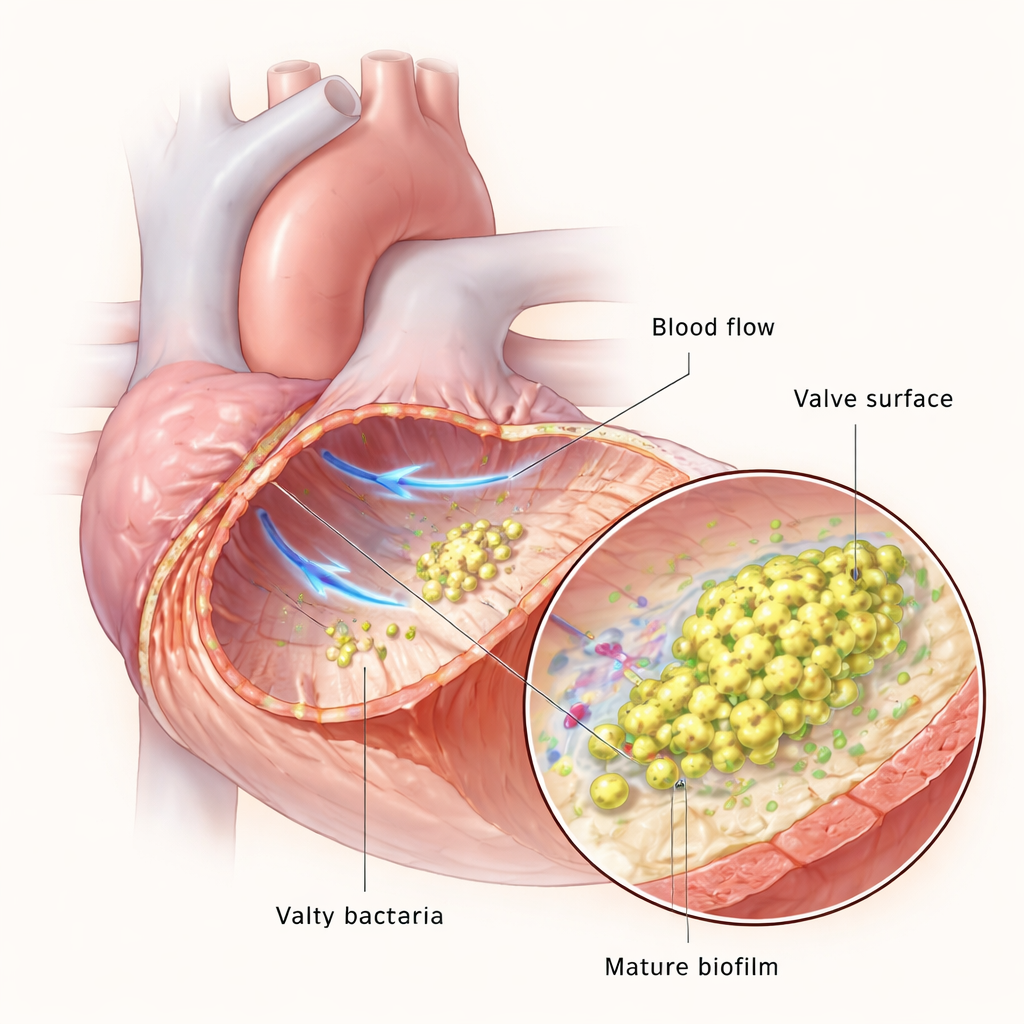
عندما تطفئ سرعة تدفّق الدم «الثرثرة» البكتيرية
غالبًا ما تنسق البكتيريا سلوكها باستخدام استشعار الكثافة، نظام كيميائي «للتصويت» يُشغّل أو يُطفيء جينات عندما يتجاوز عدد الخلايا عتبة معينة. Fsr هو نظام استشعار الكثافة المستخدم لدى E. faecalis. على نحو مفاجئ، وجد الباحثون أن السوائل المتحركة القوية تَجرف جزيئات الإشارة اللازمة لتفعيل Fsr. في المراحل المبكرة من العدوى، عندما تلتصق البكتيريا بسطح النبتة المكشوف وتشعر بكامل قوة تدفّق الدم، يكون Fsr صامتًا إلى حد كبير. فقط لاحقًا، عندما تكبر المستعمرات الدقيقة وتدفن أعمق داخل النبتة — محمية من التدفق — ينشط Fsr. يعني هذا أنه في القلب الحقيقي، لا يحدّد استشعار الكثافة فقط عدد البكتيريا، بل أيضًا موقعها داخل البنية ثلاثية الأبعاد.
إيقاف Fsr يسمح للأغشية الحيوية بالنمو المفرط
لاختبار ما يفعله Fsr فعليًا في العدوى، قارن الفريق بين بكتيريا طبيعية وطفرات تفتقر إلى نظام Fsr كاملًا. في البداية، استوطن كلا النوعين الصمامات بنفس المقدار. لكن بعد ثلاثة أيام، كانت الحيوانات المصابة بسلالات ناقصة Fsr تملك نباتات أكبر وعددًا أكبر بكثير من البكتيريا المكدّسة فيها. أظهرت التصويرات المفصّلة أن أغشيتهم الحيوية غطّت سطح الخثرة أكثر وكانت مستعمراتهم الدقيقة أكبر. كما أدى فقدان Fsr إلى إيقاف اثنين من الإنزيمات المفرزة الأساسية، GelE وSprE، اللذين يساعدان عادة في تشكيل الغشاء الحيوي وقد يقيّدان النمو المفرط. الحيوانات المصابة بطفرات تفتقد هذين الإنزيمين أيضًا طوّرت أغشية حيوية أضخم، وإن لم تكن بدرجة التطرف نفسها كما في سلالات خالية من Fsr، مما يوحي بوجود عوامل أخرى يتحكم فيها Fsr وتشارك في الظاهرة. 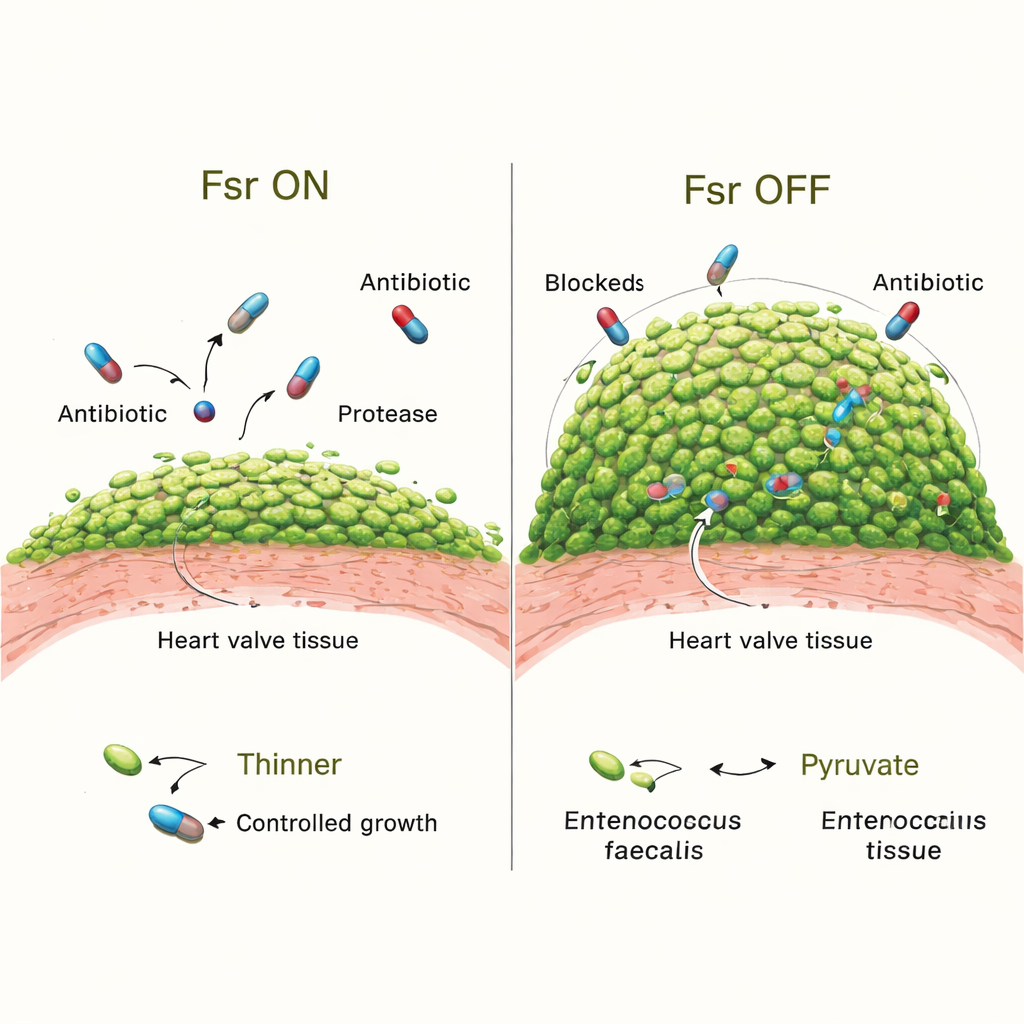
إعادة توصيل أيضية وقوة أكبر في مواجهة المضادّات الحيوية
كشف تحليل التعبير الجيني للبكتيريا داخل الصمامات المصابة أن Fsr يفعل أكثر من التحكم في بعض الإنزيمات. في غياب Fsr، تغير نشاط مئات الجينات، خصوصًا تلك المشاركة في امتصاص السكريات وإنتاج الطاقة. برز زوج جيني واحد، lrgA وlrgB: كانا مشغّلين بشدة في بكتيريا ناقصة Fsr وساعدا الخلايا على استغلال البيروفات أكثر كجزيء غني بالطاقة موجود في الدم. عندما حذف الباحثون lrgAB مع Fsr، زال النمو المفرط للأغشية الحيوية، مما يشير إلى دور محوري لهذا المسار الأيضي في تغذية العدوى المتضخّمة. ولاحظ الباحثون أن الأغشية الحيوية الناقصة Fsr كانت أيضًا أصعب علاجًا. في الجرذان التي أعطيت المضاد الحيوي جنتاميسين، تقلّصت الإصابات بالبكتيريا الطبيعية وتحسّنت معدّلات الصفائح الدموية — وهو علامة على تحسّن شدة المرض. بالمقابل، بالكاد استجابت الإصابات الناقصة Fsr، رغم أن البكتيريا لم تكن أكثر مقاومة للأدوية في اختبارات المختبر المعيارية.
تواء البشر الخاص بالالتهاب
كشفت الدراسة أيضًا عن احتمال أن هذه البكتيريا تُثير الالتهاب لدى البشر بطريقة خاصة. يستطيع إنزيم GelE قطع السلائف البشرية لإشارة المناعة IL‑1β إلى الشكل النشِط الذي يُحرّك الاستجابات الالتهابية. بشكل محيّر، قطع GelE IL‑1β في الجرذان بصورة مختلفة، مفكّكًا إياها بدلاً من تنشيطها، وكان القطع الدقيق للتنشيط مفقودًا في بروتينات الجرذان والفئران. هذا التأثير الخاص بالأنواع يشير إلى أن GelE قد يساعد لدى البشر في تركيز الالتهاب عند حافة الغشاء الحيوي، مما قد يزيد تلف الأنسجة أثناء التهاب الشغاف.
من المختبر إلى العيادة: لماذا يهم فقدان Fsr للمرضى
لفحص ما إذا كانت هذه النتائج التجريبية تهم في الواقع السريري، حلّل الباحثون عزلات E. faecalis من 81 مريضًا يعانون من التهاب شغاف عدواني في سويسرا والولايات المتحدة. افتقرت ما يقرب من نصف السلالات طبيعيًا إلى نظام Fsr. المرضى المصابون بهذه السلالات السالبة لـFsr شهدوا بكتيريميا أطول مدة — أيامًا أكثر تُكتشف فيها البكتيريا في دمهم — وكانوا أكثر عرضة للدخول في فئة عالية الشدة التي شملت العناية المركزة، فترات إقامة مطوّلة في المستشفى، إجراءات قلبية كبرى، أو الوفاة. لم تستطع جينات الضراوة الأخرى تفسير هذا النمط، مما يشير مباشرة إلى فقدان Fsr كعلامة رئيسية لمرض أكثر عدوانية.
لماذا يهم هذا لعلاجات المستقبل
معًا، تقلب هذه النتائج الفكرة البسيطة القائلة بأن تعطيل الاتصال البكتيري سيضعف العدوى دائمًا. في التهاب شغاف E. faecalis، يكبح نظام Fsr فعليًا توسع الأغشية الحيوية ويجعل البكتيريا أكثر عرضة للمضادات الحيوية. عندما يفقد Fsr، تنمو البكتيريا أغشية حيوية أكثر كثافة، وتستغل مغذيات الدم بكفاءة أعلى، وتدفع نحو إصابات عنيدة ومطوّلة. بالنسبة للمرضى، يعني هذا أن السلالات التي تفتقر إلى Fsr قد تتنبأ بمرض يصعب علاجه، وأن العلاجات التي تُغلِق استشعار الكثافة بلا تمييز قد تأتي بنتائج عكسية في هذا السياق. بدلًا من ذلك، قد تكون استهدافاتٌ دقيقة للمسارات الأيضية مثل استخدام البيروفات، أو مراقبة حالة Fsr وGelE كعلامات تنبؤية، طرقًا أفضل لإدارة هذه الالتهابات القلبية الخطيرة.
الاستشهاد: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
الكلمات المفتاحية: التهاب شغاف القلب العدوائي, الأغشية الحيوية البكتيرية, استشعار الكثافة, Enterococcus faecalis, تحمّل المضادّات الحيوية