Clear Sky Science · ar
RNA ذات VPg مصمَّمة تحقق ترميزًا مستقلًا عن الغِطاء، منخفض المناعة ودقيقًا للبروتينات العلاجية في الجسم الحي
إعادة كتابة قواعد أدوية الحمض النووي الريبي
ساعدت اللقاحات المعتمدة على الحمض النووي الريبي الرسول (mRNA) في تغيير مسار جائحة كوفيد-19، لكن استخدام جزيئات مماثلة لاستبدال أو تعويض بروتينات مفقودة في الأمراض المزمنة أصعب بكثير. يميل الجسم إلى تدمير الحمض النووي الريبي الغريب بسرعة وإطلاق استجابات مناعية قوية، والعديد من تصميمات RNA ذاتية التضخيم الحالية ترتكب أخطاء أثناء نسخ نفسها. تصف هذه الدراسة نوعًا جديدًا من RNA ذاتي التضخيم—مصنوعًا من أجزاء من نوروفيروس بشري—مصممًا ليكون طويل الأمد، أقل قابلية لإثارة الالتهاب، ودقيقًا على نحو غير معتاد، مما يفتح الباب أمام أدوية RNA أكثر دقة وديمومة.
حمض نووي ريبيري ذاتي النسخ أكثر ذكاءً
تحمل علاجات mRNA التقليدية «وصفة» واحدة للبروتين وتُقرأ مرة واحدة بواسطة الخلية قبل أن تُحلّل. يتضمن RNA ذاتي التضخيم (saRNA) آليات فيروسية إضافية تسمح للحمض النووي الريبي بنسخ نفسه داخل الخلايا، معززًا الإنتاج بشكل كبير بجرعة صغيرة. أكثر أنظمة saRNA دراسةً مشتقة من الفيروسات الألفا، لكنها كبيرة الحجم، وتثير دفاعات مضادة للفيروسات قوية، وتنسخ سلاسلها بدقة منخفضة نسبيًا. لجأ المؤلفون بدلًا من ذلك إلى نوروفيروس بشري، وهو سبب شائع لالتهاب المعدة المعوي. عزلوا مقطعًا مدمجًا من المادة الوراثية للنوروفيروس وأعادوا بنائه كحامل للجينات العلاجية. في جوهره يوجد VPg، بروتين فيروسي صغير مرتبط كيميائيًا بالطرف الأمامي للـRNA. يستبدل VPg بنية «الغِطاء» المعتادة الموجودة على mRNA البشري ويسمح بترجمة الـRNA عبر مجموعة مختلفة من عوامل الخلية الأقل حساسية لإشارات الإجهاد المعينة. 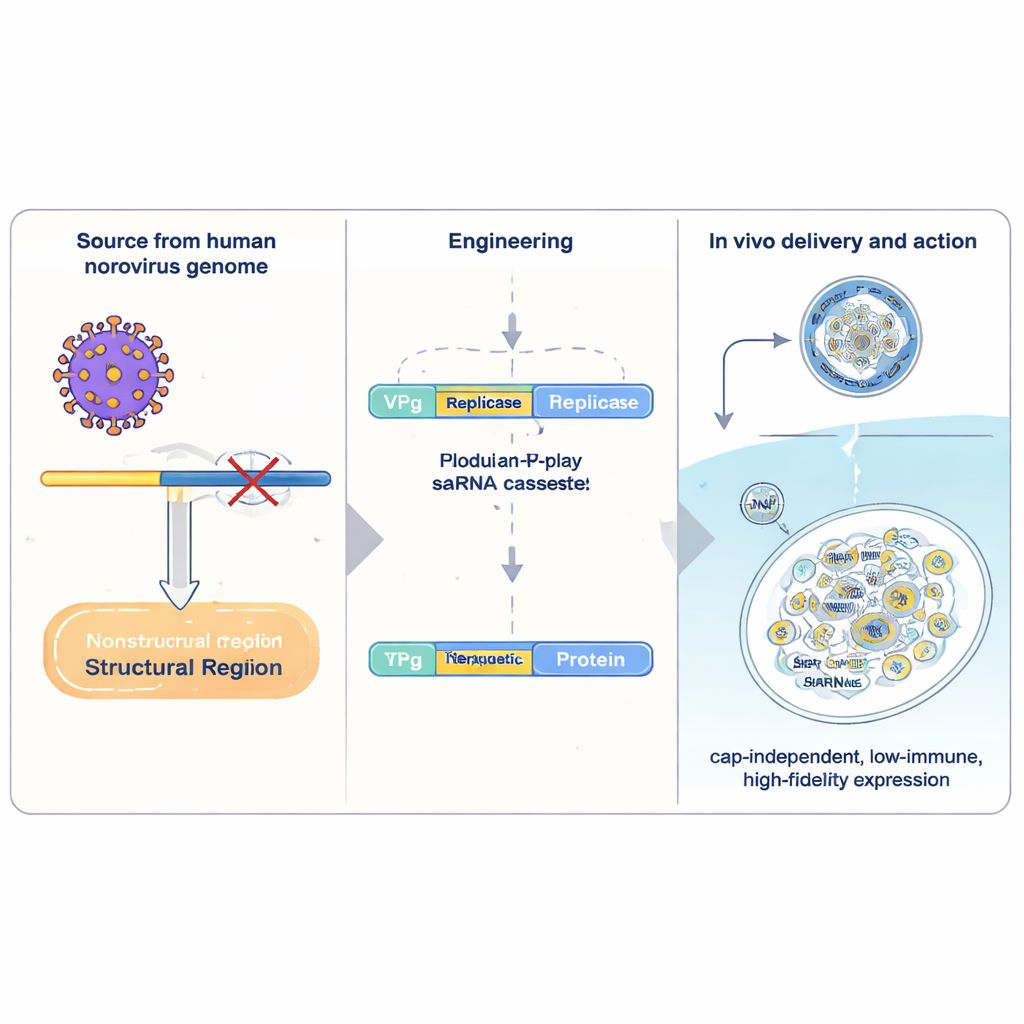
دقة عالية دون إثارة الجهاز المناعي
بالنسبة للعلاجات البروتينية، الدقة مهمة: حتى الأخطاء الصغيرة في النسخ يمكن أن تغير سلوك الدواء أو تُنتج نواتج سامة. أظهر الفريق أنه عندما يرتبط VPg النوروروبي بالفَرَسَنة النسخية للفيروس (بلمرة)، فإنه يبطئ معدل إضافة اللبنات غير الصحيحة، مما يقلل بشكل حاد معدل الأخطاء. حدّدوا أحماضًا أمينية محددة في VPg التي تتصل بمنطقة تحكم رئيسية في البلمرة وأثبتوا أن تشويش هذا الواجه يجعل النسخ أقل دقة. في الوقت نفسه، تصاميم saRNA التقليدية تولّد كميات كبيرة من RNA مزدوج السلسلة، وهو ناقوس جزيئي يفعّل دفاعات مضادة للفيروسات ويوقف إنتاج البروتين. من خلال إعادة تصميم البلمرة لتفضيل شكل بداية واحد مرتبط بـVPg وإعادة ترتيب الجينوم بحيث يُنتَج الشريط العلاجي فقط بكفاءة، خفّض المؤلفون بشكل كبير تكوّن RNA مزدوج السلسلة. علاوة على ذلك، ضبطوا منطقة ذيلية من الـRNA حتى يرتبط VPg في الموقع الصحيح، مانعين قطعًا قصيرة وغير مقصودة قد تُترجم إلى ببتيدات بعيدة.
يعمل حيث يفشل mRNA القياسي
اختُبر saRNA القائم على VPg الجديد في ظروف مرضية متطلبة حيث يعاني mRNA المغطى التقليدي. في هزال المرتبط بالسرطان—متلازمة هدم تفقد فيها العضلات والدهون—تُطفأ عوامل ترجمة رئيسية تتعرف على غطاء الـmRNA القياسي، مما يجعل رسائل mRNA المعتمدة على الغطاء غير فعالة. لأن VPg يستخدم مدخلًا بديلاً إلى آلية ترجمة الخلية، استمر في دفع إنتاج هرمون الجريلين المسؤول عن الشهية والتمثيل الغذائي في نموذج فأري لسرطان البنكرياس. ساعدت الحقن الشهرية بجرعات منخفضة على الحفاظ على العضلات والدهون، وحسّنت تناول الطعام والتمثيل الغذائي، ومدّت البقاء على قيد الحياة بشكل معتدل، دون سمية واضحة أو علامات تنشيط مناعي مزمن.
هجوم سرطان دقيق ومناعة ذاتية أقل ضجيجًا
لاختبار ما إذا كانت الدقة العالية في النسخ مهمة فعلاً، حمّل الباحثون ناقل VPg بتركيب أونكوليتيكي معقد، GSDMDENG، مصمم لعمل ثقوب في ميتوكوندريا خلايا السرطان وتحفيز استجابات مناعية نوعية للورم. عندما وُضع نفس التركيب على saRNA تقليدي من فيروس الألفا، تراكمت الطفرات عبر جولات متكررة من النسخ وأضعفت وظائفه الانتقائية لقتل الخلايا السرطانية وتحفيز المناعة. على النقيض من ذلك، حافظ نظام VPg على التسلسل المقصود، أنتج قتلًا قويًا لخلايا الورم، وأثار استجابات خلوية T متينة أبطأت أو منعت سرطان البنكرياس في نماذج الفئران. أخيرًا، طبّقوا saRNA القائم على VPg على تحدٍّ مختلف: مرض الطُعم مقابل المضيف المزمن، حيث تهاجم الخلايا المناعية الرئتين بعد زرع نخاع العظام. خفّض saRNA المشفر للبروتين C المنشط من تكون الأجسام المضادة الضارة، ومنع تليّف الرئتين، وحسّن التنفّس في الفئران، بينما أثار تركيب مماثل قائم على فيروس الألفا مناعة فطرية أقوى وأسفر عن نتائج أسوأ.
لماذا يهم هذا لأدوية الـRNA المستقبلية
تجمَع الأعمال معًا لتقدّم منصة RNA مدمجة «قابلة للتوصيل» تربط ثلاث صفات مرغوبة: تنسخ نفسها بدقة، مصمَّمة لتقليل إنذارات الجهاز المناعي، وتتجاوز بعض اختناقات الترجمة التي تقيد mRNA القياسي. لأن الجين العلاجي يُستبدل ببساطة في عمود فقري ثابت مبني على نوروفيروس، يمكن اختبار بروتينات متنوعة—من الهرمونات إلى منظمات التخثر إلى عوامل أونكوليتيك—على نفس الهيكل. بينما يبقى الكثير من العمل قبل الاستخدام البشري، يقترح نهج VPg saRNA هذا مسارًا نحو أدوية RNA تعمل أشبه بحقن البروتين المستقرة: بجرعات منخفضة، أطول أمداً، ومصممة لتعمل حتى في الأنسجة المريضة حيث لا يمكن قراءة رسائل mRNA العادية بثقة. 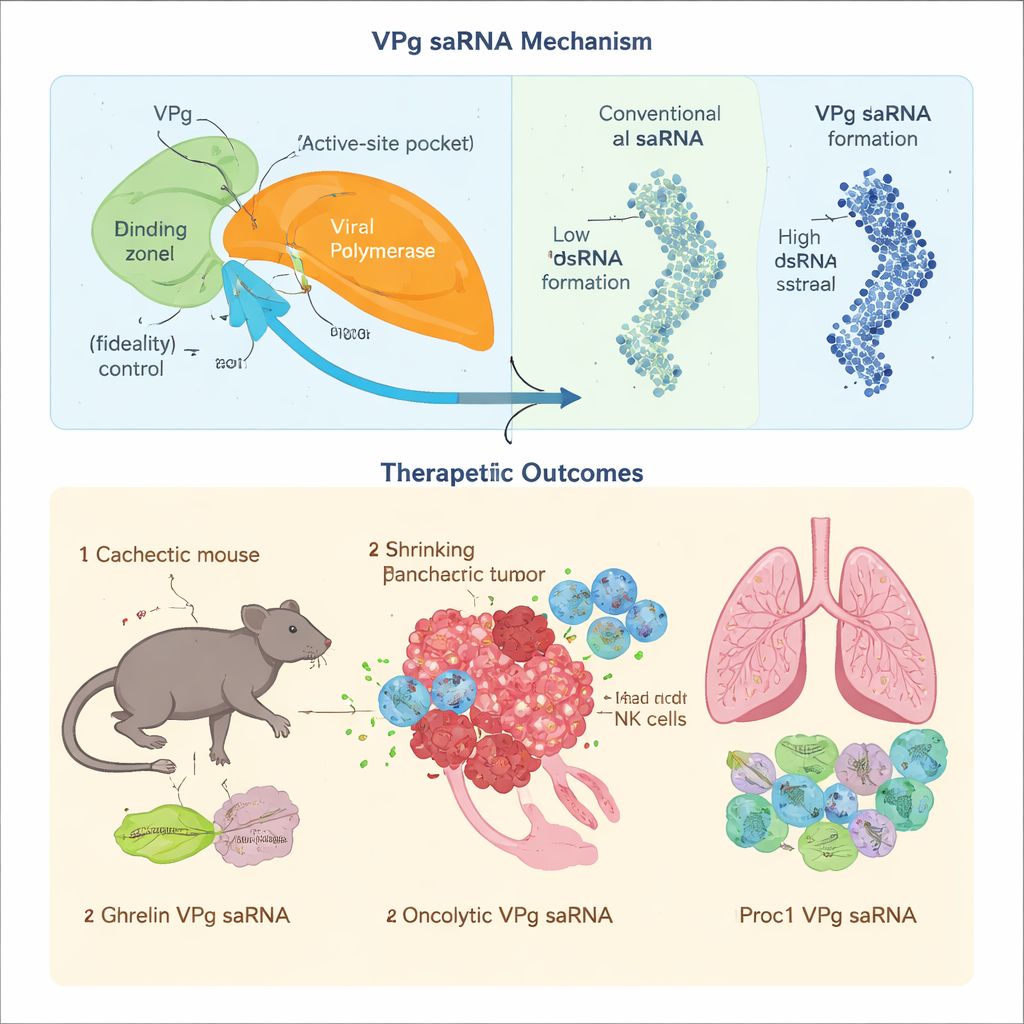
الاستشهاد: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
الكلمات المفتاحية: RNA ذاتية التضخيم, علاجات mRNA, VPg نوروفيروس البشري, هزال السرطان, مرض الطُعم مقابل المضيف