Clear Sky Science · ar
تحسين التليف الرئوي لدى الفئران عبر استهداف الخلايا الطلائية السنخية المتوسطة الموجه بتواقيع نسخية
لماذا يهم تندب الرئتين
التليف الرئوي مرض رئوي خطير تتحول فيه الحويصلات الهوائية الرقيقة تدريجياً إلى نسيج ندبي صلب، مما يجعل كل نفس مهمة شاقة. الأطباء يعلمون أن هذا التندب يبدأ عندما تخرج آليات الإصلاح الطبيعية عن مسارها، لكن ظل من غير الواضح أي الخلايا تحديداً هي المسؤولة وكيفية إزالتها دون الإضرار بالنسيج الرئوي السليم. تستكشف هذه الدراسة طريقة جديدة لـ «قراءة» الرسائل الجزيئية داخل خلايا الرئة، واستخدام تلك المعلومات لتحديد الخلايا الانتقالية الضارة واستئصالها انتقائياً لتقليل التندب في الفئران.
الخلايا الموقوفة أثناء إصلاح خاطئ
بعد إصابة الرئة، تتكاثر عادة خلايا من النوع الثاني المنتجة لمادة السطح المبطن ثم تنضج إلى خلايا رقيقة من النوع الأول التي تبطن الحويصلات الهوائية وتسمح بمرور الأكسجين إلى الدم. في حالات التليف، تُحبس كثير من هذه الخلايا في حالة وسيطة أو انتقالية بدلاً من إتمام هذا التحول. كشفت دراسات سابقة لتسلسل RNA لخلايا مفردة عن هذه الخلايا الوسيطة في كلٍ من الفئران والبشر، لكن لم يتضح ما إذا كانت مجرد مشاهدين أم محركات أساسية للمرض. ركز المؤلفون على نوع وسيط في الفئران يُسمى Krt8+ وسط تفريق السنخ، ونظائره البشرية المعروفة بالخلايا البازالودية الشاذة، التي تظهر بأعداد كبيرة في الرئتين المتندبتين.
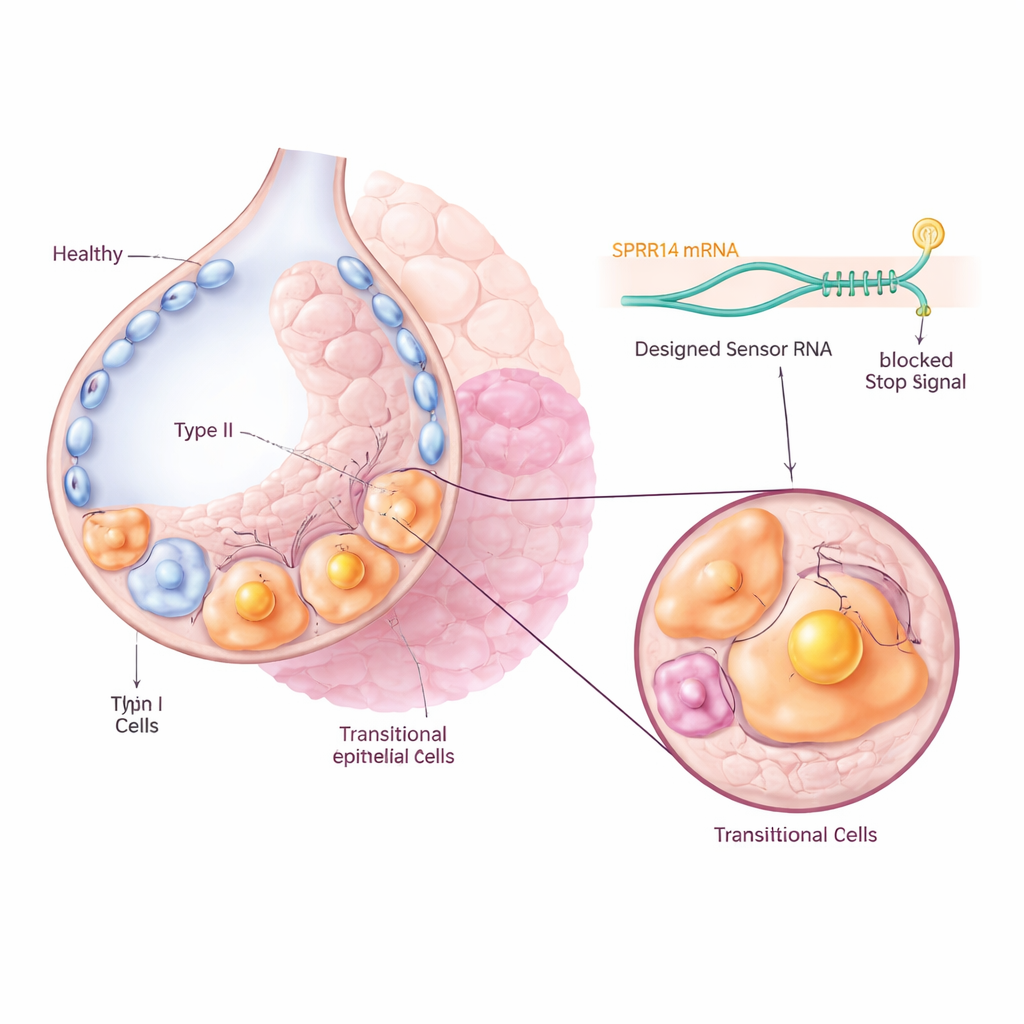
العثور على وسم جزيئي فريد
لكي يستهدفوا هذه الخلايا المسببة للمشكلة دون المساس بالخلايا السليمة المجاورة، بحث الفريق أولاً في مجموعات بيانات واسعة للتعبير الجيني عن علامة تُفعّل بقوة وبشكل محدد في السكان الانتقاليين. حدّدوا جزيئاً اسمه SPRR1A كـ «وسم اسم» بارز: كان معبراً عنه بشكل مرتفع ومركز في خلايا Krt8+ الوسيطة في رئات الفئران المتليفَة، وفي الخلايا البازالودية الشاذة KRT5-/KRT17+ لدى مرضى التليف الرئوي مجهول السبب، بينما كان غائباً إلى حد كبير في خلايا الرئة الطبيعية. أكدت المشاهد المجهرية لأنسجة الرئتين من الفئران والبشر أن SPRR1A ظهر أساساً في المناطق المصابة والمُعاد تشكيلها وليس في الحويصلات الهوائية السليمة، ما يوحي بأنه يمكن أن يكون مقبضاً دقيقاً لتحديد الخلايا المذنبة.
برمجة الخلايا بمستشعر RNA
ثم استخدم الباحثون تقنية طوِّرت حديثاً تُسمى CellREADR، التي تعمل كمستشعر جزيئي داخلي. صمّموا سلاسل RNA قصيرة يمكنها الاقتران القاعدي مع RNA الخاص بـ SPRR1A داخل الخلية. عندما يكتشف المستشعر SPRR1A، يُشغِّل إنتاج بروتين «فعّال» ملحق، مثل وسم فلوري أو مستقبل يجعل الخلية حساسة لدواء معين. في الفئران، استُخدمت فيروسات لتوصيل هذه تركيبات المستشعر–الفعّال إلى خلايا الرئة. شُغِّل الإشارة الفلورية فقط في الخلايا التي كانت تنتج SPRR1A فعلياً، مما أتاح للفريق تتبّع وعزل الخلايا الانتقالية مباشرة من رئات متليفة. أظهر تسلسل الخلية الواحدة أن الخلايا الموسومة تطابقت عن كثب مع توقيع الجينات الانتقالي المعروف، مؤكداً أن مستشعر الـ RNA كان يستهدف السكان المقصودين بدقة.
إطفاء الحالات الوسيطة الضارة
بعد ذلك، استُبدل البروتين الفلوري غير الضار بمستقبل سم الدفتريا، بحيث يمكن قتل الخلايا الإيجابية لـ SPRR1A انتقائياً بإعطاء سم الدفتريا. من خلال توقيت العلاج ليتزامن مع ذروة وفرة الخلايا الانتقالية بعد إصابة رئوية كيميائية، تمكن المؤلفون من إزالة نحو ثلث هذا التجمع. أدت هذه الإزالة الموجهة إلى تقليل واضح في تندب الرئة: انخفض تراكم الكولاجين، وتراجع مستوى البروتينات الليفية، وعادت بنى الحويصلات الهوائية لتبدو أكثر طبيعياً. أظهرت التحليلات المفصّلة أن معظم الخلايا الإيجابية لـ SPRR1A حملت علامات حالة مرهقة تشبه الشيخوخة، مع مجموعة صغيرة قادرة على تكاثر عالي، ما يشير إلى أن هذه الخلايا الوسيطة تفشل في إصلاح النسيج بشكل صحيح وتساهم في استمرار العملية الليفية.
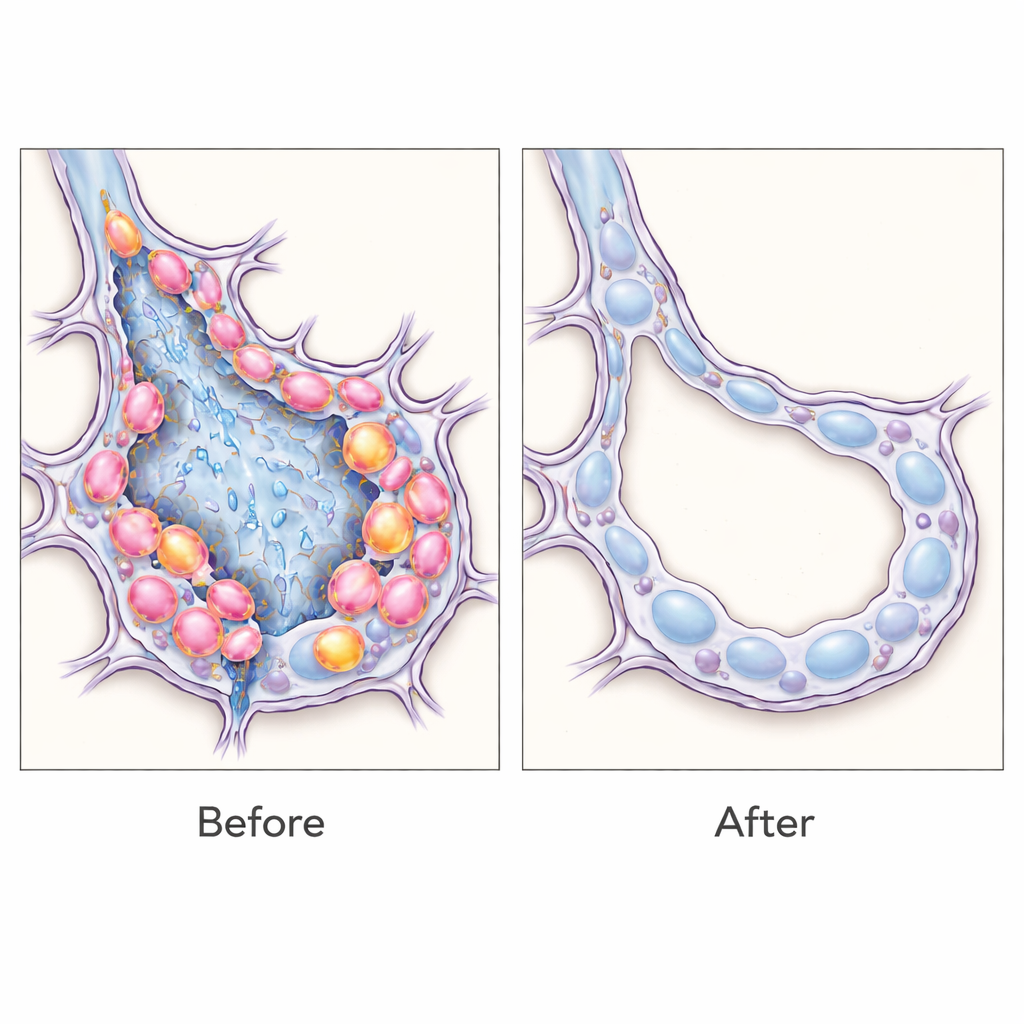
ماذا يعني هذا للعلاجات المستقبلية
تُدلّل هذه النتائج على أن الخلايا الطلائية الانتقالية ليست مجرد مؤشرات بل محركات نشطة للتليف الرئوي، وأن إزالتها بشكل انتقائي يمكن أن تعيد التوازن نحو بنية رئوية أكثر صحة في الفئران. وعلى نطاق أوسع، تُظهر الدراسة استراتيجية مرنة: من خلال «قراءة» تواقيع RNA المحددة لكل خلية، يمكن للباحثين وسم ودراسة وحتى استئصال مجموعات خلوية محددة ضمن النسيج الحي دون الحاجة إلى إنشاء خطوط حيوانية مخصصة في كل مرة. بينما لا يزال أمامنا الكثير قبل أن تُكيّف أدوات استشعار الـ RNA هذه بأمان للإنسان، يفتح هذا النهج مساراً نحو علاجات دقيقة تستهدف أنواع الخلايا المحددة التي تعيق الشفاء في التندب الرئوي المزمن وربما في أمراض ليفية أخرى.
الاستشهاد: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
الكلمات المفتاحية: التليف الرئوي, الخلايا الطلائية السنخية, تسلسل RNA على مستوى الخلية الواحدة, تكنولوجيا استشعار الـ RNA, شيخوخة خلوية