Clear Sky Science · ar
من تشكيل مركب TDP-43/RNA إلى تراكم TDP-43 المرتبط بالأمراض عبر نهج بنيوي وخَلَوِي
لماذا هذا البروتين الدماغي مهم
تتميز الأمراض التنكسية العصبية مثل التصلب الجانبي الضموري والخرف الجبهي الصدغي غالبًا بتجمعات من البروتينات المُشوَّهة داخل الخلايا العصبية. أحد المشتبه بهم الأكثر شيوعًا هو بروتين يُدعى TDP-43، الذي يساعد عادة في معالجة RNA—النسخة العاملة من جيناتنا. تسأل هذه الدراسة سؤالًا جوهريًا: ماذا يفعل TDP-43 في الخلايا السليمة، وما الذي يحدث ليَتحول مساعد RNA المفيد إلى بروتين سام يشكل تجمعات؟
كيف يعمل TDP-43 في الخلايا العصبية السليمة
عادةً ما يتواجد TDP-43 في نواة الخلية، حيث يرتبط بقطع طويلة من RNA غنية بتكرارات الوحدات «GU». باستخدام مزيج من علم الأحياء البنيوي وتجارب خلوية، يُظهر المؤلفون أن جزيئات TDP-43 تصطف بشكل تعاوني على طول هذه المناطق الغنية بـ GU، مكونة سلاسل ناعمة ومتواصلة على الـ RNA. عند ترتيبها بهذه الطريقة، يبقى الطرف الأمامي من البروتين—النطاق الطرفي النشوءي (N-terminal domain)—مفصولًا ماديًا بين الجزيئات المجاورة. نتيجة لذلك، تظل هذه المقاطع الطرفية متاحة لتصل عبر وربط مقاطع بعيدة غنية بـ GU من نفس الـ RNA، مما يلف ويكثف الإنترونات الطويلة (المقاطع غير المشفرة داخل الجينات) بطريقة لطيفة دون تكوُّن تجمعات ضارة.
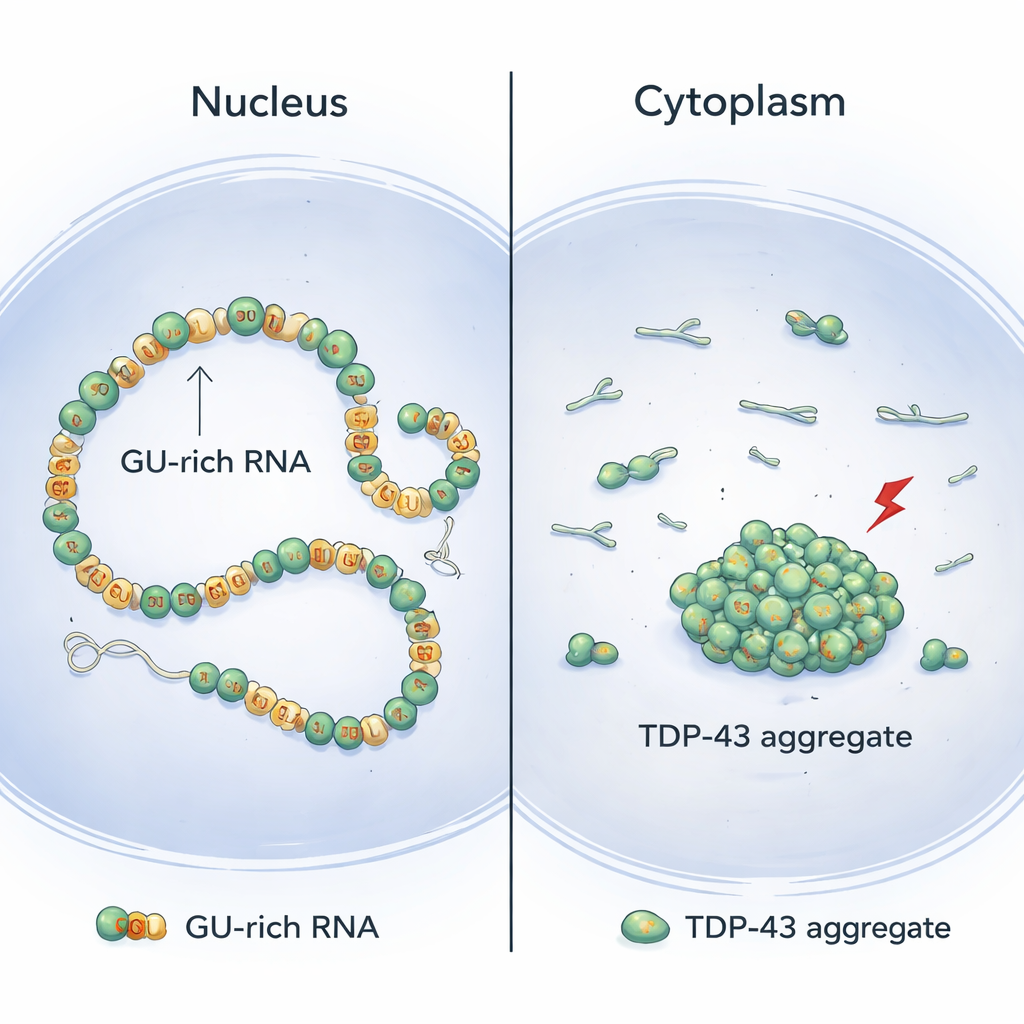
صراع مصمم داخل البروتين
استقصى الفريق بعد ذلك كيف تتنافس أجزاء مختلفة من TDP-43 أو تتعاون مع بعضها البعض. ركزوا على منطقتين: النطاق الطرفي النشوءي، الذي يمكن أن يلتصق بنطاقات N-terminal الأخرى، والوحدات المركزية الرابطة للـ RNA، التي تدفع الارتباط التعاوني على RNA الغني بـ GU. باستخدام تقنيات حساسة مثل مطيافية الرنين المغناطيسي النووي (NMR)، والمعايرة الحرارية، وانتثار الأشعة السينية بزوايا صغيرة، وجدوا أنه عندما يرتبط TDP-43 بالـ RNA بشكل تعاوني، فإن هندسة السلسلة تضعف فعليًا الاتصالات المباشرة بين النطاقات الطرفية N-terminal للجزيئات المجاورة. بعبارة أخرى، الارتباط التعاوني القوي بالـ RNA يكبح التفاعلات الطرفية المحلية. لكن عندما ينكسر هذا التعاون—على سبيل المثال، بإدخال مقاطع غير GU في الـ RNA أو عن طريق طفرات في TDP-43—تتحرك النطاقات الطرفية في البروتينات المجاورة بالقرب من بعضها ويمكنها الآن أن تتشابك معًا.
من التكتل المفيد إلى التكوّن الضار للتجمعات
اختُبرت هذه الرؤى البنيوية في خلايا حية. استخدم المؤلفون أنظمة خلوية مهندَسة لتتبع كيفية امتزاج أو انفصال طفرات TDP-43 المختلفة داخل حُجرات صناعية غنية بالـ RNA. وجدوا أن كلًا من الارتباط التعاوني بالـ RNA والتفاعلات الطرفية N-terminal يساعدان في تنظيم TDP-43 إلى تراكيب مرتبة أعلى، لكن بطرق مختلفة. الارتباط التعاوني يسلسِل البروتينات على طول RNA الغني بـ GU، بينما تربط الاتصالات الطرفية مجموعات بعيدة معًا. لكن تحت ضغط تأكسدي طفيف، يتغير المشهد. يسبب عامل إجهاد كيميائي (الزرنيخ) تعديلات كيميائية محددة—مثل الأسيتلة—على الوحدات المركزية الرابطة للـ RNA، ما يجعلها أكثر ميلًا للالتصاق ببعضها. إذا ظل الارتباط التعاوني بالـ RNA سليمًا، يبقى TDP-43 قابلًا للذوبان إلى حد كبير. وإذا ضعُف التعاون، تعمل الروابط الطرفية بين جزيئات TDP-43 المجاورة كهيكل يدفع الأنوية المُأسَتلة للاقتراب من بعضها، مما يشجع على التجمع غير القابل للانعكاس.
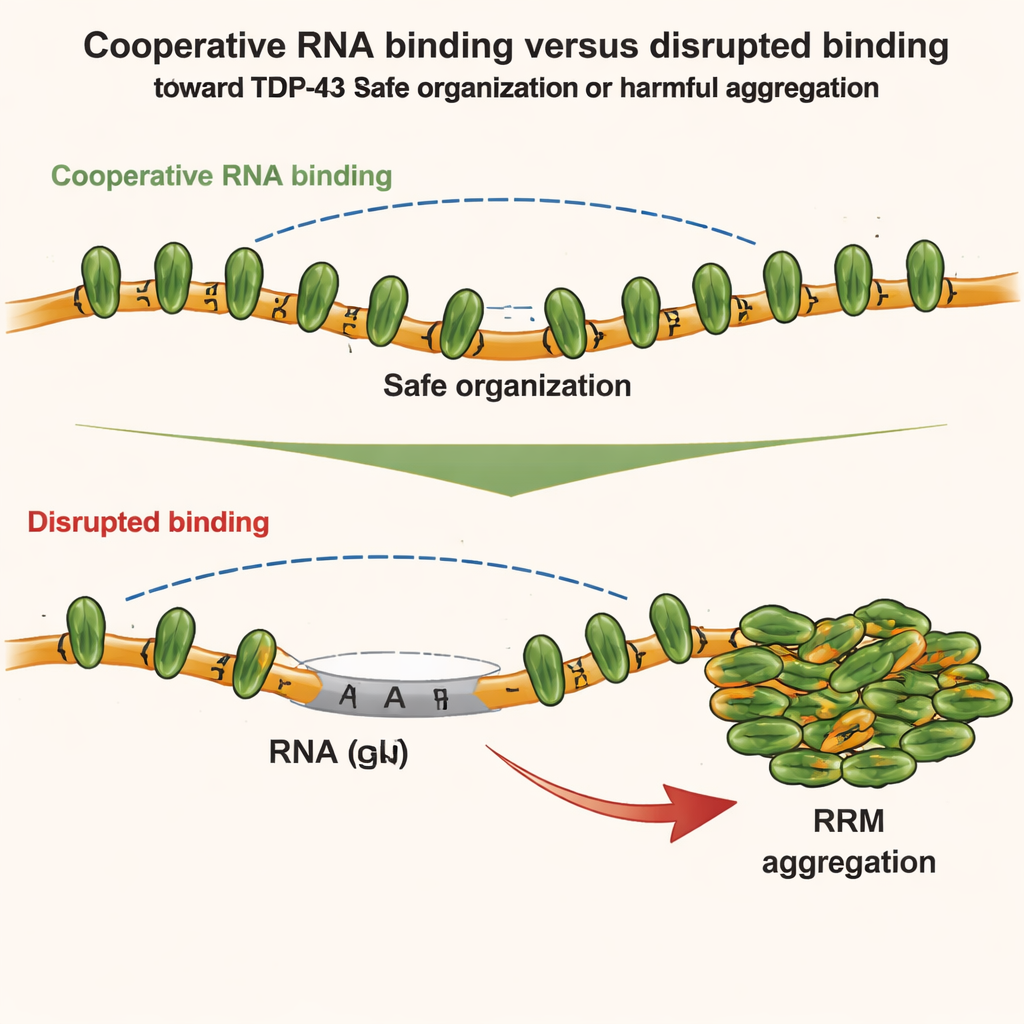
لماذا يتجمع TDP-43 أكثر في السيتوبلازم
النموذج الناشئ من هذا العمل يساهم في تفسير سبب وجود تراكمات TDP-43 في كثير من الأحيان في سيتوبلازم الخلايا العصبية المريضة بدلًا من النواة. في النواة، تكون الإنترونات الطويلة التي تحتوي على العديد من تكرارات GU شائعة، مما يفضّل ارتباطًا تعاونيًا مستمرًا يحافظ على انخفاض التفاعلات الطرفية الخطرة بين الجيران ويسمح بطيّات آمنة على المدى الطويل بدلًا من التكوّن. في السيتوبلازم، بالمقابل، تحتوي الـ RNAs الناضجة على عدد أقل بكثير من القطع الغنية بـ GU. هذا يجعل ارتباط TDP-43 أكثر رُقعِيَّة وأقل تعاونًا، مما يزيد من احتمال تفاعل النطاقات الطرفية المجاورة ويهيئ الأرضية للتجمع بمجرد حدوث تغييرات كيميائية ناجمة عن الإجهاد. دعماً لهذا التصور، أدى تزويد النواة صناعيًا بإنترونات إضافية غنية بـ GU إلى تقليل تكاثف TDP-43 تحت الإجهاد.
ماذا يعني هذا للعلاجات المستقبلية
ببساطة، تصوّر الدراسة TDP-43 كبروتين متوازن بين تنظيم مفيد للـ RNA وتكوّن ضار للتجمعات، مع عمل الارتباط التعاوني بـ RNA الغني بـ GU كآلية أمان. عندما يفشل هذا الشبك الأمني—بسبب تغيّر تسلسل الـ RNA أو طفرات البروتين أو إجهاد خلوي—يمكن أن تتحول نفس النطاقات التي تضغُط عادةً المقاطع الطويلة من الـ RNA إلى عوامل تدفع تكوّن تجمعات سامة. بالنسبة لغير المتخصصين، الخلاصة الأساسية هي أن الحفاظ على النوع الصحيح من التفاعلات بين TDP-43 وRNA قد يكون استراتيجية واعدة لمنع أو إبطاء تكاثف البروتين الذي يُرى في التصلب الجانبي الضموري وأمراض دماغية ذات صلة.
الاستشهاد: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
الكلمات المفتاحية: تَكَثُّف TDP-43, بروتينات رابطة بـ RNA, التصلب الجانبي الضموري (ALS), تفاعلات البروتين–RNA, الانحلال العصبي