Clear Sky Science · ar
استهداف مستقبل mGlyR بالنانوبوديز لعلاج الاكتئاب
لماذا يهم هذا النهج الجديد لعلاج الاكتئاب
العديد من الأشخاص المصابين بالاكتئاب الشديد لا يحصلون على ارتياح كافٍ من الأدوية الحالية، التي قد تكون بطيئة المفعول وتسبب آثارًا جانبية غير مرغوبة. تستكشف هذه الدراسة نوعًا مختلفًا تمامًا من العلاج: أجسام مضادة مصغرة مهندَسة تُسمى نانوبوديز، تستهدف مستقبلًا واحدًا في الدماغ مرتبطًا بالمزاج. من خلال إظهار أن نانوبوديًا واحدًا يمكن أن يخفف بسرعة الأعراض الشبيهة بالاكتئاب لدى الفئران، تفتح الأبحاث مسارًا جديدًا نحو علاجات حيوية دقيقة للغاية للاكتئاب الصعب العلاج. 
هدف جديد مخفي في توصيلات الدماغ
تعمل معظم مضادات الاكتئاب على ناقلات عصبية كلاسيكية مثل السيروتونين والدوبامين. هنا، يتركز الاهتمام على نظام آخر يعتمد على الجليسين، جزيء صغير يعمل أيضًا كمرسال في الدماغ. يوجد مستقبل جديد للجليسين، يُدعى mGlyR، بكميات عالية في القشرة الجبهية الأمامية، المنطقة التي تساعد في التحكم بالعواطف واستجابات التوتر. يميل الأشخاص المصابون بالاكتئاب الشديد إلى وجود كمية أكبر من هذا المستقبل، والفئران المربّاة بدون mGlyR تظهر مرونة غير اعتيادية تجاه التوتر وتعرض سلوكيات أقل تشبه الاكتئاب. أشارت هذه المؤشرات إلى أن خفض نشاط mGlyR قد يكون له فوائد مضادة للاكتئاب.
تصميم أداة مضادة للاكتئاب صغيرة ودقيقة
بدلاً من البحث عن دواء تقليدي صغير الجزيء، لجأ العلماء إلى النانوبوديز — أجسام مضادة أحادية المجال مشتقة من حيوانات مثل اللاما. النانوبوديز أصغر بكثير من الأجسام المضادة التقليدية، ويمكن أن تكون محددة للغاية، وتزداد دراسة إمكانياتها كعقاقير. قامت الفريق بتمنيع لاما بخلايا تعرض mGlyR، ثم استخدم تقنية عرض الأفاج لاختيار أجزاء من الأجسام المضادة عبر مليارات المرشحات. من بين 61 مرشحًا واعدًا، برز نانوبودي واحد باسم Nb20 باعتباره الأقوى والأكثر انتقائية في الارتباط بـ mGlyR. أظهرت الاختبارات في خلايا مزروعة أن Nb20 يلتصق بإحكام بالنطاق الخارجي للمستقبل لكنه لا يلتصق بمستقبلات دماغية ذات صلة، مما يؤكد دقته.
كيف يعيد النانوبودي توصيل إشارات الخلية
يتحكم mGlyR في الإشارة الدماغية بطريقة غير معتادة. على جانبه الداخلي، لا يرتبط مباشرةً بالبروتينات G النموذجية، بل يتصل بمجمع مساعد يُدعى RGS7/Gβ5 يسرع إيقاف إشارات بروتين G. عندما يكون هذا المجمع نشطًا جدًا، فإنه يضعف استجابة الخلايا العصبية. باستخدام اختبار ضوئي في خلايا حية، وجد الباحثون أن Nb20 يتداخل مع آلية الإيقاف هذه: عندما يكون Nb20 حاضرًا وmGlyR نشطًا، تنطفئ بروتينات G ببطء أكبر، ما يعني أن مجمع RGS7/Gβ5 يصبح أقل فعالية. أظهرت صور المجهر الإلكتروني بالتبريد بتفاصيل تقترب من الذرية أن Nb20 يضم النطاق الخارجي «Cache» للمستقبل ويحرّك شكله بشكل طفيف. تبدو تلك التحولات وكأنها تنتقل عبر البروتين إلى الجانب الداخلي، مما يجعل مجمع RGS7/Gβ5 أكثر ارتخاءً ومرونة، وأقل قدرة على قمع الإشارة. 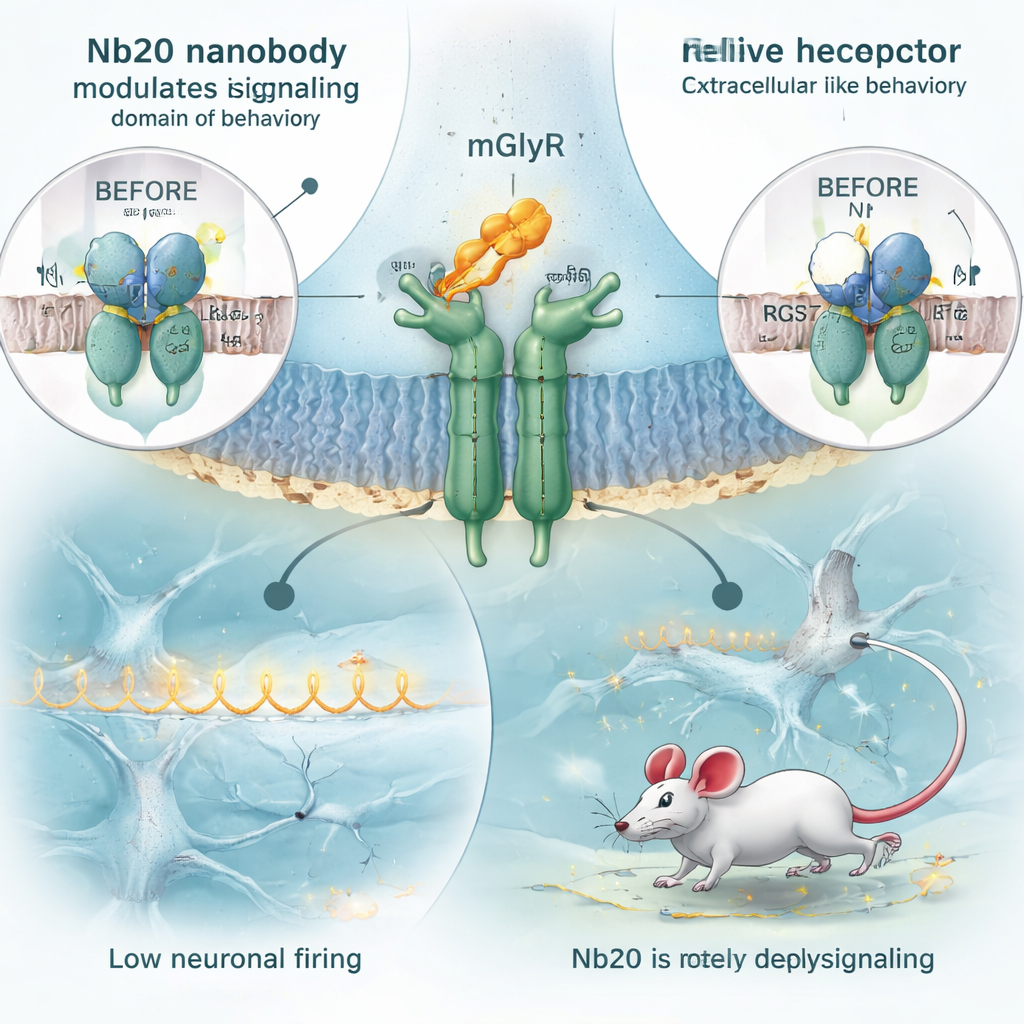
من الجزيئات إلى المزاج في الفئران
سأل الفريق بعد ذلك ما إذا كان لهذا التأثير الجزيئي أثر على السلوك. عندما تم توصيل Nb20 مباشرة في أدمغة الفئران، أظهرت الحيوانات مؤشرات أقل على السلوك الشبيه بالاكتئاب: كافحت أكثر في اختبارات قائمة على التوتر ودفنت عددًا أقل من الكرات الزجاجية، وهو سلوك مرتبط بالقلق والميول الوسواسية. اللافت أن إعطاء Nb20 عن طريق مسار أنفي بسيط — قطرات المحلول في الأنف — أنتج أيضًا تأثيرات مضادة للاكتئاب قوية في فئران تعرضت لأسابيع من التوتر غير المتوقع. عبر عدة اختبارات سلوكية، كانت فوائد Nb20 قابلة للمقارنة مع مضاد الاكتئاب سريع المفعول كيتامين، لكن دون تغيرات في الحركة الأساسية أو التناسق. أظهرت تسجيلات من شرائح دماغية أن Nb20 جعل بعض خلايا القشرة الجبهية الأمامية أسهل إثارة، متسقًا مع تحول نحو دوائر أكثر نشاطًا تتحكم بالمزاج.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
تقدم هذه الدراسة دليلاً مبدئيًا على أن أداة حيوية محددة للغاية، موجهة إلى مستقبل واحد مرتبط بالاكتئاب، يمكن أن تحسن بسرعة السلوكيات المتعلقة بالمزاج لدى الحيوانات. وتشير إلى أن أدوية قائمة على النانوبوديز تستهدف mGlyR قد توفر يومًا خيارًا جديدًا للأشخاص الذين لا يستجيب اكتئابهم للأدوية الحالية. لا يزال العمل كثيرًا قبل إمكانية التجارب على البشر، بما في ذلك تحسين دخول Nb20 إلى الدماغ، وضمان السلامة، والتأكد من أن آليات مماثلة تعمل لدى البشر. ومع ذلك، تُبرز النتائج فكرة قوية: بدلاً من تغيير كيمياء الدماغ على نطاق واسع، قد يكون من الممكن تخفيف الاكتئاب عن طريق دفع مستقبل واحد رئيسي وشركائه في الإشارة بدقة نحو حالة أكثر صحة.
الاستشهاد: Laboute, T., Zucca, S., Sial, O.K. et al. Targeting mGlyR with nanobodies for depression. Nat Commun 17, 831 (2026). https://doi.org/10.1038/s41467-026-68339-x
الكلمات المفتاحية: علاج الاكتئاب, نانوبوديز, مستقبل الجليسين, العلاج المناعي للدماغ, القشدة الجبهية الأمامية