Clear Sky Science · ar
تعزيز عبر الأنف بـ LcrV غير المعزز يقوي مناعة الرئتين لدى الفئران الملقَّحة أوليًا بحويصلات الغشاء الخارجي لـ Yersinia ضد الطاعون الرئوي
دفاع من خطوتين ضد قاتل مشهور
قد يبدو الطاعون كمرض من التاريخ الوسيط، لكن الشكل الرئوي منه، الطاعون الرئوي، لا يزال قادراً على القتل بسرعة وينتقل عبر الهواء. تساعد المضادات الحيوية، ومع ذلك تظل السلالات المقاومة للعقاقير واحتمال الإفراج المتعمد يجعل الطاعون ضمن قوائم المراقبة المعاصرة. تستكشف هذه الدراسة على الفئران استراتيجية تطعيم ثنائية المراحل تهدف ليس فقط إلى رفع مستوى الأجسام المضادة في الدم، بل إلى تدريب «حراس» مناعيين مُطَوَّلين يقيمون داخل الرئتين، جاهزين لإيقاف عدوى مميتة قبل أن تترسخ.
لماذا تهم الحماية الموجهة إلى الرئة
هناك شكلان رئيسيان للطاعون: الدَبْلِيّ (bubonic)، الذي يبدأ عادة بتورم العقد اللمفاوية بعد لدغة برغوث، والطاعون الرئوي الذي يهاجم الرئتين ويمكن أن يكون مميتاً تقريباً إذا تأخر العلاج حتى يوم واحد. اللقاحات التجريبية الحالية تؤدي أداءً معقولاً ضد الطاعون الدبلي لكنها واجهت صعوبة ضد الشكل الرئوي. أحد الأسباب أن معظم الحقن تعطى في العضلات وتعلّم الجهاز المناعي أساساً في مجرى الدم، لا على الأسطح الرطبة للمجاري الهوائية حيث يبدأ الطاعون الرئوي. لحماية الرئتين فعلاً، يزداد اعتقاد العلماء أنه يجب على اللقاحات زرع خلايا مناعية «مقيمة» تتخذ مواقع طويلة الأمد داخل نسيج الرئة نفسها.
بناء لقاح صف أول أكثر أمانًا
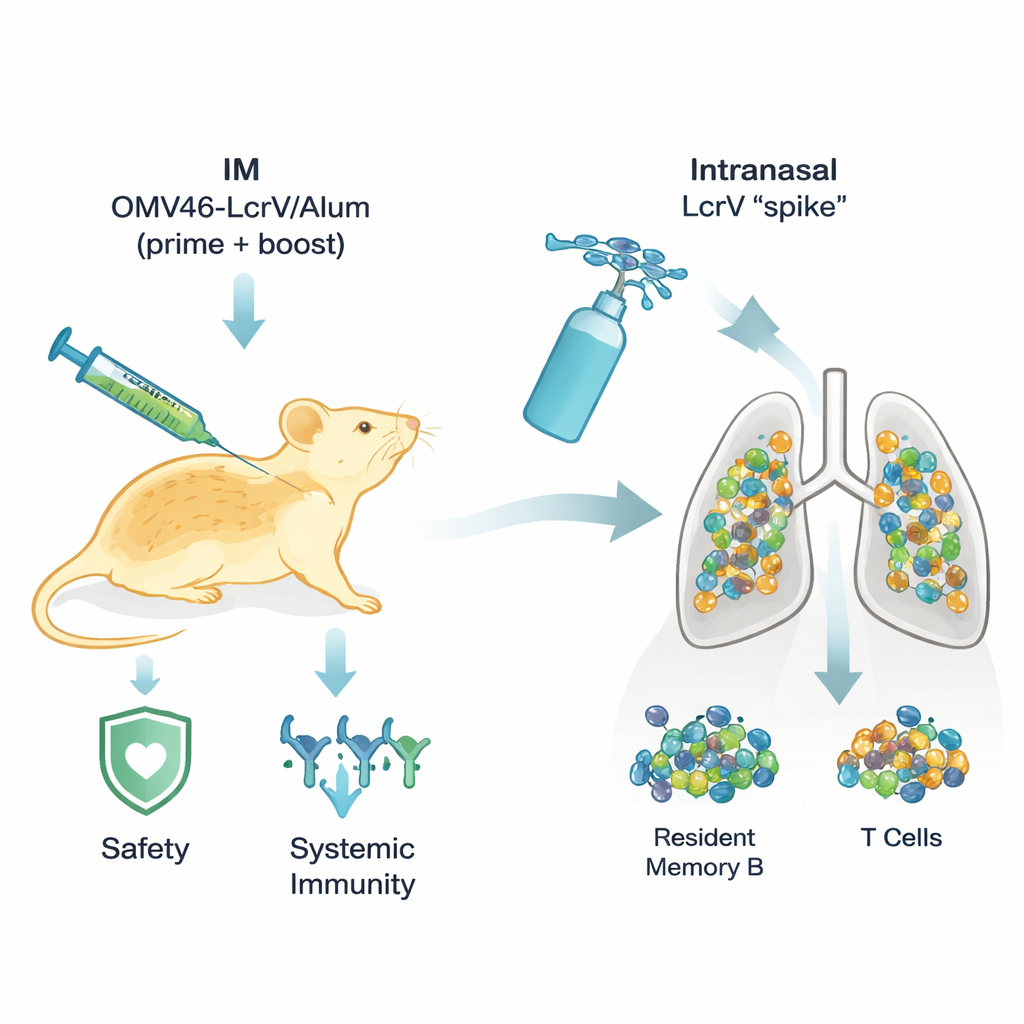
كان الفريق قد طور سابقًا لقاح طاعون واعدًا مبنيًا على حويصلات الغشاء الخارجي (OMVs) من قُرَيْبٍ من Yersinia، مزينة ببروتين طاعون رئيسي يُدعى LcrV. هذا الحقن OMV46‑LcrV وفر حماية قوية لرئات الفئران لكنه تسبب ببعض التفاعلات قصيرة الأمد. للحد من هذه الآثار الجانبية، امتص الباحثون الحويصلات على أملاح الألمنيوم («الألوم»)؛ وهي مكوّن لقاح مستخدم منذ زمن طويل يجعل اللقاحات أكثر أمانًا بشكل عام ويساعد على تكوين الأجسام المضادة. في الفئران، النسخة المرتبطة بالألوم (OMV46‑LcrV/Alum) لم تعد تسبب فقدان الوزن أو إشارات التهابية مقلقة في الدم، ومع ذلك ظلت تحمي معظم الحيوانات من تحديات طاعون بجرعات عالية جدًا. ومع ذلك، انخفضت حمايتها قليلًا عند أعلى جرعة عدوى، مما يوحي بأن الأمان تحسّن مع تكلفة طفيفة في الفعالية.
إضافة «دفعة» أنفية لتعزيز الحماية الرئوية
لاستعادة الحماية بل وتعزيزها دون إضافة مكونات قاسية إلى الرئتين، استعان الباحثون بمفهوم جُرِّب أولًا لكوفيد‑19: «تأسيس ثم دفعة» (prime and spike). فُسِّرت الفئران أولًا ومن ثم عُززت بحقن OMV46‑LcrV/Alum الآمنة داخل العضلات، ثم تلقت لاحقًا جرعة صغيرة من بروتين LcrV المنقّى مرشوشة في الأنف، دون محسن إضافي. هذه «الدفعة» عبر الأنف لم تُحدث اضطرابًا في الوزن أو تعداد الدم أو بنية الرئة. ومع ذلك غيرت المناعة في المجاري الهوائية بشكل كامل. بعد المعزِّز الأنفي، احتوت السوائل التي تغسل الرئتين على أجسام مضادة نوعية لـ LcrV بكميات أكبر، بما في ذلك IgA، وهو شكل ملائم بشكل خاص لتغليف وحماية الأسطح المخاطية. كما امتلأت الرئتان بخلايا B الذاكرة المقيمة (التي يمكن أن تتحول سريعًا إلى مصانع مفْرِزة للأجسام المضادة)، وخلايا T الذاكرة المقيمة، والبلعميات المتخصصة التي تجوب الفراغات الهوائية. هذه الخلايا أنتجت مزيجًا من بروتينات الإشارة المفيدة—مثل إنترفيرون‑γ و IL‑17A و IL‑4—التي دعمت معًا إزالة البكتيريا وتوزان الالتهاب.
اختبار الحماية في ظروف صعبة
ترجمت هذه التغيرات المناعية إلى حماية لافتة في العالم الحقيقي. نَجت الفئران التي تلقت فقط حقن OMV المرتبطة بالألوم من تجارب طاعون عديدة، لكن جزءًا منها مات بعد أكبر جرعات بكتيرية. الفئران التي تلقت أيضًا دفعة أنفية من LcrV نجت حتى من أشد العدوى الرئوية، بما في ذلك سلالات تفتقر إلى مكوّن كبسولي رئيسي وفي حيوانات مسنة لديها حالة فرط حمولة بالحديد التي تجعل عادة عدوى Yersinia أسوأ. في هذه الفئران ذات «التأسيس‑والدفعة»، كانت البكتيريا تكاد تكون غائبة تمامًا من الرئتين والكبد والطحال خلال أيام. عندما قام العلماء بتحييد جزيئات إشارة T‑cell الرئيسية، أو حجب حركة الخلايا اللمفاوية من العقد اللمفاوية إلى الأنسجة، انخفضت الحماية بشكل حاد، مما يُظهر أن الخلايا المقيمة في الرئة الناتجة عن النظام ضرورية. نقل هذه الخلايا المقيمة من نوعي B وT إلى فئران أخرى حسّن بقائها مباشرة، ما يبرز أن الخلايا نفسها، وليس الأجسام المضادة الدائرة فقط، توفر الدرع الإضافي.
ذاكرة رئوية طويلة الأمد وآفاق مستقبلية
سأل الفريق أيضًا ما إذا كان معزّز أنفي معطى بعد عدة أشهر من الحقن يمكن أن يوقظ المناعة الرئوية مجددًا. عندما أُخِّرت جرعة LcrV عبر الأنف لنحو ستة أشهر، عززت مرة أخرى الأجسام المضادة وخلايا الذاكرة المقيمة في الرئتين واستعادت الحماية الكاملة ضد تحدٍ شديد بالطاعون الرئوي، بينما كانت الحيوانات التي تلقت الحقن العضلية فقط جزئيًا غير محمية. هذا يوحي بأن الأشخاص الذين طُعّموا سابقًا بلقاح مشابه قد يتلقون، من حيث المبدأ، معزّزًا بسيطًا عبر الأنف أثناء تفشٍّ سريعًا لتحديث دفاعات رئتهم. رغم أن هذه التجارب أُجريت على الفئران فقط، وستتطلب التجارب البشرية نماذج حيوانية إضافية أولاً، يشير العمل إلى استراتيجيات لقاح تجمع بين عملية الحقن التقليدية وسهولة الحماية الموضعية القوية للمناعة المخاطية.
ماذا يعني هذا للناس
بالنسبة للقارئ العام، الرسالة الأساسية هي أن المكان الذي يرسل فيه اللقاح مدافعيك المناعيين قد يكون بنفس أهمية عددهم. من خلال تدريب الجهاز المناعي أولًا بحقنة آمنة ثم توجيه بروتين طاعون رئيسي مباشرة إلى الأنف، تعلم هذه المقاربة ذات الخطوتين الرئتين نفسها كيف تتذكر وتصد بكتيريا الطاعون. إذا نجحت استراتيجيات مماثلة في البشر، فقد توفر وسيلة سريعة وطويلة الأمد للحماية من الطاعون الرئوي—وقد تلهم أيضًا لقاحات جديدة تحمي مجارينا الهوائية بشكل أفضل ضد مجموعة من الجراثيم التنفسية الخطرة.
الاستشهاد: Majumder, S., Das, S., Saqib, M. et al. Intranasal unadjuvanted LcrV boosts parental Yersinia OMV primed lung immunity against pneumonic plague in mice. Nat Commun 17, 1624 (2026). https://doi.org/10.1038/s41467-026-68334-2
الكلمات المفتاحية: الطاعون الرئوي, لقاح مخاطي, معزّز عبر الأنف, مناعة الرئة, Yersinia pestis