Clear Sky Science · ar
نشاط DOT1L يحد من سرعة استطالة النسخ ويعزز توقف RNAPII لتسهيل الطفرنة بواسطة AID
كيف تضبط خلايا جهازنا المناعي بدقة تحريرات الحمض النووي الخطرة
يبتكر جهازنا المناعي أجسامًا مضادة قوية عن طريق تحوير حمضه النووي عمداً، وهي استراتيجية محفوفة بالمخاطر قد تساهم أحيانًا في السرطان. يطرح هذا البحث سؤالًا مخادع البساطة مع تداعيات كبيرة: ما الذي يحدد أين وبأي كفاءة تحدث هذه الطفرات المتعمدة؟ تتلخص الإجابة في بروتين يُدعى DOT1L، الذي يضبط سرعة قراءة الجينات داخل خلايا B وبذلك يساعد في توجيه آلية الطفرة إلى المواقع المناسبة.
تشغيل الطفرة لصقل الأجسام المضادة
عندما تواجه خلايا B عدوى، فإنها تطوّر أجسامها المضادة بطريقتين. تُدخِل تغييرات صغيرة في منطقة الربط للأجسام المضادة لتحسين قوتها في الالتصاق بالجراثيم، وتستبدل ذيل الجسم المضاد لتغيير استجابة الجهاز المناعي. تنطلق كلا التطويرين بإنزيم يُسمى AID، الذي يقطع ويغير الحمض النووي في الجينات النشطة. ورغم أهمية AID للمناعة الجيدة، فإنه يمكن أن يطال أيضًا جينات أخرى، محدثًا كسورًا خطيرة تدفع سرطانات الدم. أظهرت أعمال سابقة أن AID يفضّل الجينات التي تُقرأ بكثافة وتتحكم بها مفاتيح قوية للحمض النووي تسمى المحفزات الفائقة، لكن ذلك لم يفسر بالكامل لماذا تتعرض مجموعة مختارة فقط من الجينات للخطر فعلاً.
علامة كروماتين تميّز الجينات الحسّاسة لـ AID
ركّز المؤلفون على البروتينات التي تتواجد بالقرب من AID داخل النواة. باستخدام تقنية ترميز التقارب في خلايا بشرية، وجدوا أن AID يتجمع قرب DOT1L، إنزيم يضع علامة كيميائية على موضع محدد في بروتينات الهيستون التي يلتف حولها الحمض النووي. هذه العلامة، على الهيستون H3 في الموضع K79، شائعة على الجينات النشطة. في خلايا B الفأرية، حملت الجينات التي يطهّرها AID بشكل متكرر — بما في ذلك جينات الأجسام المضادة والأهداف الخارجية المرتبطة بالسرطان — مستويات مرتفعة بشكل خاص من هذه العلامات التي يصنعها DOT1L. عندما عطّل الباحثون DOT1L في خطوط خلايا B أو أوقفوا نشاطه دوائيًا، تراجع "تبديل الفئة" للأجسام المضادة، وكذلك انخفضت الفواصل التي يسببها AID واندماجات الجينات المعرضة للسرطان بين جينات الأجسام المضادة والجين النمو cMyc. والأهم أن وظيفة DOT1L التحفيزية، لا مجرد وجوده، كانت مطلوبة: فالإصدارات الطافرة التي لم تعد قادرة على وضع علامة الهيستون فشلت في استعادة تبديل الأجسام المضادة الطبيعي.
إبطاء قارئ الجينات لمنح AID وقتًا
للوهلة الأولى، يبدو هذا محيرًا لأن DOT1L مرتبط بالجينات النشطة، ومع ذلك لم يؤدِ إزالته ببساطة إلى إغلاق الجينات. باستخدام طريقة تلتقط نسخ الـRNA الجديدة، اكتشف الفريق أن خلايا B التي تفتقر إلى DOT1L أنتجت فعليًا المزيد من النسخ الناشئة عبر العديد من الجينات المعلّمة بواسطة DOT1L — بالرغم من وجود أقل بقليل من إنزيم قراءة الجينات الرئيسي، بوليميراز RNA II، على تلك الجينات. من خلال دمج قياس الـRNA الناشئ مع خرائط احتلال البوليميراز، استنتجوا أنه، في الظروف الطبيعية، تعمل علامات الهيستون التي يضعها DOT1L كمطبات سرعة لطيفة. فهي تبطئ البوليميراز أثناء تحركه على طول الجين وتطيل التوقفات القصيرة قرب البداية وضمن جسم الجينات الموسومة بـDOT1L. من دون DOT1L، يزداد سرعة البوليميراز وتصبح فترات الوقوف أقصر. وبما أن AID يحتاج نوافذ زمنية قصيرة حين يكون الحمض النووي مكشوفًا ويأخر البوليميراز، فإن هذه الزيادة في السرعة تقلل بشكل مفارق من قدرة AID على الالتصاق وأداء وظيفته، حتى مع ارتفاع النسخ الكلي.
فصل نشاط الجين عن مخاطر الطفرة
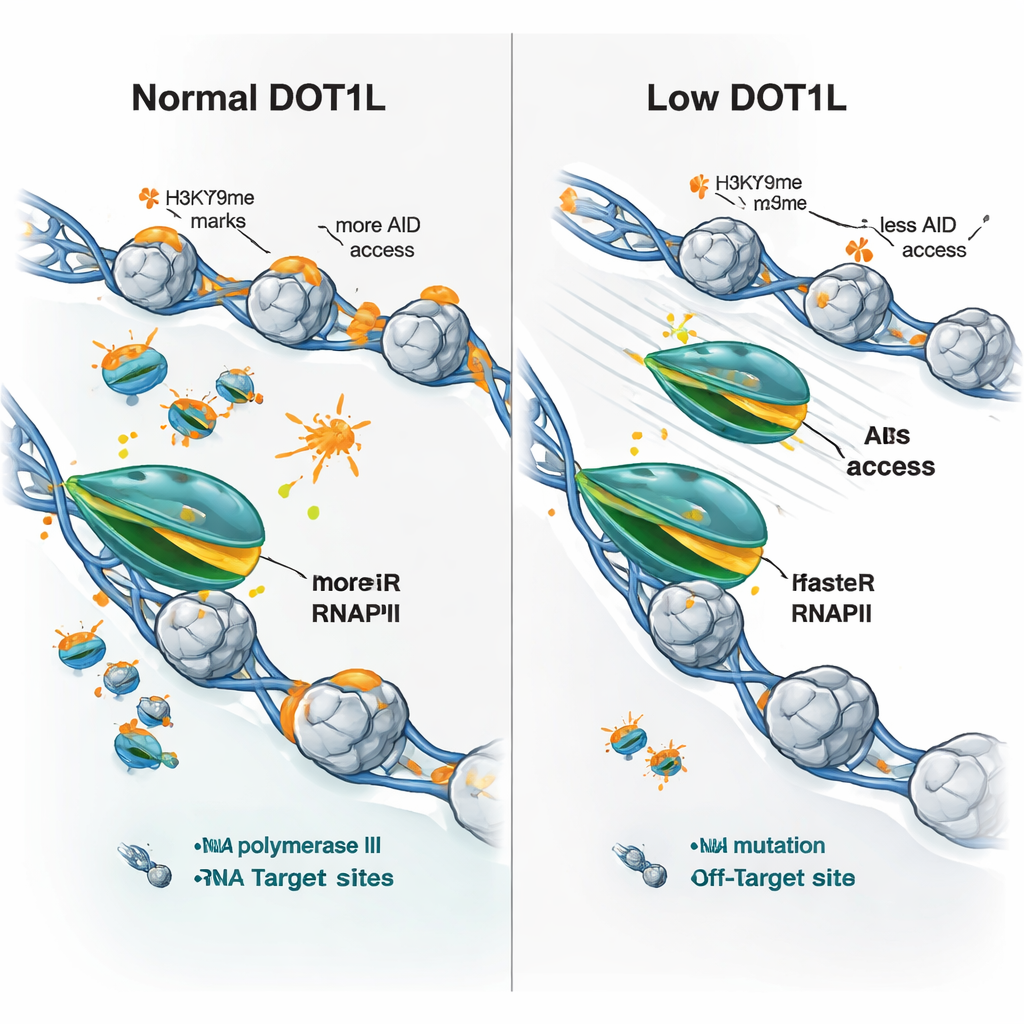
سأل الباحثون بعد ذلك ما إذا كانت هذه التغيرات في السرعة يمكن أن تفسر النمط المختلط لتعبير الجينات الذي يُرى عند فقدان DOT1L — بعض الجينات ترتفع، وأخرى تنخفض. وجدوا أن جميع الجينات الموسومة بـDOT1L تقريبًا تشترك في سمة واحدة في خلايا الطيّ: استطالة أسرع لبوليميراز RNA II. لكن النتيجة كانت تعتمد على الحالة الابتدائية. فقد تميل الجينات البطيئة والضعيفة التعبير إلى إنتاج المزيد من الـRNA عندما يسرع البوليميراز، في حين أن الجينات الطويلة والنشطة بالفعل والتي تمتلك بوليميرازات سريعة أحيانًا تنتج أقل، على الأرجح لأن المرور السريع جدًا يعطل المعالجة أو الإتمام الفعال. والأهم أنه، سواء في جينات الأجسام المضادة أو في أهداف AID الخارجية الكلاسيكية، أدى فقدان DOT1L إلى حركة أسرع للبوليميراز، ودلائل أقل على "توقف" البوليميراز، وانخفاض كبير في احتلال AID، حتى عندما لم تُخفَض مستويات التعبير الجيني نفسها.
لماذا هذا مهم للمناعة والسرطان
معًا، تصوّر هذه الدراسة DOT1L كمنسق حركة دقيق لآلية قراءة الجينات في خلايا B. عبر تثبيته لعلامات هيستونية محددة، يبطئ DOT1L إلى حد طفيف بوليميراز RNA II ويطيل توقفاته، ما يخلق بيئة نسخية تتيح لـAID الانخراط المنتج مع جينات الأجسام المضادة — وللأسف، مع مجموعة محدودة من الجينات الضعيفة الأخرى — لإدخال طفرات. عندما يغيب DOT1L أو يُثبط، يمر البوليميراز بسرعة، مما يترك فرصًا أقل لـAID للعمل، فيضعف ذلك تنوع الأجسام المضادة ويقلل في الوقت ذاته من خطر بعض الترتيبات الضارة. تشرح هذه الرؤية الآلية لماذا يمكن لفقدان DOT1L أن يرفع ويخفض تعبير الجينات في الوقت نفسه، وتربط التحكم الدقيق في سرعة النسخ مباشرةً بالأماكن التي يجرؤ فيها جهازنا المناعي على إعادة كتابة حمضه النووي.
الاستشهاد: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
الكلمات المفتاحية: تنوع الأجسام المضادة, إنزيم AID, DOT1L, نسخ الجينات, خلايا B