Clear Sky Science · ar
التصميم الحاسوبي لسايكلوبروبانازات عامة الاختصاص مع انتقائية متباينة التشكيل الفراغي
لماذا تهم الهياكل الثلاثية الصغيرة للأدوية
السايكلوبروانات — حلقات كربون ثلاثية الذرات — هي وحدات بناء صغيرة مشدودة يمكن أن تغير بشكل كبير سلوك الدواء داخل الجسم. الترتيب الثلاثي الأبعاد الدقيق للذرات (كيمياؤها الفراغية) قد يقرر ما إذا كانت الجزيئة تتحول إلى دواء مفيد أو لبديل غير فعّال أو حتى ضار. تصف هذه الورقة استراتيجية حاسوبية لتصميم إنزيمات قادرة بشكل موثوق على إنتاج جميع الأشكال الثلاثية‑الأبعاد الأربعة الممكنة لهذه الحلقات من نفس المواد الأولية، ما يفتح الباب لاستكشاف أسرع وأنظف لمرشحي الأدوية.
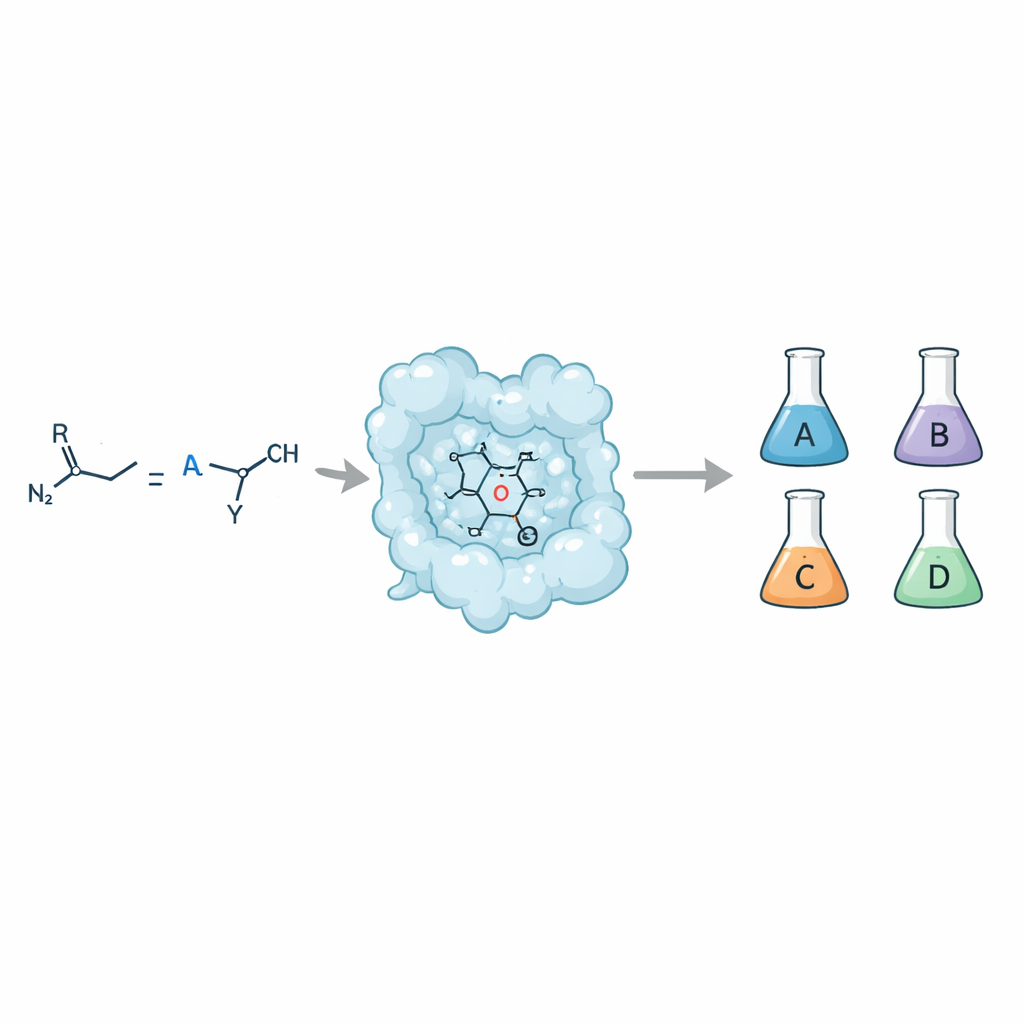
من وصفة واحدة إلى أربعة نتائج مختلفة
عندما يتفاعل رابطة مزدوجة بسيطة (أليفين) مع مانح كاربين مثل مركب ديازوي، يمكن أن يكون الناتج حلقة سايكلوبروان. لكن تلك الحلقة قد تتخذ أربعة أشكال متماكبة مميزة، كل منها يحتوي على نفس الذرات مرتبة بشكل مختلف في الفراغ. يرغب الكيميائيون في الوصول إلى كل واحدة من هذه الأشكال لأن تفاعلها مع الأهداف البيولوجية قد يختلف اختلافاً كبيراً ويؤثر على خصائص الدواء الأساسية مثل الامتصاص والتمثيل والسلامة. يمكن للمحفزات الجزيئية التقليدية أحياناً تحقيق هذا التحكم، لكن القيام بذلك باستخدام إنزيمات — المحفزات التي توفرها الطبيعة — كان صعباً، خاصة عند السعي لتحقيق انتقائية عالية مع تسامح واسع تجاه ركائز مختلفة.
تصميم الإنزيمات على شاشة الحاسوب
طور المؤلفون سير عمل حاسوبي متعدد الحالات قائم على الآلية لمعالجة هذه المشكلة. بدأوا باستخدام حسابات كيميائية كمومية لنمذجة حالات الانتقال العابرة — هياكل عالية الطاقة على طريق التفاعل — لتكوين كل واحد من الأشكال الأربعة للسايكلوبروان. ثم وُضعت هذه النماذج داخل مواقع الفعل في بروتينات مختلفة تحتوي على الهيم، واستخدموا برنامج Rosetta لتصميم البروتينات لتقييم مدى استقرار أو عدم استقرار كل حالة انتقال داخل كل بروتين. بشكل حاسم، كان سجل التصميم يكافئ الطفرات التي تُفضّل حالة الانتقال المرغوبة (تصميم إيجابي) وتُعيق الحالات المتنافسة (تصميم سلبي)، مما علّم الإنزيم فعلياً أن «يفضّل» منتجاً ثلاثي‑الأبعاد واحداً على الآخرين.
بناء صندوق أدوات إنزيمي كامل
باستخدام هذا النهج، أنشأ الفريق عائلة من إنزيمات السايكلوبروباناز «العامة». بدءاً من الميوغلوبين، أعادوا تصميم موقع فعله للحصول على متغيرات تنتج السايكلوبروان trans-(1R,2R) بانتقائية عالية جداً ونشاط جيد عبر أكثر من 20 أليفيناً مختلفاً، بما في ذلك ركائز غير منشّطة وفقيرة إلكترونياً وتتسم بالتحدي. وقد زوّد ميوغلوبين تم هندسته سابقاً المنتج التكميلي trans-(1S,2S). للوصول إلى المنتجين من نوع cis، لجأ المؤلفون إلى بروتينات هيم أخرى. أعادوا تشكيل إنزيم بكتيري P450cam للحصول على متغيرات تعطي بنشاط المنتج cis-(1S,2R)، وأعادوا توظيف إنزيم بشري (indoleamine 2,3‑dioxygenase‑1, IDO1) — الذي لم يُستخدم سابقاً لكيمياء الكاربين — ليفضّل المنتج cis-(1R,2S). إجمالاً، تستطيع هذه المحفزات الحيوية الأربعة تقديم كل متباين سهامي من مجموعة نواتج السايكلوبروان نفسها، غالباً مع تحكّم يصل إلى 99% لكل من الاعتدال الفراغي الثنائي (diastereomer) والمرآة الفراغية (enantiomer).
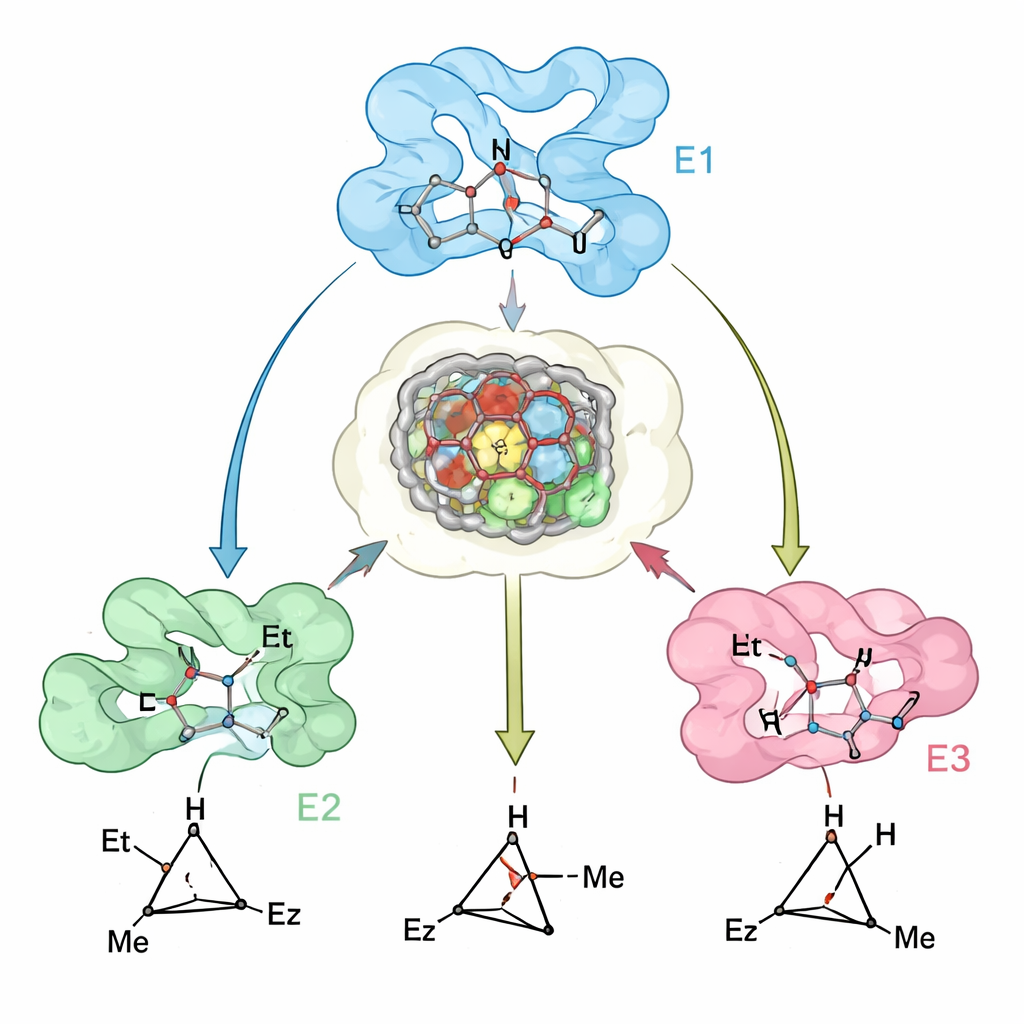
رؤية مدى تطابق التصميم مع الواقع
لاختبار مدى انعكاس نماذجهم الحاسوبية للإنزيمات الحقيقية، حلل الباحثون هياكل بلورية لمتغير ميوغلوبين رئيسي وقارنوها مع الهياكل المتوقعة. كان التطابق قريباً، وأبرزت البيانات التجريبية ميزة دقيقة لكنها مهمة: موقع الفعل في البروتين منظم مسبقاً لاستقبال حالة الانتقال المفضلة، بينما تجعل تغييرات طفيفة في الحلقات واللولب القريب ربط حالة الانتقال «الخاطئة» غير مواتٍ من حيث الطاقة. حيث كانت التنبؤات أقل دقة — مثل بعض الركائز الضخمة — أمكن تتبع الاختلافات إلى حركات في السلسلة الخلفية لم تُلتقط بالكامل في النمذجة، مما يشير إلى مسارات واضحة لتحسين طرق التصميم المستقبلية.
ما يعنيه هذا للأدوية والمحفزات المستقبلية
من خلال الجمع بين نمذجة حالة الانتقال المبنية على الفيزياء وإعادة تصميم البروتين الذكية، يُظهر هذا العمل أنه يمكن برمجة النتائج الفراغية لتفاعلات محكومة بواسطة الإنزيمات مسبقاً، بدلاً من اكتشافها فقط عبر التجربة والخطأ والتطوّر. توفر مجموعة السايكلوبروبانازات الناتجة وسيلة عملية للكيميائيين لصنع مجموعات كاملة من متباينات السايكلوبروان من طيف واسع من الأليفينات المبدئية، مما يبسط بشكل كبير دراسات العلاقة بين البنية والنشاط في اكتشاف الأدوية وتخليق المنتجات الطبيعية. وينبغي أن تكون نفس الاستراتيجية قابلة للتكييف مع أنواع إنزيمات وفئات تفاعلات أخرى، مما يسرّع ابتكار محفزات حيوية تمنح تحكماً ثلاثي‑الأبعاد دقيقاً فوق جزيئات معقّدة.
الاستشهاد: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
الكلمات المفتاحية: التحفيز الحيوي, تكوُّن السايكلوبروبان, تصميم الإنزيمات, الكيمياء الفراغية, بروتينات الهيم