Clear Sky Science · ar
تحول طوبولوجي منظَّم زمانياً ومكانياً في الهيدروكسيدات المزدوجة الطبقية يمكّن التمعدن التآزري لـ AsIII/Cd2+
تنظيف مادتين سامّتين عن طريق واحد
يُعد الزرنيخ والكادميوم من أخطر المعادن السامة في مياه الشرب والتربة حول العالم. يضرّان بالأعضاء ويزيدان من خطر الإصابة بالسرطان، ومن المعروف أنهما صعبا الإزالة، خاصة عندما يظهران معاً. تصف هذه الدراسة مادة جديدة شبيهة بالمعادن يمكنها استخلاص الملوِّثين الاثنين من الماء والتربة بكفاءة أكبر بكثير من الطرق الحالية، وتعمل بشكل أفضل حتى عندما يتواجد السّمّان في الوقت نفسه.
لماذا الزرنيخ والكادميوم صعبان جداً
يتصرّف الزرنيخ والكادميوم بشكل مختلف جداً في الماء. الشكل الأكثر تنقّلاً من الزرنيخ، المسمّى أرسينيت، غير مشحون وينسلّ بسهولة عبر الفلاتر، بينما يحمل الكادميوم شحنة موجبة ويلتصق بقوة بالعديد من الأسطح المعدنية. في معظم مواد التنظيف، يتسابق الكادميوم إلى الداخل أولاً ويحتل المواقع التفاعلية الرئيسية، ما يمنع الأرسينيت من الالتصاق أو التحول إلى شكل أقل سمية. هذا يعني أن التقنيات الحالية غالباً ما تزيل عنصراً واحداً على حساب الآخر، مما يضطر المهندسين إلى قبول مقايضات أو استخدام علاجات معقّدة متعددة الخطوات.
إسفنج معدني يغيّر شكله
عالج الباحثون هذه المشكلة بإعادة تصميم فئة من المواد المعروفة باسم الهيدروكسيدات المزدوجة الطبقية—معادن تتكوّن من صفائح مشحونة موجبة مع ماء وأيونات محشورة بينها. عبر تسخين هذه المعادن، أنشأوا شكلًا مُقاربًا يُدعى أكسيد مزدوج طبقي مليئًا بالعيوب على مقياس ذري ويكون شديد الرغبة في التفاعل مع الماء. عند وضع الأكسيد في الماء، ماصّ بسرعة جزيئات الماء في كامل حجمه، مكوّناً مجموعات هيدروكسيل وفيرة (مواقع –OH التفاعلية) بدلاً من الاقتصار على تزيين السطح الخارجي فحسب. تعمل هذه المواقع التفاعلية الداخلية كالاسفنج ثلاثي الأبعاد لأيونات المعادن بدلاً من طبقة رقيقة، ما يزيد بشكل كبير من قدرة المادة على التقاط الملوِّثات.
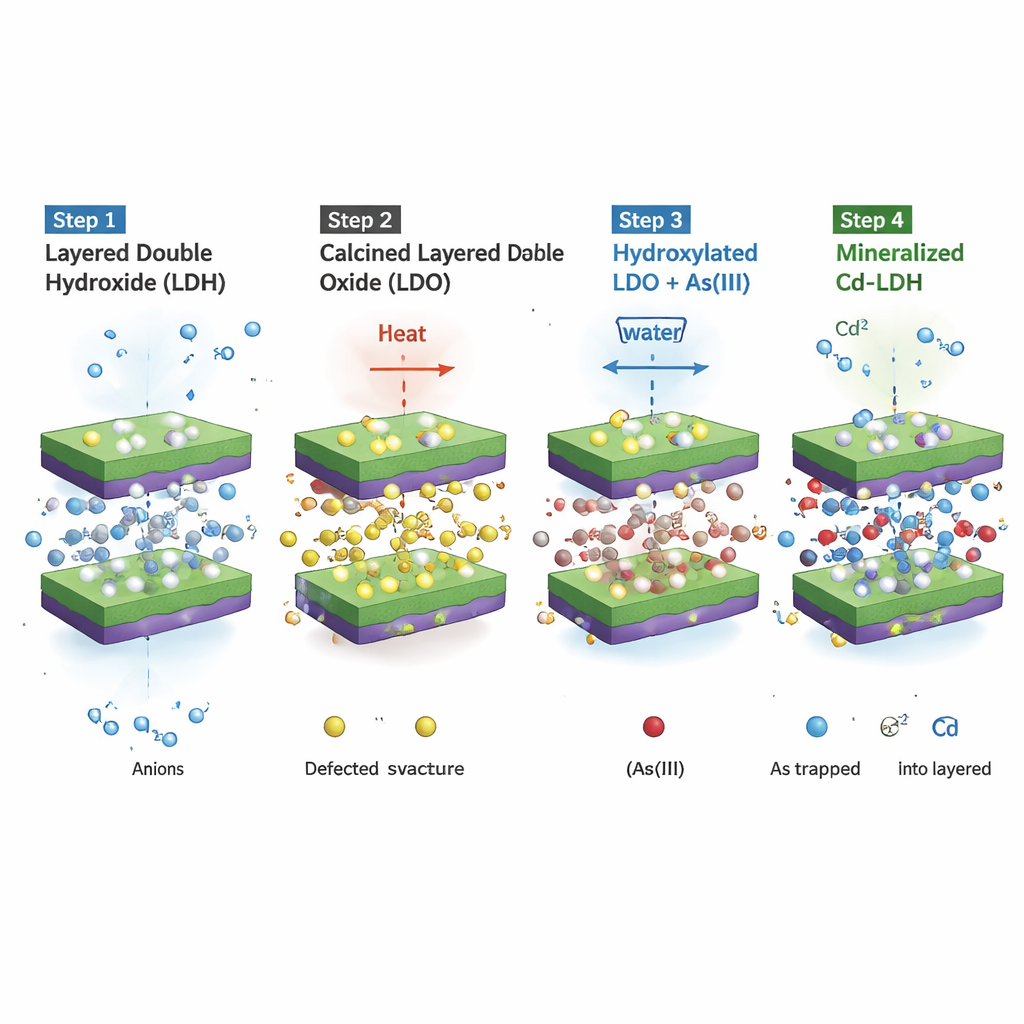
تحويل الزرنيخ والكادميوم إلى مساعدين لا متنافسين
في اختبارات وُجد فيها الأرسينيت والكادميوم معاً، التقطت المادة الجديدة، المصنوعة من المغنيسيوم والمنغنيز (MgMn-LDO)، ما يصل إلى حوالي 822 ميليغراماً من الزرنيخ و1896 ميليغراماً من الكادميوم لكل غرام من المادة—وهو أفضل بعدّة مرات من أفضل الممتصات المبلَّغ عنها سابقاً. بشكل مفاجئ، توقّف التنافس بين الملوِّثين وبدأا يساعدان بعضهما البعض. سرّع وجود الكادميوم إزالة الأرسينيت إلى حد أن العملية وصلت إلى حالة توازُنية خلال دقائق بدل ساعات، بزيادة في معدلات التفاعل تقارب 181 مرة مقارنةً بالزرنيخ وحده. استطاعت المادة تنظيف المياه الملوَّثة إلى مستويات عند أو أقل من إرشادات منظمة الصحة العالمية، حتى عند انطلاقها من مستويات تلوّث عالية نسبياً، وأدّت أداءً جيداً في محاليل مخبرية ومياه صرف مناجم وترب حقيقية.
إعادة ترتيب داخلية رباعية الخطوات
يكمن السرّ في سلسلة منظَّمة بعناية من التحولات الداخلية التي تتكشف داخل كل جسيم. أولاً، يحوّل التسخين الهيدروكسيد الطبقي الأصلي إلى أكسيد غنيّ بالعيوب. ثانياً، يدفع التماس مع الماء «الهيدروكسلة بالجُملَة» (bulk hydroxylation)، مما يملأ المادة بمجموعات –OH المشتقة من الماء ويهيئها للتفاعل. ثالثاً، يصل الأرسينيت ويتأكسد على مواقع المنغنيز إلى شكل أقل سمّية وسالب الشحنة هو الفوسفات (أرسينات)؛ في الوقت نفسه تتدفّق الإلكترونات إلى المنغنيز، وتقوم البنية بـ«تذكّر» وترميم ترتيبها الطبقي الأصلي. في هذه الحالة المُرمَّمة، يُحشى الزرنيخ بين الطبقات ويُثبت بقوة. وبعد ذلك فقط تحدث الخطوة الرابعة: يبدأ الكادميوم في الاستبدال مكان ذرات المغنيسيوم داخل الطبقات، في عملية شبيهة بالاستبدالات الطبيعية في المعادن الجيولوجية، مكوّناً شكلاً نهائياً أكثر استقراراً وممعدناً يقاوم التسرب.
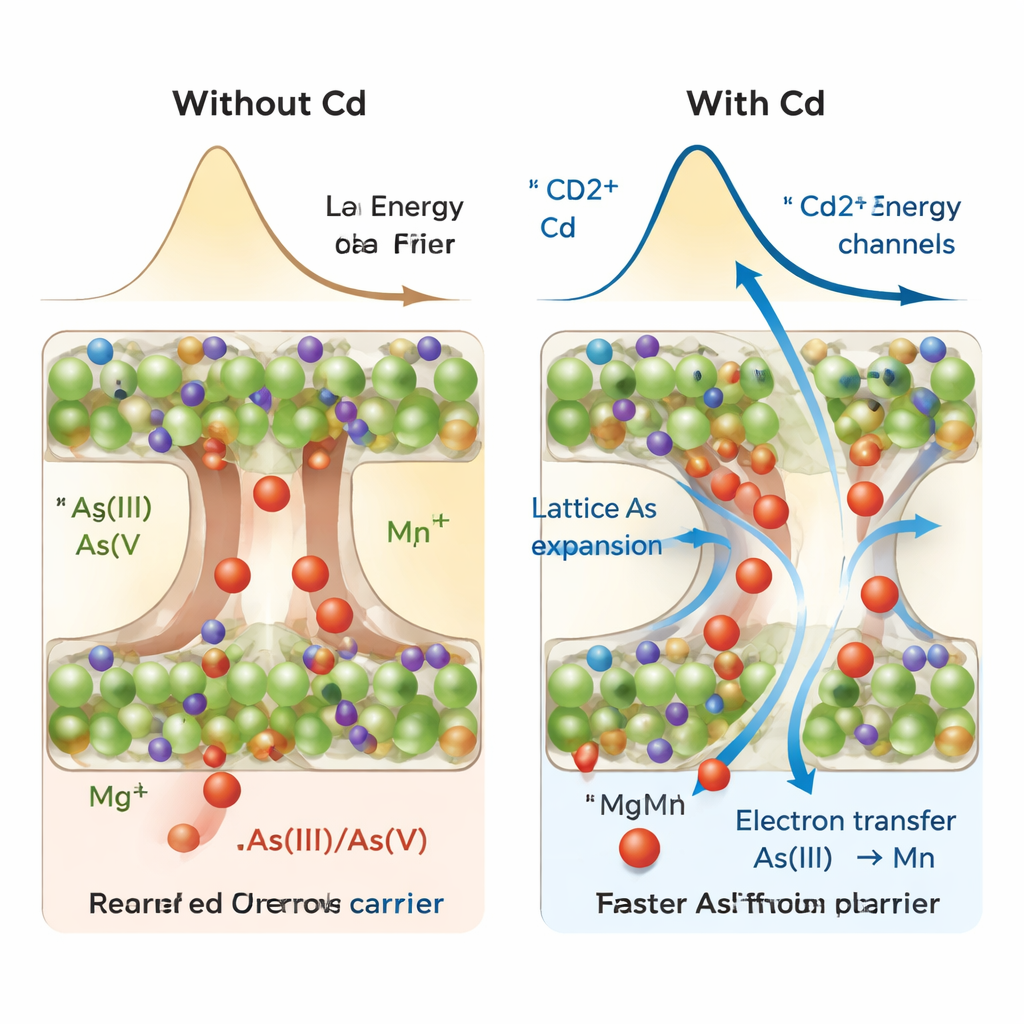
كيف يسرّع الكادميوم احتباس الزرنيخ
لا يقتصر تبادل الذرات بواسطة الكادميوم على تثبيت الكادميوم نفسه فحسب. بما أن أيونات الكادميوم أكبر قليلاً من المغنيسيوم، فإن استبدالها يوسّع الحيز البلّوري ويوسّع قنوات الانتشار داخل المادة. تظهر المحاكاة الحاسوبية وتجارب الطيف أن هذا التوسع يخفض حاجز الطاقة لتحرّك أنواع الزرنيخ إلى أعماق البنية عبر مسارات معينة، وفي الوقت نفسه يضعف قليلاً روابط معدن–أكسجين محددة. هذا يجعل من الأسهل انتقال الإلكترونات من الأرسينيت إلى المنغنيز وتحويل الزرنيخ وتثبيته بين الطبقات. باختصار، يعيد الكادميوم تشكيل البنية الداخلية بحيث يمكن للزرنيخ أن يهاجر ويترسّخ بصورة أسرع وأكثرِ شمولاً.
من اكتشاف مختبري إلى تنظيف واقعي
بما أن المادة مصنوعة من عناصر شائعة نسبياً وبخطوة تسخين بسيطة، يمكن إنتاجها على مقياس يصل إلى الكيلوغرامات على الأقل. أظهرت اختبارات ميدانية على مياه صرف مناجم وترب صناعية شديدة التلوّث انخفاضات كبيرة—غالباً حوالي 90% أو أكثر—في كل من الزرنيخ والكادميوم لتفي بمعايير الري أو مياه الشرب. للغير مختصين، الخلاصة أن المؤلفين ابتكروا معدنًا ذكيًا وقابلاً للتكيّف يعيد ترتيب نفسه زمنياً ومكانياً بحيث يتم تحييد الزرنيخ أولاً ثم يُدمَج الكادميوم في البنية. هذا الترتيب المبتكر يحوّل معدنين خطيرين إلى حلفاء متبادلِين في احتجازهما، ويفتح الطريق نحو تنظيف أكثر فاعلية وعملية للتلوّث المعقّد بالمعادن.
الاستشهاد: Zheng, M., Du, H., Cao, X. et al. Spatiotemporally ordered topological transformation in layered double hydroxides enables synergistic mineralization of AsIII/Cd2+. Nat Commun 17, 1619 (2026). https://doi.org/10.1038/s41467-026-68326-2
الكلمات المفتاحية: إزالة الزرنيخ, تلوّث الكادميوم, تنقية المياه, هيدروكسيد مزدوج طبقي, إزالة المعادن الثقيلة