Clear Sky Science · ar
إنزيم جليسيرول-3-فوسفات أسيلترانسفيراز يزيد سمية α-سينوكلين عن طريق زيادة بيروكسدة الدهون
لماذا تهم الدهون في الدماغ لمرض باركنسون
عادةً ما يوصف مرض باركنسون كمشكلة في بروتين يسمى ألفا‑سينوكلين الذي يتكتل ويتلف خلايا الدماغ المسؤولة عن الحركة. تُظهر هذه الدراسة أن دهون الدماغ—وخاصة طريقة تصنيعها وتلفها—تؤدي دورًا أقوى مما كان متوقعًا في مدى سُمّية ألفا‑سينوكلين. من خلال الكشف عن إنزيم يصنع الدهون يزيد إصابة الخلايا العصبية، تشير النتائج إلى مسار دوائي جديد يمكن استهدافه قد يكمل الجهود الحالية لمعالجة باركنسون من جذوره.
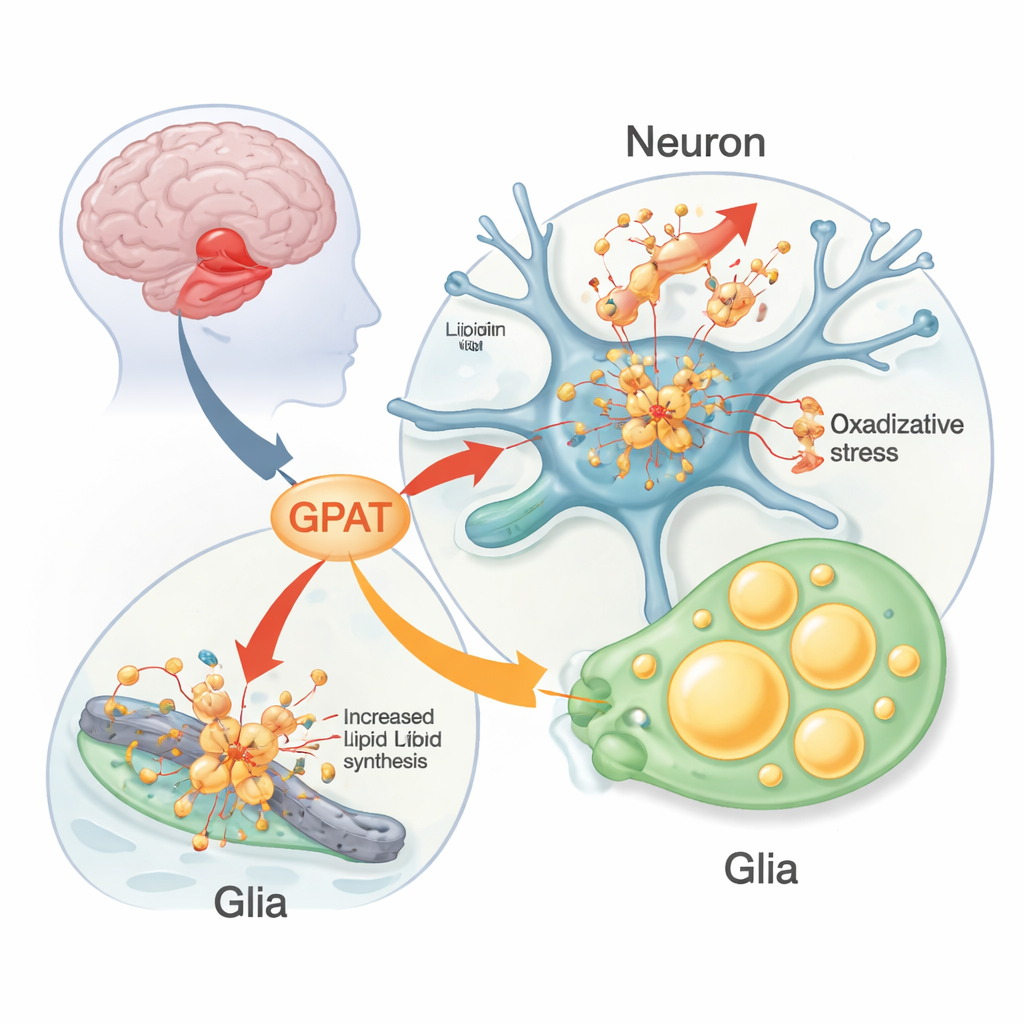
بروتين يتصرف بشكل خاطئ في باركنسون
يفقد الأشخاص المصابون بباركنسون تدريجيًا الخلايا العصبية المنتجة للدوبامين في منطقة عميقة من الدماغ تنسق الحركة. داخل هذه الخلايا المحتضرة، يجد العلماء غالبًا رواسب كثيفة تُسمى أجسام لويي، مليئة بالبروتين ألفا‑سينوكلين. في بعض العائلات النادرة، تؤدي طفرات أو نسخ إضافية من جين ألفا‑سينوكلين إلى باركنسون بشكل مباشر، لكن المتغيرات الجينية الشائعة في ذلك الجين تزيد الخطر بشكل طفيف فقط. هذا يقترح أن جينات ومسارات أخرى تعدّل مدى ضرر ألفا‑سينوكلين. تتزايد الأدلة التي تشير إلى أن الدهون—الدهون والجزيئات الشبيهة بالدهون التي تشكل أغشية الخلايا ومخازن الطاقة—شركاء محوريون في كل من تجمع ألفا‑سينوكلين ووفاة الخلايا العصبية.
اكتشاف إنزيم دهني قوي في نماذج ذبابة الفاكهة
استخدم الباحثون ذباب الفاكهة المعدّل لإنتاج ألفا‑سينوكلين البشري في جهازه العصبي كنموذج حي للاختبار. تطور لدى هذه الذباب مشكلات شبيهة بباركنسون: خسارة الخلايا العصبية المنتجة للدوبامين، صعوبة في التسلق، واضطراب في إيقاعات النشاط اليومية. عدّل الفريق بشكل منهجي نسخ ذبابة من جينات مخاطرة باركنسون البشرية لمعرفة أيها يغير تأثير ألفا‑سينوكلين. برز جين واحد: يُدعى mino، الذي يصنع شكلًا ميتوكوندريًا من إنزيم جليسيرول‑3‑فوسفات أسيلترانسفيراز (GPAT). يقع GPAT عند نقطة الدخول لبناء الفسفوليبيدات والدهون الثلاثية—الدهون التي تشكل الأغشية وقطرات الدهون. عندما قلل الفريق نشاط mino في الخلايا العصبية، احتفظت ذبابة ألفا‑سينوكلين بالمزيد من خلايا الدوبامين وتحركت بشكل أفضل لفترة أطول؛ أما زيادة mino فكان لها تأثير معاكس وضار.
الدهون المتضررة، الميتوكوندريا المتوترة، وقطرات الدهون في الخلايا الدبقية
عند التعمق أكثر، وجد العلماء أن GPAT يؤثر في مقدار الضرر التأكسدي المتراكم في دهون الدماغ. في ذباب ألفا‑سينوكلين المحتفظ بها عند درجة حرارة أعلى (ما يزيد من مظاهر المرض)، ارتفعت بيروكسدة الدهون—وهي «صدأ» كيميائي للدهون—في أغشية الدماغ. خفض mino قلص هذا الضرر، في حين أن فرط التعبير عنه زاد منه؛ وبدون ألفا‑سينوكلين، كان لتغيير mino تأثير ضئيل. عكست مؤشرات موت الخلايا في منطقة الدماغ البصرية هذا النمط. كما رصد الفريق تراكمًا ملفتًا لقطرات الدهون—كرات صغيرة لتخزين الدهون—ليس داخل الخلايا العصبية نفسها بل في الخلايا الدبقية المجاورة. توسعت هذه القطرات مع تقدم العمر في ذباب ألفا‑سينوكلين وتعدّلت بواسطة إنزيمات تبني أو تكسر الدهون الثلاثية، مما يبرز شراكة أيضية نشطة بين الخلايا العصبية والخلايا الدبقية تحت الضغط.
إعادة توصيل الأيض وتكتل ألفا‑سينوكلين
كشفت قياسات المستقلبات من أدمغة الذباب أن تعبير ألفا‑سينوكلين مرتبط بعنق زجاجة في دورة إنتاج الطاقة الخلوية: تراكم بقوة لمادتين وسطيتين في دورة ثلاثي الكربوكسيلات (TCA) هما السترات وإيزوسيتريت، بينما تحوّلت خطوات لاحقة بتغيّرات أقل وضوحًا. كما ارتفعت مستويات اللاكتات، بما يتوافق مع زيادة تحطيم الجلوكوز. في الوقت نفسه، أظهر تحليل دقيق للدهون تغيّرات في توازن الفسفوليبيدات الغشائية وتركيب أحماضها الدهنية، مفضلاً أنواعًا أكثر عرضة للضرر التأكسدي. عندما قلّل الفريق عدة إنزيمات GPAT—بما في ذلك mino في الميتوكوندريا وإنزيمات ذات صلة على الشبكة الإندوبلازمية—ظل ألفا‑سينوكلين يتراكم، لكن ميله لتكوين أوليغومرات عالية الرتبة (حزم متعددة البروتينات) انخفض، وأظهرت الميتوكوندريا علامات أقل على إجهاد الأكسيد النشط و«الشيخوخة».
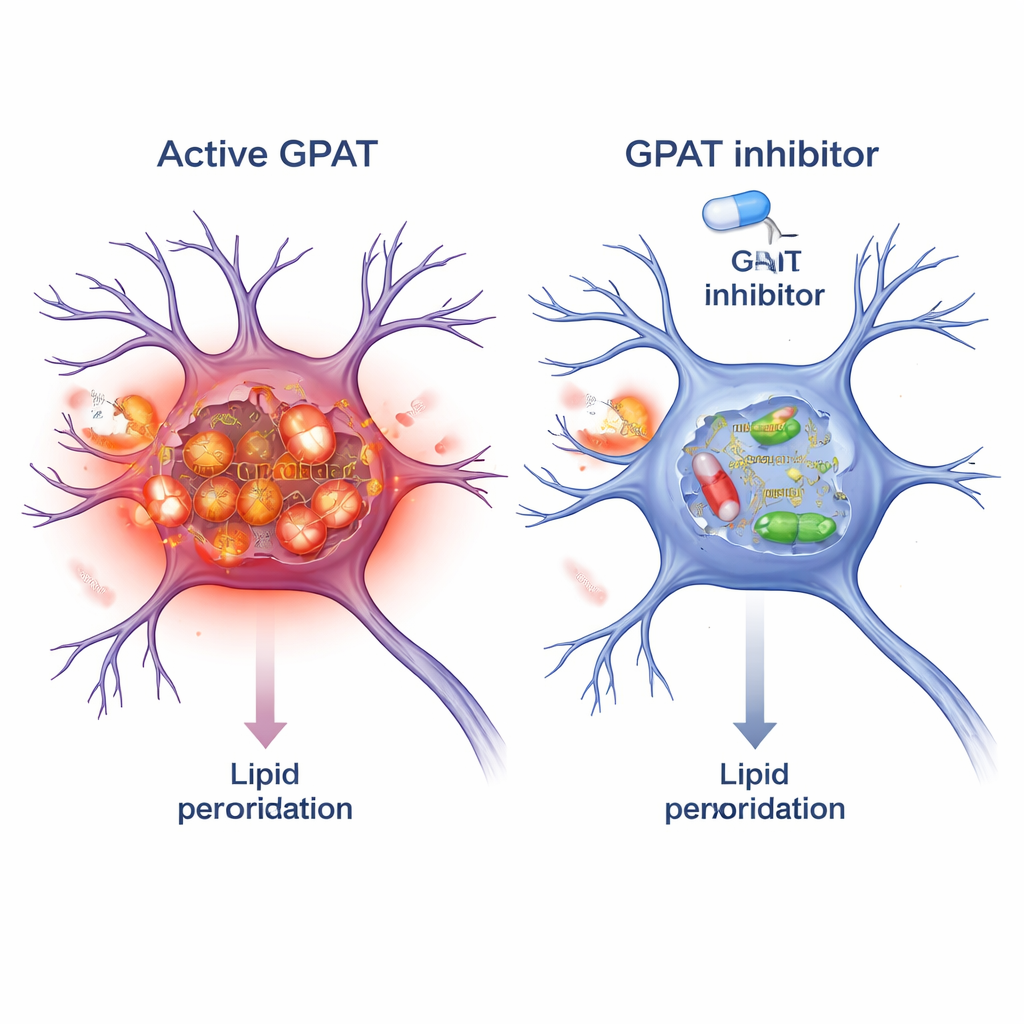
حجب GPAT كاستراتيجية وقائية
بما أن GPAT إنزيم، فيمكن استهدافه بأدوية جزيئية صغيرة. اختبر الباحثون FSG67، وهو مثبط GPAT موجود طُور أصلاً لمعالجة السمنة والسكري. في ذباب ألفا‑سينوكلين، أعاد إضافة FSG67 إلى الغذاء فوائد خفض GPAT الوراثي: تحسّن الحركة، وبقاؤها الأفضل لخلايا الدوبامين، وانخفاض أوليغومرات ألفا‑سينوكلين الضارة، وانخفاض إجهاد الأكسدة الميتوكوندري. وللتحقق مما إذا كان هذا المفهوم ينطبق على الثدييات، عالَجوا خلايا عصبية من أدمغة الفئران في زراعة بمخازن ألياف ألفا‑سينوكلين المسبقة التشكّل، التي تُوقظ تجمعات سامة. خفّض العلاج المشترك مع FSG67 تراكم ألفا‑سينوكلين المفسفر، وخفّض عدة مؤشرات مستقلة لبيروكسدة الدهون داخل هذه الخلايا العصبية.
ماذا يعني هذا للأشخاص المصابين بباركنسون
بعبارات بسيطة، تُظهر هذه الدراسة أن طريقة تعامل الدماغ مع الدهون يمكن أن تضبط سمية ألفا‑سينوكلين صعودًا أو هبوطًا. عندما يكون GPAT نشطًا جدًا، تُبنى دهون أكثر عرضة للتلف داخل الأغشية وقطرات التخزين، مما يجعلها أسهل للتأكسد؛ ويبدو أن بيئة الدهون التالفة هذه تُفضل الأشكال الضارة من ألفا‑سينوكلين وتجهد الميتوكوندريا، مصانع الطاقة الخلوية. إعادة خفض نشاط GPAT—وراثيًا أو بدواء—تحوّل التوازن نحو «صدأ» دهني أقل، وتجميعات بروتينية سامة أقل، وخلايا عصبية أكثر صحة. مع أن هذه النتائج مبكرة ومستمدة من ذباب ونماذج خلوية للفئران، فإنها تبرز أيض الدهون، وGPAT بشكل خاص، كزاوية واعدة جديدة لعلاجات باركنسون قد تكمل استراتيجيات تستهدف ألفا‑سينوكلين مباشرة.
الاستشهاد: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
الكلمات المفتاحية: مرض باركنسون, ألفا-سينوكلين, بيروكسدة الدهون, مثبط GPAT, الضمور العصبي